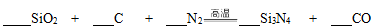- 化学基本概念和基本理论
- 共1765题
6.己知在碱性溶液中可发生如下反应:
2R(OH)3 + 3C1O- + 4OH- = 2RO4n-+3Cl- +5H2O。则RO4n-中 r 的化合价是
正确答案
知识点
有机物X是合成药物沐舒坦的中间体,其合成路线如下:
请回答:
8.X中含氮官能团的名称是 ▲ 。
9.反应①的试剂和条件是 ▲ 。
10.反应①~⑤中属于取代反应的是 ▲ (填反应序号)。
11.反应⑤的化学方程式 ▲ 。
12.反应②和③的顺序不能颠倒,理由是 ▲ 。
13.写出符合下列要求A的所有同分异构体结构简式 ▲ 。
i. 苯环上的一氯取代物有四种;
ii. 既能与酸反应,又能与碱反应,且与NaOH反应的物质的量之比为1∶2。
正确答案
氨基
解析
根据X的结构简式可知,X中含氮官能团的名称是氨基,故答案为:氨基;
考查方向
解题思路
比较甲苯和A的分子式,结合X的结构可知,甲苯与硝酸发生硝化反应生成A为



易错点
本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度中等。
正确答案
浓硝酸和浓硫酸、加热或水浴加热
解析
反应①是甲苯的硝化反应,所用的试剂和条件是浓硝酸和浓硫酸、加热或水浴加热,故答案为:浓硝酸和浓硫酸、加热或水浴加热;
考查方向
解题思路
比较甲苯和A的分子式,结合X的结构可知,甲苯与硝酸发生硝化反应生成A为



易错点
本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度中等。
正确答案
①④⑤
解析
根据上面的分析可知,反应①~⑤中属于取代反应的是①④⑤,故答案为:①④⑤;
考查方向
解题思路
比较甲苯和A的分子式,结合X的结构可知,甲苯与硝酸发生硝化反应生成A为



易错点
本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度中等。
正确答案
解析
应⑤的化学方程式为

考查方向
解题思路
比较甲苯和A的分子式,结合X的结构可知,甲苯与硝酸发生硝化反应生成A为



易错点
本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度中等。
正确答案
防止氨基被氧化
解析
因为氨基容易被氧化,所以反应②和③的顺序不能颠倒,故答案为:防止氨基被氧化;
考查方向
解题思路
比较甲苯和A的分子式,结合X的结构可知,甲苯与硝酸发生硝化反应生成A为



易错点
本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度中等。
正确答案
解析
根据条件i.苯环上的一氯取代物有四种,说明苯环上有两个处于间位或邻位的不同基团;ii.能与酸反应,说明有氨基,能与碱反应,说明有酯基或羧基,且与NaOH反应的物质的量之比为1:2,则符合要求A的所有同分异构体结构简式为

考查方向
解题思路
比较甲苯和A的分子式,结合X的结构可知,甲苯与硝酸发生硝化反应生成A为



易错点
本题考查了有机框图推断以及有机化学方程式的书写,据官能团的性质以及所给流程图正确的判断各物质的结构简式是解题的关键,题目难度中等。
7.下列有关物质的性质或该物质性质的应用均正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图。该拒食素与下列某试剂充分反应,所得有机物分子中官能团个数增加,则该试剂是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.按要求完成下列填空
Ⅰ.已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) ΔH=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的ΔH=( )
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:
①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化
b.υ正(
c.混合气体的平均相对分子质量不发生变化
d.
②在某温度下,反应物的起始浓度分别为:c(CO)= 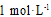
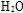

(3)熔融碳酸盐燃料电池的电解质为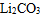
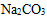
Ⅱ.氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得: 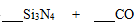
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了30mol氮气,反应生成了5mol一氧化碳,则此时混合气体的平均摩尔质量是( )。
(3)氮化硅陶瓷的机械强度高,硬度接近于刚玉(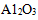
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途
正确答案
Ⅰ.
(1)-2219.9 kJ/mol
(2)b d 0.5
(3)CO-2e_+CO32-=2CO2
Ⅱ.
(1)3 6 2 1 6
(2)28 g/mol
(3) AC
解析
解析已在路上飞奔,马上就到!
知识点
3.右下表为元素周期表的一部分,其中A、X、Y、W、Z为短周期元素,W元素的核电荷数为X元素的2倍。据此,下列说法中错误的是
正确答案
解析
A、X、Y、W、Z为短周期元素,由元素周期表可知:X应位于第二周期,且应处于周期表中右半部分,W与X处于同一主族,且W元素原子的核电荷数为X元素的2倍,那么X为O,W为S,可知Y为Si、Z为P、T为As,A为Cl,B为Br,
A.非金属性X>W>Z,对应气态氢化物的热稳定性变化减弱;电子层越多原子半径越大,则原子半径为Z>W>X,故A正确;
B.电解A的钠盐溶液,生成NaOH、氢气、氯气,阴极生成NaOH,为使钠离子向阴极移动,选阳离子交换膜,故B错误;
C.S可以单质存在,非金属性Y、Z、W、A逐渐增强,对应最高价氧化物的水化物的酸性依次递增,故C正确;
D.As位于金属与非金属性的交界处,则T元素的单质具有半导体特性,As的化合价为+3价时为中间价态,则T2X3具有氧化性和还原性,故D正确
考查方向
位置结构性质的相互关系应用;元素周期律和元素周期表的综合应用
解题思路
A、X、Y、W、Z为短周期元素,由元素周期表可知:X应位于第二周期,且应处于周期表中右半部分,W与X处于同一主族,且W元素原子的核电荷数为X元素的2倍,那么X为O,W为S,可知Y为Si、Z为P、T为As,A为Cl,B为Br,结合元素周期律与元素化合物结构与性质解答
易错点
D项:As2O3中据价态推断氧化性和还原性
教师点评
本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、性质、元素周期律等为解答的关键,侧重分析与应用能力的考查,注意W、X为元素推断的突破口,题目难度不大
知识点
6.A、B、C、D、E五种元素分属于三个短周期,且原子序数依次增大。A、C同主族,可形成离子化合物CA;B、D同主族,且D的原子序数是B的2倍,则下列说法正确的是
正确答案
解析
A、B、C、D、E五种元素分属于三个短周期,且原子序数依次增大.A、C同主族,可形成离子化合物CA,则A为H,C为Na;B、D同主族,且D的原子序数是B的2倍,则B为O,D为S,结合原子序数为E为Cl,
A.B元素在周期表中的位置为第二周期ⅥA族,故A错误;
B.D的氧化物为二氧化硫,与有色物质化合生成无色物质,E的单质为氯气,与水反应生成HClO具有强氧化性,漂白的原理不相同,故B错误;
C.由A、B、C、D组成的两种盐分别为硫酸氢钠、亚硫酸氢钠,反应可产生SO2气体,故C正确;
D.上述元素的非金属气态氢化物还原性最强的是D,还原性S2->Cl-,故D错误
考查方向
位置、结构与性质的应用
解题思路
A、B、C、D、E五种元素分属于三个短周期,且原子序数依次增大.A、C同主族,可形成离子化合物CA,则A为H,C为Na;B、D同主族,且D的原子序数是B的2倍,则B为O,D为S,结合原子序数为E为Cl,然后结合元素周期律及元素化合物来解答
易错点
D项:非金属气态氢化物还原性
教师点评
本题考查位置、结构与性质的应用,把握元素的位置、元素化合物知识推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大
知识点
6.四种短周期元素X、Y、Z、W的原子序数依次增大,X、W原子序数之和等于Y、Z原子序数之和。X、W两元素位于同一主族,Y元素是其所在周期中原子半径最大的元 素(惰性气体元素除外),Z的单质是银白色固体,易导电,常温下不易溶于浓硫酸。下列有关推断错误的是
正确答案
解析
四种短周期元素X、Y、Z、W的原子序数依次增大,Z单质是银白色固体,易导电,常温下不易溶于浓硫酸,短周期元素中能够与浓硫酸发生钝化的为金属Al,则Z为Al元素;Y元素是其所在周期中原子半径最大的元素(惰性气体元素除外),则Y位于ⅠA族,为Li或Na元素;W的原子数大于Al,又X、W两元素位于同一主族,则X、W族序数大于Ⅲ,故Y只能为Na元素;X、W原子序数之和等于Y、Z原子序数之和,则X、W的原子序数之和=11+13=24,设X、W的原子序数分别为x、x+8,则x+x+8=24,解得x=8,则X为O、W为S元素,
A.X为O元素,其氢化物为水,分子中存在氢键,导致水的沸点较高,故A正确;
B.非金属性O>S,非金属性越强,对应离子的还原性越弱,则阴离子还原性:X<W;金属性Na>Al,金属性越强,对应离子的氧化性越弱,则阳离子氧化性:Z>Y,故B错误;
C.X为O、Y为Na,二者形成的过氧化钠为离子化合物,过氧化钠中含有共价键,故C正确;
D.Z为Al、W为S,硫化铝在水溶液中发生双水解反应,所以硫化铝在水溶液中不能稳定存在,故D正确
考查方向
原子结构与元素周期律
解题思路
四种短周期元素X、Y、Z、W的原子序数依次增大,Z单质是银白色固体,易导电,常温下不易溶于浓硫酸,短周期元素中能够与浓硫酸发生钝化的为金属Al,则Z为Al元素;Y元素是其所在周期中原子半径最大的元素(惰性气体元素除外),则Y位于ⅠA族,为Li或Na元素;W的原子数大于Al,又X、W两元素位于同一主族,则X、W族序数大于Ⅲ,故Y只能为Na元素;X、W原子序数之和等于Y、Z原子序数之和,则X、W的原子序数之和=11+13=24,设X、W的原子序数分别为x、x+8,则x+x+8=24,解得x=8,则X为O、W为S元素,据此结合元素周期律知识进行解答
易错点
A项:氢键的存在导致沸点较高
教师点评
本题考查了原子结构与元素周期律的应用,题目难度中等,根据题干信息正确推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系
知识点
下列有关化学用语表示正确的是
正确答案
解析
有关化学用语常涉及常见物质的组成和结构,尤其是一些常见物质电子式、结构式、结构简式及模型等等,内容比较基础。
知识点
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。已知:
①反应C+G
②I是一种常见的温室气体,它和E可以发生反应:2E+I
为60%。
回答问题:
(1)①中反应的化学方程式为__________;
(2)化合物I的电子式为__________,它的空间结构是__________;
(3)1。6g G溶于盐酸,得到的溶液与铜粉完全反应,计算至少需铜粉的质量(写出粒子方程式和计算过程);
(4)C与过量NaOH溶液反应的离子方程式为__________;
(5)E在I中燃烧观察到的现象是__________。
正确答案
(1)Al+ Fe2O3
(2)
(3)2Fe3++Cu=2 Fe2++ Cu2+ n(Fe2O3)=0.01mol,依据离子方程式,则n(Cu )= 0.01mol,m(Cu )=0.64g。
(4)2 Al + 2OH- + 2 H2O=2AlO2- + 3H2↑ AlO2- + CO2 + 2H2O = Al(OH)3↓+ HCO3-
(5)剧烈燃烧,放出热量,生成黑色固体和白色固体。
解析
该题有多处“题眼”。依据题目信息C、B是单质,G、H是二元化合物,
知识点
谁是最宝贵的资源之一。下列表述正确的是
正确答案
解析
略
知识点
用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应A可实现氯的循环利用。反应A: 4HCl+O2==2Cl2+2H2O
(1)已知:
Ⅰ反应A中, 4mol HCl被氧化,放出115.6kJ的热量。
Ⅱ
①H2O的电子式是_______________。
②反应A的热化学方程式是_______________。
③断开1mol H—O键与断开1 mol H—Cl键所需能量相差约为__________KJ,H2O中
H—O键比HCl中H—Cl键(填“强”或“若”)_______________。
(2)对于反应A下图是4种投料比[n(HCl):n(O2)分别为[1:1、2:1、4:1、6:1、]下图为反应温度对HCl平衡转化率影响的曲线。
①曲线b对应的投料比是______________.
②当曲线b、 c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投
料比的关系是_________________.
⑧投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是_______________.
正确答案
(1)①
②4HCl(g)+O2 
③32
(2)①4:1
②投料比越高,对应的反应温度越低。
③30.8%
解析
略
知识点
下列有关物质结构的表述正确的是
正确答案
解析
略
知识点
下列有关化学用语表示正确的是
正确答案
解析
略
知识点
下列有关化学用语表示正确的是
正确答案
解析
有关化学用语常涉及常见物质的组成和结构,尤其是一些常见物质电子式、结构式、结构简式及模型等等,内容比较基础。
知识点
扫码查看完整答案与解析