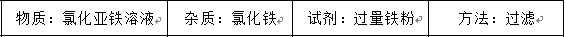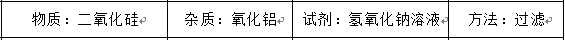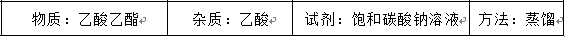- 物质的分离、提纯和检验
- 共229题
工业上从废催化剂(主要成分是钯和活性炭,还含有少量铁、锌)中回收钯,采用如下流程:
已知:钯(Pd)的性质与铂相似。钯与王水在加热条件发生的主要反应是:
3Pd +12HCl + 2HNO3 
请回答下列问题:
(1)酸溶I前先将废催化剂在700℃下进行灼烧,同时不断通入空气的作用是_______________
_________________________。加入盐酸的目的是__________________________________。
(2)酸溶Ⅱ需控制温度不宜过高,除了控制一定反应速率外,其原因是_______________________
__________________。
(3)若用足量的烧碱吸收混有空气的气体Ⅱ,吸收后溶液中含有的溶质的化学式有NaOH、NaNO2、___________。
(4)使用甲醛还原钯的化合物时,溶液须保持碱性,否则会造成甲醛的额外损耗,原因是_______________________________________。
(5)操作I的名称是_______________,溶液I可能含有的有机离子为________________。
(6)催化剂中另一主要成分活性炭可以用浓硝酸除去,写出该反应的化学方程式:
_____________________________________________________。
正确答案
(1)除去废催化剂中的活性炭(2分) 除去铁、锌等杂质 (2分)
(2)防止硝酸分解,防止盐酸、硝酸挥发(2分)
(3)NaNO3(2分)(4)酸性条件下,甲醛会被硝酸氧化(2分)
(5)过滤(2分) HCOO−(2分)
(6)C+4HNO3(浓)
解析
略
知识点
利用酸解法制钛白粉产生的废液[含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4],生产铁红和补血剂乳酸亚铁。其生产步骤如下:
已知:TiOSO4可溶于水,在水中可以电离为TiO2+和SO42—。
请回答:
(1)步骤①中分离硫酸亚铁溶液和滤渣的操作是 。
(2)滤渣的主要成分为TiO2•xH2O,写出TiOSO4水解生成TiO2•xH2O的化学方程式 。
(3)硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为 。
(4)用平衡移动的原理解释步骤⑤中加乳酸能得到乳酸亚铁的原因 。
(5)步骤④的离子方程式是 。
(6)步骤⑥必须控制一定的真空度,原因是有利于蒸发水以及 。
(7)为测定步骤②中所得晶体中FeSO4·7H2O的质量分数,取晶体样品a g,溶于稀硫酸配成100.00 mL溶液,取出20.00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol•L-1 KMnO4溶液20.00 mL,所得晶体中FeSO4·7H2O的质量分数为(用a表示) 。
正确答案
见解析。
解析
(1)过滤
(2)TiOSO4 +(x+1)H2O ==TiO2 • xH2O↓+H2SO4
(3)1: 4
(4)
(5)Fe2++2HCO3—==FeCO3↓+H2O+CO2↑
(6)防止Fe2+被氧化
(7)13.9/a
知识点
提纯下列物质所选试剂及对应分离方法均可行的是
正确答案
解析
略
知识点
29.某学习小组按如下实验流程探究
实验(一) 碘含量的测定
取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)实验(一) 中的仪器名称:仪器A( ), 仪器 B ( ) 。
(2)①根据表中数据绘制滴定曲线:
②该次滴定终点时用去AgNO3溶液的体积为( )mL,计算得海带中碘的百分含量为( )%。
(3)①分液漏斗使用前须检漏,检漏方法为( )。
②步骤X中,萃取后分液漏斗内观察到的现象是( ) 
③下列有关步骤Y的说法,正确的是 ( ) 。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
④实验(二) 中操作Z的名称是( )。
(4)方案甲中采用蒸馏不合理,理由是( ) 。
正确答案
(1)坩埚 500mL容量瓶 ;
(2) ① 
(3)①向分液漏斗中加入少量水,检查旋塞处是否漏水;将漏斗倒转过来,检查玻璃塞是否漏水 ; ②液体分上下两层,下层呈紫红色 ; ③AB ; ④过滤
(4)主要由于碘易升华,会导致碘的损失
解析
解析已在路上飞奔,马上就到!
知识点
除去下列物质中的杂质选用的试剂和方法最合理的是
正确答案
解析
略
知识点
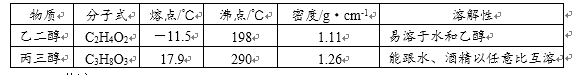
有一瓶乙二醇和丙三醇的混合物,它们的性质如下表。则将乙二醇和丙三醇互相分离的最佳方法是()
正确答案
解析
略
知识点
饱和食盐水在化工生产和中学化学中有广泛应用,下列使用饱和食盐水的叙述错误的是
正确答案
解析
略
知识点
实验室中某些气体的制取、除杂及收集装置如图所示。仅用此装置和表中提供的物质完成相关实验,最合理的是
正确答案
解析
略
知识点
用下图所示实验装置进行相应实验,能达到实验目的的是
正确答案
解析
略
知识点
下列分离与提纯的方法不可行的是
正确答案
解析
略
知识点
扫码查看完整答案与解析