- 化学常用计量
- 共355题
10.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2: 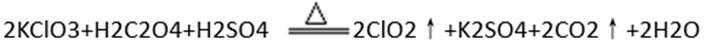
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.实验室常用酸性KMnO4溶液除去CO2中的SO2,发生如下反应(未配平)

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11、LiAlH4
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.用石墨做电极电解200 mL CuSO4溶液,电解过程中电子转移的物质的量n(e-)与产生气体的体积V(标准状况)的关系如图所示。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
(1)软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O.
(2)除去反应混合物中的不溶物
(3)电解混合液MnSO4+ZnSO4+2H2O
下列说法不正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成的镍电池广泛应用于混合动力汽车系统,但电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计如下实验流程:
回答下列问题:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.铜是生物体必需的微最元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)写出铜与稀硝酸反应的化学方程式_________。
(2)为了保护环境和节约资源,通常先用H2O2和稀硫酸的混合溶液溶出废旧印刷电路板中的铜,最终实现铜的回收利用。写出溶出铜的离子方程式_________ 。
(3)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:

(4)铜在潮湿的空气中能发生吸氧腐蚀而生锈,铜锈的主要成分为Cu2(OH)2CO3(碱式碳酸铜)。试写出上述过程中负极的电极反应式 ___________。
(5)研究性学习小组用“间接碘量法”测定某试样CuSO4·5H2O(不含能与I—反应的氧化性杂质)的含量。取ag试样配成l00mL溶液,每次取25.00mL,滴加KI溶液后有白色碘化物沉淀生成。写出该反应的离子方程式____________。继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫代硫酸钠标准溶液滴定,发生反应的化学方程式为:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.Na2FeO4是一种高效多功能水处理剂,既能消毒杀菌,又能除去悬浮物杂质。一种制备Na2FeO4的反应原理为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列有关说法正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3 =bO2↑+cCl2↑+d HClO4 + eH2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的是 ()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.2010年在上海举办的世博会将主打环保牌,20辆氢燃料电池公交车、300辆氢燃料电池出租车将投入运行,它们以氢气为能源,实现了真正的零污染。氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析




