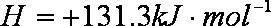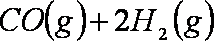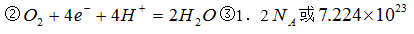- 热化学方程式
- 共127题
氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
① 工业合成氨的热化学方程式是________。
② 若起始时向容器内放入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则
Q(填“>”、“<”或“=”)_______184.4 kJ。
③ 已知:
1 mol N-H键断裂吸收的能量约等于_______kJ。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g) 
①焓变ΔH(填“>”、“<”或“=”)___________ 0
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
③ 上图中的B点处,NH3的平衡转化率为_______。
(3)氮气是制备含氮化合物的一种重要物质,而氮的化合物用途广泛。
下面是利用氮气制备含氮化合物的一种途径:
①过程Ⅱ的化学方程式是___________ 。
②运输时,严禁NH3与卤素(如Cl2)混装运输。若二者接触时剧烈反应产生白烟,并且0.4 mol NH3参加反应时有0.3 mol 电子转移。写出反应的化学方程式___________ 。
③氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。
已知:4NH3(g) + 3O2(g) == 2N2(g) + 6H2O(g) ΔH = ―1316 kJ/mol,则该燃料电池的负极反应式是___________ 。
正确答案
见解析。
解析
(1)① N2(g)+3H2(g) =2NH3(g) ΔH= –92.2 kJ/mol
② <
③391
(2)① <
②nNH3增大,平衡正向移动,则增大CO2的转化率
③32%
(3)① N2 + 3H2
② 8NH3 + 3Cl2 == 6NH4Cl + N2
③ 2NH3―6e- + 6OH- == N2↑+ 6H2O
知识点
27.科学家开发出一种“洁净煤技术”,通过向地下煤层“气化炉”中交替鼓入空气和水蒸气的方法,连续产出高热值的煤炭气,其主要成分是CO和


(1)“气化炉”中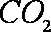
(2)用煤炭气合成甲醇的反应为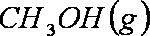
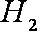
①生成甲醇的反应为__________反应(填“放热”或“吸热”)。
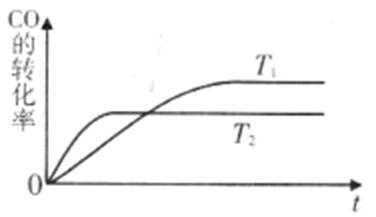
②若该反应在绝热、恒容的密闭体系中进行,下面3个图中,既正确又能说明反应在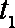
③在不改变原料用量的前提下,为提高CO的转化率,可以采取的措施是__________ (答一种措施即可)。
(3)近年来,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆,甲醇燃料电池的工作原理如下图所示。
①该电池工作时,b口通入的物质为__________,c口通入的物质为__________。
②该电池正极的电极反应式为__________。
③工作一段时间后,当6.4g甲醇完全反应生成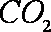
正确答案
(1)
(2)①放热 ; ②c; ③降低温度(或增大压强、分离出甲醇等)
(3)
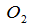
解析
解析已在路上飞奔,马上就到!
知识点
28.甲醇又称“木精”,是重要的溶剂和基本有机原料。工业上常以CO和H2为原料合成甲醇。
(1)已知每1g液态甲醇不完全燃烧生成一氧化碳和液态水时放出13.8kJ热量,写出甲醇不完全燃烧的热化学方程式:__________________。
(2)工业上常利用反应:




A.1~1.5 B.2.5~3 C.3.5~4.5
(3)制甲醇所需要的氢气,可用下列反应制取:
150℃时,在容积为2L的恒温恒容密闭容器中充入1 mol CO和2 mol H2O(g),反应达到平衡后测得H2的体积分数为25%。
① 平衡时CO的转化率为_________。
②150℃下,若起始时充入

(4)某研究小组设计了如图所示的原电池装置,向导管中通入物质的量之比为1:1的CO和

① 电池工作一段时间后,电解质溶液的pH_________(填“增大”、“减小”或“不变”)。
②电池工作一段时间后,测得电解质溶液增重6.2g(不考虑未反应气体的溶解),则负极参加反应的气体质量为_________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
(1)上述流程中碳酸钾溶液所起的作用
(2)分解池中反应的化学方程式为( );
(3)在合成塔中,若有4.4k
(4)从平衡移动原理分析,低温有利于原料气的转化,实际生产
(5)图13是甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:
正确答案
(1)富集空气中的

(2)
(3)
(4)保证有较快的反应速率,提高生产率(能答出与速率相关的答案即可)
(5)甲醇;正;
解析
解析已在路上飞奔,马上就到!
知识点
23.(1)M由两种短周期元素组成,每个M分子含有18个电子,其分子球棍模型如右图所示。测得M的摩尔质量为32g/mol。画出编号为2的原子结构示意图:( )。
(2)已知1.0mol·L—1NaHSO3溶液的pH为3.5,加入氯水,振荡后溶液pH迅速降低。溶液pH降低的原因是 ( ) (用离子方程式表示)。
(3)在常温常压和光照条件下,N2在催化剂(TiO2)表面与H2O反应,生成1molNH3和O2时的能量变化值为382.5kJ,达到平衡后此反应NH3生成量与温度的实验数据如下表。则该反应的热化学方程式为 ( ) 。
(4)在溶液中,一定浓度的NH4+能溶解部分Mg(OH)2固体,反应如下:
2NH4+(aq) + Mg(OH)2(s) Mg2+(aq)+2NH3·H2O(aq) 写出上述反应的平衡常数表达式( );某研究性学习小组为探究Mg2+与NH3·H2O反应形成沉淀的情况,设计如下两组实验
请分析实验①、②产生不同现象的原因:( )。
(5) 在室温下,化学反应I–(aq)+ ClO–(aq) = IO–(aq) + Cl–(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
已知表中初始反应速率与有关离子浓度关系可以表示为v= k [I–]1 [ClO–]b [OH–]c(温度一定时,k为常数)。
①设计实验2和实验4的目的是( ) ;
②若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH = 13,反应的初始速率v= ( ) 。
23.

(2)已知1.0mol·L—1NaHSO3溶液的pH为3.5,加入氯水,振荡后溶液pH迅速降低。溶液pH降低的原因是 (用离子方程式表示)。
(3)在常温常压和光照条件下,N2在催化剂(TiO2)表面与H2O反应,生成1molNH3和O2时的能量变化值为382.5kJ,达到平衡后此反应NH3生成量与温度的实验数据如下表。则该反应的热化学方程式为 。
(4)在溶液中,一定浓度的NH4+能溶解部分Mg(OH)2固体,反应如下:
2NH4+(aq) + Mg(OH)2(s) 
写出上述反应的平衡常数表达式
某研究性学习小组为探究Mg2+与NH3·H2O反应形成沉淀的情况,设计如下两组实验
请分析实验①、②产生不同现象的原因:
。
(5) 在室温下,化学反应I–(aq)+ ClO–(aq) = IO–(aq) + Cl–(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
已知表中初始反应速率与有关离子浓度关系可以表示为v= k [I–]1 [ClO–]b [OH–]c(温度一定时,k为常数)。
①设计实验2和实验4的目的是 ;
②若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH = 13,反应的初始速率v= 。
正确答案
扫码查看完整答案与解析