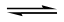
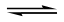
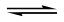
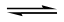
- 离子方程式的书写
- 共269题
下列离子方程式的书写与结论均合理的是( )。
正确答案
解析
略
知识点
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,舍少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
(1)加入H2O2氧化时,发生反应的化学方程式为_______________ 。
(2)滤渣2的成分是__________(填化学式)。
煅烧过程存在以下反应:
2MgSO4+C

MgSO4+3C
利用下图装置对煅烧产生的气体进行分步吸收或收集。
(3)D中收集的气体是__________(填化学式)。
(4)B中盛放的溶液是 (填序号)。
a.NaOH溶液 b.Na2CO3溶液 c.稀硝酸 d..KMnO4溶液
(5)A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: ______________________ 。
正确答案
(1)2FeSO4+H2O2+H2SO4→Fe2 (SO4)3+2 H2O
(2)Fe(OH)3
(3) CO
(4)d
(5)3S+6OH-
解析
略
知识点
在0.1 mol/L的NaHSO3溶液中有如下关系:c(Na+)>c(HSO3-) >c(SO32-) >c(H2SO3),向NaHSO3溶液中慢慢地加入少量的NaOH溶液,发生的主要反应的离子方程式为()
正确答案
解析
略
知识点
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:
(1)MgCO3与稀硫酸反应的离子方程式为___________ 。
(2)加氨水调节溶液的PH范围为___________。
(3)滤渣2 的成分是___________(填化学式)。
(4)煅烧过程存在以下反应:
利用上图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体是___________(填化学式)。
②B中盛放的溶液是___________ (填字母)。
a.NaOH 溶液
b.Na2CO3 溶液
c.稀硫酸
d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:___________ 。
正确答案
见解析。
解析
(1)MgCO3+2H+===Mg2++CO2↑+H2O
(2)2.8<PH<9.4
(3)Fe(OH)3
(4)①CO
② d
③3S+6OH-
知识点
将氯化铵固体溶解在D2O(重水)中,反应的离子方程式正确的是()
正确答案
解析
略
知识点
化学是以实验为基础的一门科学,化学实验在化学学习中具有重要的作用。
(1)下列与实验有关的叙述正确的是________(填序号)。
①新制的氯水、氨水、硝酸银溶液都必须存放在配有磨口塞的棕色玻璃瓶中
②容量瓶 、分液漏斗、酸(碱)式滴定管使用前都必须检验是否漏水
③用稀盐酸即可鉴别Na2SiO3、NaHCO3、Na[Al(OH)4]、Na2CO3四种溶液
④实验时,酸液溅到眼中,应用大量水冲洗,边洗边眨眼睛
⑤制备乙酸乙酯时,把乙醇和乙酸混合后加入到浓硫酸中
⑥用托盘天平准确称取29.25gNaCl固体,用于配制500mL0.5mol·L-1NaCl溶液
(2)某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中通入足量的CO2气体,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥。
①步骤2中发生反应的离子方程式是________。
②步骤2中通入足量的CO2气体后,检验沉淀是否完全的方法是________。
正确答案
(1) ②③⑤
(2)①[Al(OH)4]-+CO2=Al(OH)3↓+HCO;②取上层清液,逐滴加入稀硫酸,若变浑浊则说明沉淀不完全,若不变浑浊则说明沉淀完全
解析
略。
知识点
在含有n mol FeI2的溶液中通入Cl2,有x mol Cl2发生反应。下列说法正确的是()
正确答案
解析
略
知识点
9.A、B、C、D、E为五种元素的单质,其余为化合物。其中只有E为金属元素,五种元素的原子序数按B、D、C、A、E顺序依次增大,D、C元素在周期表中位置相邻,在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙化合物,C和D化合可得丁。已知乙、丙每个分子中均含有10个电子,下阁为相互转 化关系:
谘回答下列问题:
(1)下面是周期表的一部分,请将A、C、E用元素符号填在相应的位置上。
(2)写出工业上制取A反应的离子方程式_______________
(3)戊的分子式为_______.B与D形成的原子个数比为2:1的化合物中,D原子最外层为8电子结构,请写出该化合物的电子式______
(4)A与丙常温下发生反应生成甲与单质D,该反应的化学方程式_________
(5)8gE在A中燃烧放山热摄QkJ,写出该反应热化学方程式________(热量是常温下测定的)。
(6)实验室配制庚溶液的实验方法是________。
正确答案
(1)
(2)MnO2 + 4H+ + 2Cl― △ Mn2+ + Cl2↑ + 2H2O
(3)HClO
(4)
(5)2Fe(s) + 3Cl2(g) 点燃 FeCl3(s),△H = -14 Q kJ·mol-1
(6)向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉。
解析
略
知识点
下列离子方程式正确的是( )。
正确答案
解析
略
知识点

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析