- 离子方程式的书写
- 共269题
24.海洋中有丰富的食品、矿产、能源、药物和水产资源等,海洋经济越来越受到人们的重视。请填写下列空白。
(1)从海水提取食盐,工业上可以制氯气、氢气。写出该反应的离子方程式( ) 。
(2)资料查明:海水中Mg2+浓度约为Mg 1.29 g /kg,海水的平均密度:1.024g/cm3,Ksp[Mg(OH)2] = 1.1×10-11 。要富集海水中的镁离子,加入生石灰,要使溶液氢氧根离子浓度的至少达到( ) 。(请保留3位有效数字)
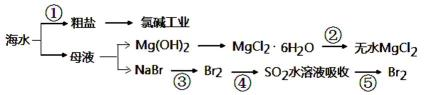
(3)利用海水得到粗盐、无水氯化镁和溴等的生产流程示意图:
i. 过程②中结晶出的MgCl2·6H2O要制得无水MgCl2需在HCl氛围中加热脱水的原因_____
_____________________________________________________________________________。
ii. 从循环经济等综合考虑,在过程③的离子方程式为_______________________________。
从反应后的溶液中分离出溴单质的操作是:向溶液中加入CCl4、 、分离出溴单质。
iii. ④和⑤反应的意义是____________________________________________________。
iv. 除去粗盐中的SO42-、Ca2+、Mg2+等杂质,需要用到的试剂为________(填序号)。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13、25℃时,有下列四种溶液:①0.1mol/L 的CH3COOH溶液 ②pH=13的NaOH溶液
③ 0.05mol/L的 H2SO4 ④0.1mol/L 的Na2CO3溶液 则下列有关说法中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.绿色、低碳、环保新能源是当今经济社会关注的热点。
I.(2分)右图是太阳光伏电池光电转换系统示意图,
由图判断:
N型半导体是电池的( )极;
电流由( ) 极流向 ( )极(填X、Y)
II.(2分)下列观点符合科学道理的有:( ) ;
A.核电站能把化学能转化为电能,应大力发展核能;
B.太阳光伏电池是把光能转换成电能的装置,其工作
原理与原电池工作原理相同;
C.大量使用锂电池是开发环保新能源的举措;
D.氢氧燃料电池是一种绿色、环保、低碳的新能源;
III.(12分)2010年全球锂离子电池总产量超过38亿只,回收废旧锂离子电池意义重大,其中需要重点回收利用的是正极材料,其主要成份有LiCoO2(钴酸锂),炭黑,铝箔等,某种回收流程如下:
(1)(3分)碱浸时,正极材料中 ( ) 溶解(填名称)发生反应的化学方程式: ( ) ;
(2)(5分)写出滤液A中通入过量CO2的离子方程式: ( ) ;D溶液呈 ( )(填“酸性”、“碱性”或“中性”),原因是(用离子方程式表示): ( ) 。
(3)(4分)酸浸发生反应的化学方程式是: ( ) ;该反应若转移0.5mole-,则在标准状况下产生O2体积为 ( ) L。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.碱式碳酸铜是一种用途广泛的化工原料。工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如下:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.下列离子方程式正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.铜是与人类关系非常密切的有色金属,已知常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生;
(1)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:
(2)在CuCl2溶液中逐滴加入过量KI溶液可能发生:


①若a反应是主要的,需要查询的数据是( ) 。
②为顺利观察到白色沉淀可以加入的最佳试剂 ( ) 。
A.SO2 B.四氯化碳 C.NaOH D.乙醇
(3)一定条件下,在CuSO4中加入NH5反应生成氢化亚铜(CuH)。
①已知NH5的所有原子都达到稀有气体的稳定结构,请写NH5电子式:( ) 。
②写出CuH在过量稀盐酸中有气体生成的离子方程式 ( )。
③将CuH溶解在适量的稀硝酸中, 完成下列化学方程式
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.能正确解释下列反应原理的离子方程式是:()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
24.硫酸铁铵 [a(NH4)2SO4·bFe2(SO4)3·cH2O] 常作为高铁的标准,可用于测定卤素的指示剂。某工厂实验室用一种硫酸亚铁样品(含少量硝酸钙)和硫酸铵为原料,设计如下工艺过程,制取硫酸铁铵:
(已知:NaClO、H2O2、KMnO4、K2Cr2O7均具有强氧化性,能氧化Fe2+。)
请完成下列填空:
(1)写出A、B适宜的化学式:A ( ) 、B ( ) 。
(2)减压过滤得到的滤渣C,其主要成分是 ( )(填化学式)。
操作甲的目的是:( ) 。
(3)操作乙、丙的名称分别是:乙( ),丙 ( ) 。
(4)检验产品硫酸铁铵中的阳离子,相关的离子方程式有( )。
(5)为了用重量法确定产品硫酸铁铵[a(NH4)2SO4·bFe2(SO4)3·cH2O]中a、b、c的值(供选用的试剂:浓硫酸、碱石灰、氢氧化钠、氯化钡),除了测得取用样品的质量外,至少还需要测定 种物质的质量。灼烧固体所需要的仪器是( )(选出合适的选项)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26. 铜是生物体必需的微量元素,也是人类最早使用的金属之一。铜的生产和使用对国计民生各个方面都产生了深远的影响。
(1)写出铜与稀硝酸反应的化学方程式___________________
(2) 为了保护环境和节约资源,通常先用H2O2和稀硫酸的混合溶液溶出废旧印刷电路 板中的铜,最终实现铜的回收利用。写出溶出铜的离子方程式____________。
(3)工业上以黄铜矿为原料,采用火法溶炼工艺生产铜。该工艺的中间过程会发生反应:

(4)铜在潮湿的空气中能发生吸氧腐蚀而生锈,铜诱的主要成分为Cu2(OH)2CO3(碱式碳酸铜)。试写出上述过程中负极的电极反应式____________。
(5)研究性学习小组用“间接碘量法”测定某试样中CuSO4.5H20(不含能与I-反应的氧化性杂质)的含量。取ag试样配成1OOmL溶液,每次取25.00mL,滴加KI溶液后有白色碘化物沉淀生成。写出该反应的离子方程式____________。
继续滴加KI溶液至沉淀不再产生,溶液中的I2用硫代硫酸钠标准溶液滴定,发生 反应的化学方程式为:I2+2Na2S203=2NaI+Na2S4O6,平均消耗cmol/L的Na2S2O3 溶液VmL。则试样中CuSO4.5H20的质量分数为____________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.下列反应的离子方程式书写正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析