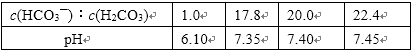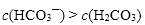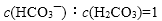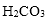- 化学反应原理
- 共2396题
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:下列判断不正确的是( )
正确答案
解析
略
知识点
人体血液中存在平衡:CO2 + H2O 

正确答案
解析
略
知识点
25oC时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是
正确答案
解析
略。
知识点
有25℃时0.1 mol/L的①氯化铵、②氯化钠、③醋酸钠三种溶液。下列有关判断不正确的是
正确答案
解析
略
知识点
某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是
正确答案
解析
略
知识点
下列溶液中有关物质的浓度关系正确的是
正确答案
解析
略。
知识点
室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是
正确答案
解析
略
知识点
常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液,有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)。
根据图示判断,下列说法正确的是
正确答案
解析
略
知识点
室温下,用0.100 mol/L NaOH 溶液分别滴定20.00 mL 0.100 mol/L的盐酸和醋酸,下列说法正确的是
正确答案
解析
略。
知识点
下列反应的离子方程式书写正确的是
正确答案
解析
略
知识点
15. 25℃时,有c(CH3COOH)+c(CH3COO-)= 0.1mol/L的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述不正确的是( )
正确答案
解析
略
知识点
含氮废水中的NH4+在一定条件下可与O2发生以下反应:
① NH4+(aq) + 3/2O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ;ΔH = -273kL/mol
② NO2-(aq) + 1/2O2(g) = NO3-(aq) ; ΔH = -73kL/mol
下列叙述不正确的是( )。
正确答案
解析
略
知识点
6.下列说法正确的是()
正确答案
解析
略
知识点
氮是地球上含量丰富的一种元素,氯及其化合物在工农业生产,生活中有着重要作用。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图:
请写出NO2和CO反应的热化学方程式______________________________________。
(2)在一定体积的密闭容器中,进行如下反应:N2(g)+3H2(g)→2NH3(g)+Q(Q>0),
其化学平衡常数K与温度T的关系如下表:
比较K1、K2的大小:K1_______K2(填“>”、“=”或“<”);
判断该反应达到化学平衡状态的依据是____(选填序号)。
a.2v(H2)正=3v(NH3)逆 b.2v(N2)正=v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)盐酸肼( N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。盐酸肼第1步水解反应的离子方程式为__________________________;盐酸肼水溶液中各离子浓度的关系正确的是____(填序号)。
a.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
b.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
c.2 C(N2H62+)+ c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
d.2 c(N2H62+) +2 c([N2H5•H2O]+)+2c([N2H4•2H2O)= c(Cl-)
正确答案
(1)NO2 (g)+CO( g) →CO2 (g)+NO(g) +234 kJ
(2)> ;a、c
(3) N2H62++ H2O→[N2H5•H2O]++ H+
a、c、d
解析
略
知识点
常温下,0.1 mol/L氨水溶液中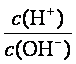
正确答案
解析
略
知识点
扫码查看完整答案与解析