- 化学反应与能量
- 共1152题
25.下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
20. 部分弱酸的电离平衡常数如下表:
下列选项正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
甲同学进行Fe2+还原性的实验,针对异常现象进行探究。
步骤一:制取FeCl2溶液。向0.1 mol•L-1 FeCl3溶液中加足量铁粉振荡,静置后取上层清液,测得pH<1。
实验二:向2 mL FeCl2溶液中滴加2滴0.1 mol•L-1 KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5 mol•L-1、pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。
(1)用离子方程式表示步骤二中溶液变红的原因: 、 。
(2)甲探究步骤二中溶液褪色的原因:
I. 取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。
III. 向2 mL 0.1 mol•L-1 FeCl3溶液中滴加2滴0.1 mol•L-1 KSCN溶液,变红,通入O2,无明显变化。
① 实验I的说明 ;②实验III的目的是 。
得出结论:溶液退色的原因是酸性条件下H2O2将SCN-氧化成SO42-。
(3)甲直接用FeCl2·4H2O配制 ① mol•L-1 的FeCl2溶液,重复步骤二中的操作,发现液体红色并未褪去。进一步探究其原因:
I.用激光笔分别照射红色液体和滴加了KSCN溶液的FeCl3溶液,前者有丁达尔效应,后者无。测所配FeCl2溶液的pH,约为3。由此,乙认为红色不褪去的可能原因是 ② 。
II.查阅资料后推测,红色不褪去的原因还可能是pH较大时H2O2不能氧化SCN-。乙利用上述部分试剂,通过实验排除了这一可能。乙的实验操作及现象是:
正确答案
见解析。
解析
(1)2Fe2++ H2O2 + 2H+ === 2Fe3++ 2H2O Fe3++3SCN-
(2)①溶液红色褪去是因为SCN-发生了反应而不是Fe3+发生反应
②排除H2O2分解产生的O2氧化SCN-的可能
(3)
①0.15
②H2O2将Fe2+氧化为Fe3+,pH增大促进Fe3+水解形成红色Fe(OH)3胶体
③取2 mL BaCl2溶液,滴加2滴0.1 mol·L-1KSCN溶液和5滴5% H2O2溶液(多答盐酸或答酸化BaCl2溶液为0分,答错一种试剂即为0分)
④无明显现象
知识点
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
①实验I的现象为 。
②FeCl2溶液与新制氯水反应的离子方程式为 。
(2)该同学分析了导致实验II现象的可能原因,并对实验方案进行了改进。改进后的
实验操作和现象如下:
根据实验III,甲同学认为Fe3+有可能与I-发
明的文字说明他得出上述结论的理由 。
(3)该同学认为需要进一步设计实验证明根据实验III中现象得出的结论。请补全下表中
的实验方案。
(4)上述实验结果表明,Fe3+有可能与I-发生氧化还原反应。进一步查阅资料知,参加反
应的Fe3+与I-的物质的量相同。该同学结合上述实验结论,分析了实验III中加入
KSCN后溶液变红的原因,认为Fe3+与I-反应的离子方程式应写为

正确答案
见解析。
解析
(1)① 滴加KSCN后溶液无明显变化,加入氯水后溶液变成红色
② 2Fe2+ + Cl2 === 2Fe3+ 
(2)溶液变成黄色,推测生成了I2
(3)
(4)2Fe3+ + 2I- 
知识点
粗制的CuSO4·5H2O晶体中含有Fe2+。提纯时,为了除去Fe2+,常加入少量H2O2,
然后再加入少量碱至溶液pH=4,可以达到除去铁离子而不损失硫酸铜的目的。下列说法
不正确的是
正确答案
解析
略
知识点
吸进人体内的氧有2%转化为加速人体衰老的氧化性极强的活性氧,若Na2SeO3能清除人体内活性氧,则Na2SeO3的作用是()
正确答案
解析
略
知识点
9.下列各组物质间反应,其中水既不作氧化剂又不作还原剂的氧化还原反应是 ( )
①F2和H2O ②Na和H2O ③Na2O2和H2O
④NO2和H2O ⑤Na2O和H2O ⑥Cl2和H2O
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
25.纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备是:
i.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4。
ii.将SiCl4分离,得到纯净的TiCl4。
iii.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
iiii.TiO2·xH2O高温分解得到TiO2。
①分离TiCl4与SiCl4所采取的操作名称是( )。
② Ⅲ中反应的化学方程式是( )。
③ 如Ⅳ在实验室完成,应将TiO2·xH2O放在( )(填仪器编号)中加热。
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a.O2


① b反应过程破坏的化学键是( ) 。
② H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的( )
(填“氧化性”或“还原性”)。
(3)某研究小组用下列装置模拟“生态马路”部分原理。(夹持装置已略去)
① 如缓慢通入22.4 L(已折算成标准状况)CO气体,结果NaOH溶液增重11 g,则CO的转化率为( )。
② 当CO气体全部通入后,还要再通一会儿空气,其目的是( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
24.以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
回答下列问题:
(1)将煅烧黄铁矿的化学方程式补充完整: FeS2+ O2 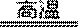
该反应中,FeS2为( )剂;SO2为( ),其常用于制备硫酸,反应过程中的化学反应方程式为( )、 SO3+H2O=H2SO4
(2)酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率和 ( );
(3)通氯气氧化时,发生的主要反应的离子方程式为( );
(4)该过程产生的污染空气的气体有三种,尾气均可用强碱溶液吸收,其中氯气被吸收的离子方程式为( )。
(5)从FeCl3溶液中得到FeCl3.6H2O晶体的操作为 ( ) 。
正确答案
答案已在路上飞奔,马上就到!
解析
解析已在路上飞奔,马上就到!
知识点
33.Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为 ( );向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式:( )。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:取少量样品溶于水,( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析