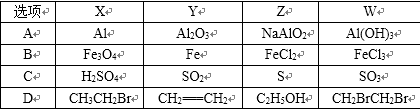
- 化学反应与能量
- 共1152题
11.不同的金属在冶炼方法上也有所不同,下列说法正确的是
正确答案
解析
A.钒、铬、锰可用铝热反应制取,铁用热还原法炼制,故A错误;
B.炼铁和炼钢都是利用氧化还原反应的原理,不同点是前者使用还原剂,后者使用氧化剂,故B错误;
C.氯化铝是共价化合物,所以熔融时,它是不导电的,工业上用电解氧化铝方法制取铝,故C错误;
D.高炉炼铁中焦炭的作用为与氧气反应产生热量和制造还原剂一氧化碳,故D正确
考查方向
金属冶炼
解题思路
A.铁通常用热还原发制取;
B.依据炼铁和炼钢原理解答;
C.工业上采用电解熔融氯化物的方式制取钠、镁,用电解氧化铝来制取铝;
D.依据炼铁原理解答
易错点
炼钢和炼铁的原理区别
教师点评
本题考查了金属的冶炼方法选择,明确金属活泼性是解题关键,注意氯化铝为共价化合物,不导电,冶炼金属铝通常用电解熔融氧化铝方法,题目难度中等
知识点
关于大宗和关键原材料的供应,应调查主要供应企业的生产经营情况,并在( )阶段签订供货意向书。
A.初步可行性研究
B.可行性研究
C.项目评估
D.项目决策审批
正确答案
B
解析
大宗和关键原材料的供应,应调查主要供应企业的生产经营情况,并在可行性研究阶段签订供货意向书。
证券价格仅反映了历史价格信息的是( )。
A.强型有效市场
B.半强型有效市场
C.弱型有效市场
D.半弱型有效市场
正确答案
C
解析
[解析] A项强型有效市场,反映了所有的信息,包括公开的和内幕的信息;B项半强型有效市场,反映了所有公开的信息,包括公司公布的财务报表和历史上的价格信息;C项弱型有效市场,仅反映了历史价格信息。D项不属于有效市场分类的类型。
人工光合作用能够借助太阳能,用CO2和H2O备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是( )
正确答案
解析
依题意,二氧化碳和水太阳能作用下生成HCOOH,化学方程式为CO2+H2
为CO2+2e-+2H+=HCOOH
故D正确;
知识点
下列市场中,证券价格反映了所有公开的和内幕的信息的是( )。
A.强型有效市场
B.半强型有效市场
C.弱型有效市场
D.半弱型有效市场
正确答案
A
解析
暂无解析
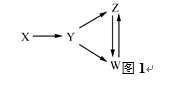
8. 一定条件下,下列各组物质能一步实现图1所示转化关系的是( )
正确答案
解析
A、Y(氧化铝)不能一步转化为W(氢氧化铝),不符合条件,故A错误;
B、四氧化三铁通过铝热反应生成单质铁,铁与弱氧化剂盐酸反应生成氯化亚铁,铁与氯气生成氯化铁;FeCl2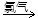
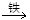
C、Z(硫)不能一步转化为W(三氧化硫),不符合条件,故C错误;
D、Z(C2H5OH)不能一步转化为W(CH2BrCH2Br),要先消去,再加成,故D错误
考查方向
本题考查常见物质的性质及其转化关系
解题思路
A、Y(氧化铝)不能一步转化为W(氢氧化铝);
B、四氧化三铁通过铝热反应生成单质铁,铁与弱氧化剂盐酸反应生成氯化亚铁,铁与氯气生成氯化铁;FeCl2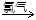
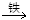
C、Z(硫)不能一步转化为W(三氧化硫);
D、Z(C2H5OH)不能一步转化为W(CH2BrCH2Br)
易错点
C项:硫不能直接生成三氧化硫
教师点评
本题考查常见物质的性质及其转化关系,在近几年的各省高考题中出现的频率较高,题目难度不大
知识点
7.下列叙述正确的是
正确答案
解析
A乙醛和甲酸两者都能发生银镜反应但它们不是同一类物质不互为同系物。B营养物质中的多糖、油脂、蛋白质在一定条件下都可以发生水解分别生成单糖、高级脂肪酸和甘油、氨基酸。C氨基酸是通过缩聚反应生成高分子化合物和氯乙烯是通过加聚反应生成高分子化合物。D通过对煤的干馏,可以提高煤的利用率
考查方向
有机物的结构与性质
解题思路
根据有机物的结构决定性质的规律分析解题,但要注意物质分类的规律
易错点
有醛的性质不一定是醛,以及同系物的判断
教师点评
本题考查有机物的性质与应用属于基础题
知识点
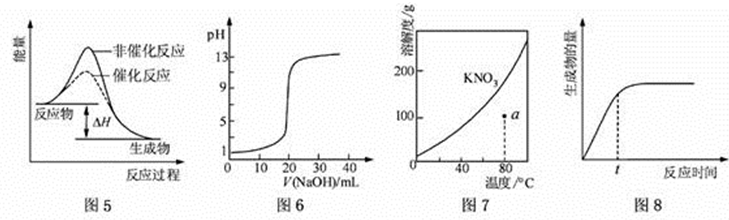
下列图示与对应的叙述相符的是
正确答案
解析
本题考查学生对化学反应热效应、酸碱中和滴定、溶解度曲线、平衡转化率等角度的理解能力。是基本理论内容的综合。高三复习要多注重这一方面的能力训练。
A.图5表示反应物总能量大于生成物总能量,是放热反应。
B.图6中当NaOH与CH3COOH等物质的反应时,溶液因盐类水解而呈碱性,突跃该曲线前。
C.图7通过a作一条辅助线,与KNO3的溶解度曲线有一交点在a点之上,说明a点溶液是不饱和溶液。
D.图8 表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时曲线并没有达到平衡,所以反应物的转化率并不是最大。
知识点
下列有关说法正确的是
正确答案
解析
本题是化学反应与热效应、电化学等的简单综合题,着力考查学生对熵变、焓变,水解反应、原电池电解池、化学反应速率的影响因素等方面的能力。
A分解反应一般是常识吸热反应,熵变、焓变都大于零,仅在高温下自发。内容来源于《选修四》P34-P36中化学方向的判断。
B铁比铜活泼,组成的原电池中铁为负极,更易被氧化。
C据平衡移动原理,升高温度平衡向逆反应方向移动,平衡转化率减小。
D水的离子积常数Kw随着温度的升高而增大,说明水的电离是吸热反应,越热越电离,水的离子积常数Kw随着温度的升高而增大。
知识点
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见
正确答案
解析
略
知识点
扫码查看完整答案与解析