- 元素周期律
- 共415题
11.已知33As、35Br位于同一周期,下列关系正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.现有X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
(1)W位于周期表第四周期第________ 族,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为________ 。
(2)Z最简单的氧化物分子是_________分了(填“极性”或“非极性”):工业上用Z的氧化物制备其单质的化学反应方程式为_________ 。锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它最常用来制造晶体篱,最新研究表明:有机锗具有明显的抗肿瘤活性,锗元素的最高价氧化物的化学式为_________ 。
(3)实验室制取X单质的离子方程式为__________;X的气态氧化物的水溶液与Y的氧化物反应的离子方程式为 ______________。
(4)在50mL lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能为 ___________mL或__________mL。
正确答案
(1)VIII 4Fe(OH)2+O2+2H2O==4Fe(OH)3
(2)非极性 SiO2+2C
(3)4H++2Cl-+MnO2
解析
解析已在路上飞奔,马上就到!
知识点
26.A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次 增大,其中B与C为同一周期,D与F为同一周期,A与D、C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,另外三种是固体。
请回答下列问题:
(1)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为 ______,其分子属于________(选填“极性”或“非极性”)分子。
D与C形成的化合物D2C2可与Y反应生成单质C,写出该反应的化学方程式并标明电子转移的方向和数目:_______________ 。
(2)E是非金属元素,其单质在电子工业中有重要应用,请写出工业生产单质E的化 学反应方程式: ___________________ 。
(3)一定条件下,A的单质气体与B的单质气体充分反应生成6.8 g W气体(已知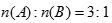
(4)A的单质与C的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通人A的单质气体,N极通入C的单质气体,则M极的电极反应式为 __________ 。
(5)在10 L的密闭容器中,通入2 mol的FC2气体和3 mol的C气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21 mol/L,则平衡时FC2的转化率为______________________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26. A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。A元素的一种核素质子数与质量数在数值上相等;B、E同主族,且核电荷数之比为1︰2;C的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子;D的最外层电子数是内层电子总数的一半。试回答下列问题:
(1)F位于周期表中第________周期________族。
(2)常温时,39 g B、C按原子个数比1︰l形成的化合物X与足量CO2反应放出Q kJ的热量,写出该反应的热化学方程式 ;
写出少量X与FeCl2溶液反应的离子方程式_______________________________________。
(3)B、C、F组成的化合物Y是家用消毒剂的主要成分,Y的溶液呈碱性,用离子方程式解释其原因______________________________;起消毒作用的微粒电子式为_________。
(4)四原子分子Z与C的单质和水反应所得的阴离子电子数相等,Z的分子空间构型为___________型,它属于_________分子(填“极性”或“非极性”);请比较Z与DA3的沸点高低并加以解释_____________________________________________________。
(5)目前人们正在研究开发一种高能电池,它是以熔融的C、E单质为两极,以C离子导电的β-Al2O3陶瓷作固体电解质,反应式为:2C+xE C2Ex 。请写出电池放电时正负极的电极反应式,正极反应式:_______________________。用该电池作电源进行电解含有0.2 mol CuSO4和0.2 mol NaCl的混合溶液500 mL时:若此电池工作一段时间后消耗23 g C单质 。则阳极产生气体体积为:________L(标准状况下);电解后溶液加水稀释至2 L ,溶液的pH为:________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.已知1~18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同电子层结构,下列关系正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.X、Y为短周期元素,X原子各电子层的电子数之比为1:4:1,它比Y原子多3个电子。下列叙述不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族, Z、R 、W同周期。下列说法错误的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.几种短周期元素的原子半径及主要化合价见下表,下列叙述错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析






