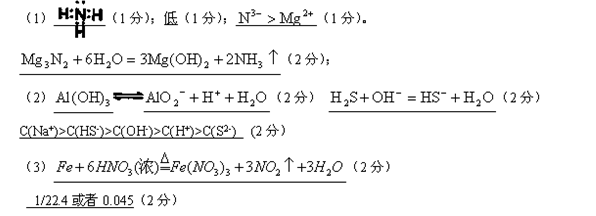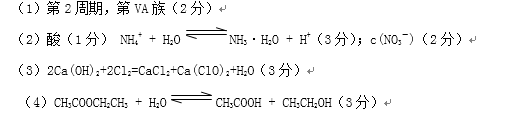- 元素周期律
- 共415题
11.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,A、C同主族,元素B的原子最外层电子数是其电子层数的2倍,D是地壳中含量最高的金属元素。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.A、B、C、D、E、F为原子序数递增的六种短周期元素;已知:A、B、C、D是组成蛋白质的基本元素;E和D可形成离子个数比均为2:l的两种化合物,F是地壳中含量最多的金属元素。
(1)写出B在周期表位置:( );D与E形成原子个数为1:1的化合物电子式: ( ) ;
(2)A与C能形成原子个数比为4:2的分子,写出该分子的结构式:( );
(3)Se是人体必需的微量元素,与D同一主族,且比.D多2个电子层,则Se的原子序数为 ( );它与同族第三周期元素的最高价氧化物对应水化物的酸性强弱比较(用化学式表示): ( ) ;
(4)用F单质作阳极,石墨作阴极,NaHCO3溶液作电解液,进行电解,阳极观察到现象有: ( ) ,用电极反应方程式解释其原因:( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个,Z单质可制成半导体材料,W与X属于同一主族。下列叙述错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.甲、乙、丙、丁四种短周期主族元素,它们的价电子数依次增大,乙形成的化合物种类最多,甲与乙的原子序数之和等于丁的原子序数,丙和乙位于同一周期,丁和乙位于不同周期。则下列说法中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.有A、B、C、D四种短周期元素, A元素属第二周期元素,最高化合价与最低化合价绝对值之差为2,B原子的最外层与次外层电子数之和为 8, C和D两原子的最外层电子数是内层电子数的一半, C元素是植物生长的营养元素之一, 试回答下列问题:
(1)A和B元素形成的酸酐的化学式为 ____________ .
(2)D元素的单质与水反应的化学方程式为 ______________________________.
(3)A和C元素气态氢化物的稳定性: ________ < ________(用分子式表示)
正确答案
(1)N2O3 N2O5 (2) 2Li+2H2O==2LiOH+H2↑ (3)PH3 NH3
解析
解析已在路上飞奔,马上就到!
知识点
27.A、B、C、D、E、F为六种短周期元素。 A、B主族序数之和等于F最高正化合价数;
F原子的最外层电子数等于其周期序数,B原子核内质子数是D原子序数的两倍,且B单质能在
D的某种化合物中燃烧生成黑色和白色两种固体。C的简单阳离子半径大于B的简单阳离子,E
是地壳中含量最丰富的元素。请用化学用语回答下列问题。
(1)B在周期表中的位置为__________________。
(2)DE2的电子式为________________,其形成的晶体类型为________。
(3)工业上冶炼F单质的方法为___________________________________________。
(4)C2E2与DE2反应的化学方程式是______________________________________。
(5)CA与A2E反应后溶液呈碱性且生成A的单质,化学方程式为__________________________。
(6)由B、F的单质作电极与C的最高价氧化物对应水化物的溶液构成原电池,负极电极反应式为________________________________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
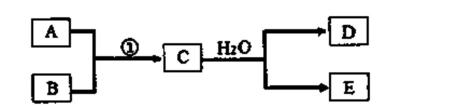
26. 已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:
(1)若条件①为点燃,目前60%的金属单质B都是从海水中提取的,气体D可以使湿润的红色石蕊试纸变蓝,气体D的电子式为:_______;常压下,其沸点比H2O_______(填“高”或“低”);物
(2)若条件①为加热,E是一种两性氢氧化物,请写出该物质的酸式电离方程式:
_______________:气体D是一
(3)若条件①为常温,B和D为同一种无色气体,常温下E的浓溶液可以使Fe钝化,写出少量Fe粉与E的浓溶液在加热条件下反应的化学方程式:_____________________。
标准状况下,将一充满C气体的试管,倒扣于水中,至液面不再升高时,再充入氧气可以使液面继续上升至充满试管。最终试管中所得溶液的浓度为____________mol/L。(假设试管中溶质不扩散)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.现有A、B、C、D、E(A、B、C、D、E分别代表元素符号)五种短周期元素,已知他们的原子序数依次增大,元素A的原子只有一个电子层;又知元素A能分别与元素B、C、D形成电子总数相等的化合物分子X、Y、Z,Y有刺激性气味,Z常温下为液态,元素E的单质的水溶液有漂白性。
请回答下列问题:
(1)元素C在周期表中的位置是( )。
(2)①化合物Y 与元素 C的最高正价氧化物的水化物恰好完全反应时 ,其生成物的水溶液呈( )性(填“酸”“碱”或“中”),其原因是(用离子方程式表示)( ) 。
②在所得生成物的水溶液中,存在着如下关系,试用离子浓度符号填写在空白处,完成下列等式: C(H+) + C(NH4+) = C(OH-) +( )。
(3)元素E的单质和石灰乳反应制漂白粉的化学反应方程式 ( ) 。
(4)A、B、D三种元素可以形成最简式为A4B2D且有香味的有机物,该有机物在酸性条件下可以水解,生成含碳原子数相同的两种常见有机物。则这种有香味的有机物在一定条件下水解的化学方程式是 ( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26. W、X、Y、Z、M、Q均为除稀有气体外的短周期元素,其原子序数依次增大,X的最外层电子数是W的4倍,Z与M的最低负化合价相同,X、M在周期表中位置如图所示。
(1)Q在周期表中的位置为( );
(2)Z与W形成的4核分子的结构式为( );
(3)由W、Y、Z、M组成的离子化合物在溶液中相互反应的离子方程式为:( )。
(4)W2与Z2反应生成化合物甲,W2与Q2反应生成化合物乙。
已知反应:乙(g)+Z2(g)→甲(g)+Q2(g),每生成1 mol Q2放热57.8 kJ。写出该反应的热化学方程式:( );
(5)X、Y可分别与Z以原子个数比1∶1形成化合物丙和丁。在催化剂存在条件下,丙与丁发生可逆反应,生成单质Y2和另一种化合物戊。写出该反应的化学方程式:( ),该反应的平衡常数表达式为 ( );
(6)将1 mol丙气体和1 mol丁气体充入一装有催化剂的恒压容器中,充分反应达平衡后:
①若气体体积较原来减少20%,则丁的转化率为 ( ) ;
②若仅将压强缩小为原来的一半,再次达平衡后,混合气体中丁的体积分数将( )(填变大、变小或不变)。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.元素X、Y、Z原子序数之和为37,X、Y在同一周期,X+、Z—具有相同的核外电子层结构。下列推测不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析