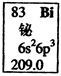- 原子核外电子排布
- 共93题
(1)中国古代四大发明之一——黑火药,它的爆炸反应为
2KNO3+3C+S
①除S外,上列元素的电负性从大到小依次为 。
②在生成物中,A的晶体类型为 ,含极性共价键的分子的中心原子轨道杂化类型为 。
③已知



(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为 ,
(3


[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]x++xH+
交换出来的
将含0.0015 mol 

正确答案
(1)①

(2)
(3)
解析
(1)①钾为活泼金属,电负性比较小;C、N、O在同周期,非金属性逐渐增强,电负性也逐渐增大;②











(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,应该都属于元素Ⅷ,原子序数T比Q多2,可以确定T为




(3)中和生成的




知识点
元素周期表中铋元素的数据见右图,下列说法正确的是
正确答案
解析
本题考查原子结构,意在考查考生对元素周期表知识记忆的再现。由元素周期表中元素方格中各种符号、数字的意义可知Bi的质子数为83,因不知中子数,无法确定其质量数,A项错误;Bi的相对原子质量为209.0,B项正确;6p亚层有3个未成对电子,C项错误;最外层5个电子分别在s、P层,能量不同,D项错误。
知识点
(一)下列有关元素锗及其化合物的叙述中正确的是
A.锗的第一电离能高于碳而电负性低于碳
B.四氯化锗与四氯化碳分子都是四面体构型
C.二氧化锗与二氧化碳都是非极性的气体化合物
D.锗和碳都存在具有原子晶体结构的单质
(二)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列问题:
(1)铜原子基态电子排布式为 ;
(2)用晶体的X射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm。又知铜的密度为9.00g·cm-3,则铜晶胞的体积是
cm3、晶胞的质量是 g,阿伏加德罗常数为 (列式计算,己知Ar(Cu)=63.6);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 ;
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是 ,反应的化学方应程式为 。
正确答案
(一) BD
(二)
(1)1s22s22p63s23p63d104s1
(2)4.7×10-23cm3 4.23×10-22g Ar(Cu)=63.6g/mol=×NA,得NA=6.01×1023mol-1。
(3)sp3 K2CuCl3
(4)过氧化氢为氧化剂,氨与Cu形成配离子,两者相互促进使反应进行。
解析
(一)锗是金属而碳是非金属元素,第一电离能要低于碳,故A错;C和Ge都是第ⅣA族元素,四氯化锗与四氯化碳都是分子晶体,其分子构型相同,故B正确;锗是金属,金属的氧化物不可能为气体化合物,故C错;锗和碳是同主族元素,晶体结构具有一定的相似性,故D正确。
(二)
(1)铜是29号元素,其基态原子的电子排布式为:1s22s22p63s23p63d104s1。
(2)铜的晶胞为面心立方最密堆积,一个晶胞能分摊到4个Cu原子;1pm=10-10cm,故一个晶胞的体积为(361×10-10cm)3=4.7×10-23cm3;一个晶胞的质量为4.7×10-23cm3×9.00g·cm-3=

(3) KCuCl3中Cu元素的化合价为+2,则另一种无限长链结构中的Cu元素的化合价为+1,CuCl3原子团的化合价为-2,故其化学式为K2CuCl3。
(4)“金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应”,这是两种物质共同作用的结果:过氧化氢具有强氧化性,而氨水能与Cu2+形成配合物。
知识点
16O和18O是氧元素的两种核素,NA表示阿弗加德罗常数,下列说法真确的是
正确答案
解析
A中的两种物质是同一种物质,都是氧气,故A错;B中的两种氧原子的电子数相等,核外电子排布也相等,故B错;16O、18O之间的转换,是原子核的变化,故C错;11.2L标况下的O2物质的量为0.05mol,含有的氧原子数为0.1NA,故D正确。
知识点
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
正确答案
解析
短周期中最外层电子数是次外层电子数一半的有Li:

知识点
扫码查看完整答案与解析