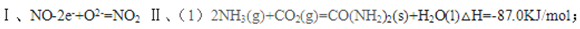- 常见金属的活动性顺序及其应用
- 共63题
22.2015年九月末爆发的德国大众柴油车尾气排放作弊事件引起了公众的关注。柴油车尾气中常含有大量氮氧化物,通常会采用喷射尿素溶液的方法,将有毒的氮氧化物还原成无污染的物质。大众选择了一种违规做法,即在客户平时用车时不开启喷射尿素的尾气后处理系统,而是通过软件让这一系统只在尾气排放检测时启动
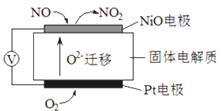
Ⅰ、通过NOx传感器可监测空气的NOx的含量,其工作原理图如下图,写出NiO电极的电极反应式_________________;
Ⅱ、以CO2与NH3为原料可合成尿素。已知:
①2NH3(g)+CO2(g)=NH2CO2 NH4(s)+l59.5kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)-116.5kJ•mol-1
③H2O(l)=H2O(g)-44.0kJ•mol-1
(1)写出CO2与NH3合成尿素和液态水的热化学反应方程式___________;
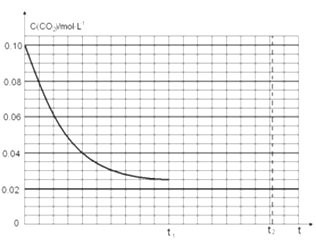
(2)恒温下将0.8molNH3和0.4molCO2放入容积为4L的密闭容器中,反应生成NH2CO2NH4(s),t1时达到平衡。则平衡时CO2的转化率是_______________。若其他条件不变,t1时将容器体积压缩到2L。请画出t1后c(CO2)随时间t变化曲线(t2达到新的平衡)。
Ⅲ、尿素在一定温度下可分解生成NH3,NH3催化还原NxOy可以消除氮氧化物的污染。已知:反应a:4NH3(g)+6NO(g)


(1)相同条件下,反应a在2L密闭容器内,选用不同的催化剂,反应产物N2的量随时间变化如图所示。下列说法正确的是________________。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(2)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体,NO2体积分数_____(填“变大”、“变小”或“不变”);
(3)恒温恒容容器中,反应c达到平衡;若起始投料相同,起始温度和压强相同,若反应在恒温恒压容器中进行,则NH3的转化率将_____________(填“变大”、“变小”或“不变”)。
正确答案
(2)75% ;
Ⅲ、(1)AD (2)变大 (3)变大
解析
I NiO 电极上NO失去电子生成NO2为负极,发生氧化反应,NiO 电极的电极反应式:NO-2e-+O2-=NO2。
II(1)依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式。依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0KJ/mol;
(2)在恒温下将0.4mol NH3和0.2mol CO2放入容积为2L的密闭容器中,达到平衡时, 2NH3(g)+CO2(g)⇌NH2CO2NH4(s)
起始量(mol/L) 0.2 0.1 0
变化量(mol/L) 0.15 0.075
平衡量(mol/L) 0.05 0.025
进而可以求出转化率=0.15/0.2=75%;t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如图所示。若其他条件不变,t1时将容器体积压缩到1L,二氧化碳浓度应增大到0.05mol/L,压强增大,平衡正向进行,由于生成物是固体,所以达到平衡状态,二氧化碳浓度保持不变,据此画出变化曲线为:,故答案为:75%
Ⅲ、(1)A.由于A点生成的N2大于B点,即条件A的反应速率大于B,活化能越小,反应速率越大,Ea(B)>Ea(A),同理可知Ea(C)>Ea(B),所以该反应的活化能大小顺序是:Ea(C)>Ea(B)>Ea(A),所以A错误。B.增大压强,使浓度增大,活化分子浓度增加,而活化分子百分数不变所以,B错误;C.单位时间内H-O键与N-H键断裂的数目相等时,说明正逆反应速率相等,反应已经达到平衡,所以C正确;D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明容器中温度不发言变化,即反应已经达到平衡,所以C正确。故答案为:CD
(2)一定条件下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,恒温恒压条件下,再充入NO2气体,则与原来的平衡为等效平衡,则NO2体积分数与原来平衡相同;若恒温恒容容器中,再充入NO2气体,容器中压强增大,与原来平衡相比较,平衡正向移动,则NO2体积分数变大;故答案为:变大。
(3)恒温恒容容器中,反应4NH3(g)+6NO2(g)
考查方向
考查了原电池电极反应的书写、题考查了化学平衡影响因素分析判断、平衡常数的应用、反应速率计算、平衡状态的判断等,侧重于考查学生对基础知识的综合应用能力。
解题思路
I NiO 电极上NO失去电子生成NO2为负极,发生氧化反应,NiO 电极的电极反应式:NO-2e-+O2-=NO2。
II(1)依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式。依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-87.0KJ/mol;
(2)在恒温下将0.4mol NH3和0.2mol CO2放入容积为2L的密闭容器中,达到平衡时,
2NH3(g)+CO2(g)⇌NH2CO2NH4(s)
起始量(mol/L) 0.2 0.1 0
变化量(mol/L) 0.15 0.075
平衡量(mol/L) 0.05 0.025
进而可以求出转化率;t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如图所示。若其他条件不变,t1时将容器体积压缩到1L,二氧化碳浓度应增大到0.05mol/L,压强增大,平衡正向进行,由于生成物是固体,所以达到平衡状态,二氧化碳浓度保持不变;
Ⅲ、(1)A.相同时间内生成的氮气的物质的量越多,则反应速率越快,活化能越低,所以该反应的活化能大小顺序是:Ea(A)<Ea(B)<Ea(C)。
B.增大压强,使浓度增大,活化分子浓度增加,而活化分子百分数不变;
C.单位时间内H-O键与N-H键断裂的数目相等时,说明正逆反应速率相等,反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明容器中温度不发言变化,即反应已经达到平衡。
(2)一定条件下,反应2NO(g)+O2(g)
(3)恒温恒容容器中,反应4NH3(g)+6NO2(g)
易错点
不能准确判断电极材料致错、不能熟练应用盖斯定律致错,没有理解化学平衡的本质特点致错。
知识点
6.下列反应中,反应后固体质量一定减少的是
正确答案
解析
A.水蒸气通过Na2O2固体生成氢氧化钠和氧气,2Na2O2+2H2O = 4NaOH+O2↑,固体质量增加,错误;
B.镁粉投入FeCl3溶液中,在FeCl3溶液中存在 FeCl3+3H2O
C.铝粉与Fe2O3发生铝热反应,Fe2O3+2Al=Al2O3+2Fe,固体质量不变,错误;
D.焦炭在电炉中还原二氧化硅,SiO2+2C
故选D。
考查方向
解题思路
A.2Na2O2+2H2O = 4NaOH+O2↑,固体质量增加;
B.镁粉投入FeCl3溶液中,在FeCl3溶液中存在 FeCl3+3H2O
C.铝粉与Fe2O3发生铝热反应,Fe2O3+2Al=Al2O3+2Fe,固体质量不变;
D.焦炭在电炉中还原二氧化硅,SiO2+2C
易错点
正确书写化学反应方程式。
知识点
11.下列离子方程式正确的是
正确答案
解析
A.氯化铝溶液中加入过量氨水,生成氢氧化铝白色沉淀,沉淀不溶解,错误;
B.MgSO4溶液中加入Ba(OH)2溶液,生成硫酸钡白色沉淀、氢氧化镁白色沉淀,错误;
C.硫化钠溶液显碱性,主要发生一级水解,错误;
D.NaHCO3溶液加入少量Ca(OH)2溶液,会产生碳酸钙白色沉淀、碳酸根离子,正确;故选D。
考查方向
解题思路
A.氯化铝溶液中加入过量氨水,生成氢氧化铝白色沉淀,沉淀不溶解;
B.MgSO4溶液中加入Ba(OH)2溶液,生成硫酸钡白色沉淀、氢氧化镁白色沉淀;
C.硫化钠溶液显碱性,主要发生一级水解;
D.NaHCO3溶液加入少量Ca(OH)2溶液,会产生碳酸钙白色沉淀、碳酸根离子;
易错点
NaHCO3溶液加入少量Ca(OH)2溶液,会产生碳酸钙白色沉淀、碳酸根离子
知识点
12.下列说法正确的是
正确答案
解析
A.锡、铁和电解质溶液构成原电池,铁易失电子而作负极,锡作正极,作负极的金属加速被腐蚀,所以镀层不再对铁制品起保护作用,错误;
B.用铜作电极电解稀硫酸时,阳极:Cu-2e-=Cu2+,阴极:2H+ +2e-=H2↑,总反应Cu+H2SO4 
C.某原电池的电极材料分别为Mg和Al,若电解质溶液为氢氧化钠,则Mg做正极,错误;
D.某可逆反应升高温度,活化能大的方向,活化分子百分数增加更多,化学反应速率增大程度大,错误;故选B。
考查方向
解题思路
A.锡、铁和电解质溶液构成原电池,锡作正极,作负极的金属加速被腐蚀,所以镀层不再对铁制品起保护作用;
B.用铜作电极电解稀硫酸时,阳极:Cu-2e-=Cu2+,阴极:2H+ +2e-=H2↑;
C.Mg和Al,若电解质溶液为氢氧化钠,则Mg做正极;
D.某可逆反应升高温度,活化能大的方向,活化分子百分数增加更多,化学反应速率增大程度大;
易错点
某可逆反应升高温度,活化能大的方向,活化分子百分数增加更多,化学反应速率增大程度大
知识点
17.硫化亚铁是一种黑色块状固体,常温下难溶于水,易溶于酸而生成能溶于水的硫化氢气体。硫化亚铁在空气中煅烧时生成二氧化硫气体和烧渣。
(1)实验室常用FeS固体与酸反应制取H2S。已知l0℃时,FeSO4· 7H2O的溶解度是20.5g,FeCl2·4H2O的溶解度是64.5g。从氧化还原反应、平衡移动和产品纯度等角度分析,实验室制取H2S时最好选用的酸是_____(填字母)。
a.浓硫酸
b.盐酸
c.稀硫酸
d.稀硝酸
实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置可选用的是______(填序号)。
(2)硫化亚铁煅烧得到的烧渣的主要成分为FeO、Fe3O4和Fe2O3等。利用该烧渣制备铁红和副产品无氯钾肥的流程如下:
已知四种盐的溶解度随温度变化的曲线如右图所示。请回答下列问题:
①检验加入铁粉过滤后的滤液中是否含有Fe3+的方法是__________。该滤液加入NH4HCO3发生反应的离子方程式是________________。
②(NH4)2SO4溶液加入KCl后得到无氯钾肥应进行的操作为______、_____、洗涤、干燥等;反应的化学方程式为_______________。
③实验室煅烧FeCO3(s)的操作中需要的仪器除了三脚架、泥三角、酒精灯,还需要_________________________。
(3)FeS煅烧后生成的SO2通入下列装置:
该实验的目的是_______。若将SO2通入水中制成饱和溶液,请设计实验证明亚硫酸是弱电解质。实验方案__________。(提供的药品及仪器:蒸馏水、0.1 mol·L-1的NaOH溶液;pH计,其他仪器自选)
正确答案
(1)c;bc;
(2)①向过滤后的滤液中加入硫氰化钾(KSCN)若溶液变血红色,证明含有铁离子(Fe3+),否则无铁离子(Fe3+);2HCO3-+Fe2+=FeCO3↓+CO2↑+H2O;
②蒸发结晶、热过滤;(NH4)2SO4+2KCl=K2SO4↓+2NH4Cl;
③玻璃棒、坩埚、坩埚钳;
(3)比较亚硫酸和碳酸的酸性强弱;
解析
(1)实验室常用FeS固体与酸反应制取H2S,浓硫酸和稀硝酸有强烈的氧化性,硫化氢有还原性,a、d不选,盐酸有挥发性,使得制得的硫化氢气体不纯净,且FeSO4· 7H2O的溶解度较小,有利于平衡正向移动,故选c;
实验室制取H2S时,属于固液不加热,发生装置bc;
(2)①检验加入铁粉过滤后的滤液中是否含有Fe3+的方法是:向过滤后的滤液中加入硫氰化钾(KSCN)若溶液变血红色,证明含有铁离子(Fe3+),否则无铁离子(Fe3+);该滤液加入NH4HCO3,反应生成碳酸亚铁、二氧化碳和水,发生反应的离子方程式是2HCO3-+Fe2+=FeCO3↓+CO2↑+H2O;
②硫酸钾的溶解度相对其他几种物质较小,蒸发后首先结晶析出,因此(NH4)2SO4溶液加入KCl后得到无氯钾肥应进行的操作为蒸发结晶,热过滤洗涤、干燥等;反应的化学方程式为(NH4)2SO4+2KCl=K2SO4↓+2NH4Cl;
③实验室煅烧FeCO3(s)的操作中需要的仪器除了三脚架、泥三角、酒精灯,还需要玻璃棒、坩埚、坩埚钳;
(3)该实验的目的是比较亚硫酸和碳酸的酸性强弱;若将SO2通入水中制成饱和溶液,请设计实验证明亚硫酸是弱电解质。实验方案__________。(提供的药品及仪器:蒸馏水、0.1 mol·L-1的NaOH溶液;pH计,其他仪器自选)
考查方向
解题思路
使学生对发生装置、收集装置、尾气处理装置的选择条件有个更好的理解,同时让学生掌握实验方案的设计。
易错点
实验方案的设计
知识点
扫码查看完整答案与解析