- 弱电解质在水溶液中的电离平衡
- 共87题
21.【选做题】本题包括A、B两小题,请选定其中一个小题,并在相应的答题区域内作答。若多做,则按A小题评分。

[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2-+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为____________________。
(2)1 mol HCHO分子中含有σ键的数目为____________mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________。
(4)与H2O分子互为等电子体的阴离子为________________。
(5)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为_____________。
材料B.[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
正确答案
(1)1s22s22p62s23p63d10(或[Ar] 3d10)(2)3;(3)sp3和sp;(4)NH2-;
(5)
(1)2SO2+CO32-+H2O=2HSO3-+CO2 (2)防止倒吸 (3)①抽滤瓶;
②减少Na2S2O5的在水中的溶解;
(4)在制备过程中Na2S2O5分解生成生Na2SO3,Na2SO3被氧化生成Na2SO4。
知识点
8.10 mL浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成的是
正确答案
解析
A.K2SO4溶液不改变盐酸中H+的量,就不影响H2的生成量,但却能稀释盐酸,降低H+的浓度,就减慢了反应速率,故为符合题意选项之一;B.CH3COONa因能结合H+且还能电离出H+,故能减慢反应速率但又不影响氢气生成,为符合题意的选项之一;C.CuSO4 加入会因置换出的铜与锌形成原电池,加快反应;D.Na2CO3会消耗盐酸而使生成氢气的量减少。
考查方向
解题思路
依据影响反应速率的原理及因素去筛选。
易错点
易忽视K2SO4溶液的稀释作用而漏选A。
知识点
6.下列有关分类的说法正确的是
正确答案
解析
A.胶体的本质特征是分散质颗粒的直径是介于1nm~100nm之间,而丁达乐效应是胶体的表观特征,所以A错误。B.阳离子、阴离子中均分别只含有一种元素,则由这样的阴、阳离子组成的物质不一定是纯净物,如FeCl2与FeCl3,考查变价元素的性质,所以A错误。C.由于白磷和红磷的的分子结构不一样,所以白磷转化为红磷是化学变化,C错误。D.碱性氧化物一定是金属氧化物,酸性氧化物,不一定是非金属氧化物,比如CrO3是酸性氧化物,所以D正确。
考查方向
解题思路
A.胶体的本质特征是分散质颗粒的直径是介于1nm~100nm之间,B.阳离子、阴离子中均分别只含有一种元素,则由这样的阴、阳离子组成的物质不一定是纯净物,如FeCl2与FeCl3,考查变价元素的性质。C.在隔绝空气条件下,白磷加热到260℃时就回转化为红磷;红磷加热到416℃时就升华,其蒸气冷却后变成白磷,白磷和红磷的的分子结构不一样,所以白磷转化为红磷是化学变化,D.金属氧化物,不一定是碱性氧化物,比如CrO3是酸性氧化物,非金属氧化物,不一定是酸性氧化物,比如NO是不成盐氧化物,酸性氧化物,不一定是非金属氧化物,比如CrO3是酸性氧化物,碱性氧化物,一定是金属氧化物。
易错点
胶体的最本质的特征是分散质颗粒的直径在1nm~100nm之间;阳离子、阴离子中均分别只含有一种元素,则由这样的阴、阳离子组成的物质一定是纯净物,如FeCl2与FeCl3
知识点
23.酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、NH4Cl等组成的糊状填充物,其结构如下图。该电池在放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH回收处理该废旧电池可以得到多种化工原料,有关数据下图所示:溶解度/(g/100g水)
某化学课外小组设计了如下废旧电池综合利用工艺(不考虑废旧电池中实际存在的少量其他金属):
回答下列问题:
(1)该酸性锌锰干电池放电时的正极反应式为________________;
(2)晶体A的化学式为________________;
(3)操作③的名称为________________;
(4)从MnO2获得K2MnO4的反应方程式为________________;
(5)用废电池的锌皮制作ZnSO4·7H2O,需去除少量杂质铁,其方法是:
①加入足量的稀H2SO4和H2O2溶解。加入H2O2反应的离子方程式是________;
②加碱调节pH为________,使铁刚好完全沉淀,过滤。向滤液中继续加碱调节pH使锌刚好完全沉淀。过滤、洗涤。
③将沉淀溶于稀H2SO4,经过___________________(答操作名称)、过滤、洗涤、干燥得到ZnSO4·7H2O,晶体用冷水洗涤的原因是__________________________。
正确答案
(1)MnO2+e-+NH4+=MnOOH+NH3
(2)NH4Cl
(3)在空气中灼烧
(4)3MnO2+KClO3+6KOH=3K2MnO4+KCl+3H2O
(5)①2Fe2++H2O2+2H+=2Fe3++2H2O
②3
③蒸发浓缩、冷却结晶 降低晶体的溶解度,减少损失
解析
(1)MnO2做正极,由MnO2得电子,电极反应为MnO2+e-+NH4+=MnOOH+NH3;故答案为:MnO2+e-+NH4+=MnOOH+NH3;
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有NH4Cl和ZnCl2,两个溶解度一个受温度影响较大,一个较小,可用重结晶法,二者可通过加热浓缩,冷却结晶分离回收,NH4Cl溶解度小,所以先析出NH4Cl晶体,故答案为:NH4Cl;
(3)碳粉和MnOOH都不溶,所以最后还有碳粉和MnOOH,根据碳粉和MnOOH性质,在空气中加热碳粉变为二氧化碳,MnOOH变为MnO2,故答案为:在空气中灼烧。
(4)MnO2 在熔融状态下与KClO3、6KOH发生氧化还原反应生成K2MnO4,故答案为:3MnO2+KClO3+6KOH=3K2MnO4+KCl+3H2O;
(5)①在酸性条件下Fe变为Fe2+ ,具有强氧化性的H2O2把Fe2+变成三价铁离子,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②根据溶度积原理,Ksp[Fe(OH)3]= c(Fe3+)×c(OH-)3,c(OH-)3= Ksp[Fe(OH)3]/ c(Fe3+)=10-39/10-5==10-34,c(H+)=Kw/c(OH-)=10-2.7,所以pH为2.7,故答案为:2.7。
③由于ZnSO4·7H2O容易分解失去结晶水,所以要通过蒸发浓缩、冷却结晶后再过滤,同时由于ZnSO4·7H2O的溶解度随温度的升高而增大,因此用冰水洗涤的目的是减少洗涤过程中ZnSO4·7H2O的损耗,故答案为:蒸发浓缩、冷却结晶;降低晶体的溶解度,减少损失。
考查方向
以酸性锌锰干电池为载体,考查电极反应的书写、化学实验操作、化学方程式及离子方程式的书写、物质的分离提纯的方法等中学化学核心知识。考查了学生对知识理解、综合运用能力及阅读材料、接受信息的能力和思维能力,对相关知识的掌握情况。
解题思路
(1)MnO2做正极,由MnO2得电子生成MnOOH。
(2)废电池糊状填充物加水处理后,过滤,滤液中主要有NH4Cl和ZnCl2,两个溶解度一个受温度影响较大,一个较小,可用重结晶法,二者可通过加热浓缩,冷却结晶分离回收,NH4Cl溶解度小,所以先析出NH4Cl晶体;
(3)碳粉和MnOOH都不溶,所以最后还有碳粉和MnOOH,根据碳粉和MnOOH性质,在空气中加热碳粉变为二氧化碳,MnOOH变为MnO2;
(4)MnO2 在熔融状态下与KClO3、6KOH发生氧化还原反应生成K2MnO4;
(5)①在酸性条件下Fe变为Fe2+ ,具有强氧化性的H2O2把Fe2+变成三价铁离子,
②根据溶度积原理,Ksp[Fe(OH)3]= c(Fe3+)×c(OH-)3,进而求解pH。
③由于ZnSO4·7H2O的溶解度随温度的升高而增大,因此用冰水洗涤的目的是减少洗涤过程中ZnSO4·7H2O的损耗。
易错点
不能有效提取图表中信息,阅读材料、接受信息的能力不强,物质的分离提纯的方法掌握不熟练。
知识点
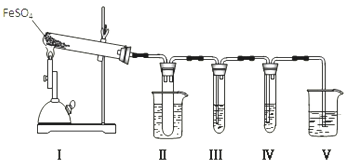
21.已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物。已知SO3的熔点是16.8℃,沸点是44.8℃。
(1)装置Ⅱ的试管中不装任何试剂,其作用是______,试管浸泡在50℃的水浴中,目的是______;
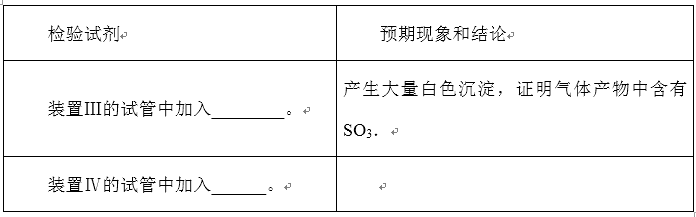
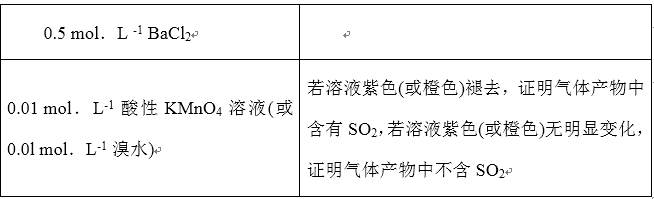
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分.请完成实验设计,填写检验试剂、预期现象与结论.限选试剂:3mol•L-1 H2SO4、6mol•L-1 NaOH、0.5mol•L-1 BaCl2、0.5mol•L-1 Ba(NO3)2、0.01mol•L-1酸性KMnO4溶液、0.01mol•L-1溴水.
(3)也有同学认为可以通过检验试管中残留固体证明分解产物。方案如下:取适量残留固体于试管中,加入足量稀硫酸,将所得溶液分为两份。向第一份溶液中滴加硫氰化钾溶液,若变红,证明分解产物中有氧化铁;向第二份溶液滴加酸性高锰钾溶液,若褪色证明分解产物中有氧化亚铁。
①写出第一份溶液中反应的离子方程式_____________________________;
②有同学认为高锰酸钾溶液褪色不能说明分解产物有氧化亚铁,理由是_________;
正确答案
(1)防止溶液倒吸入装置Ⅰ中(或安全瓶);防止SO3液化或凝固
(2)
(3)①Fe3++3SCN-
②如果FeSO4未完全分解,溶液里也存在Fe2+;
解析
(1)Ⅰ中产生的气体极易和溶液反应时,会产生倒吸,所以装置II的试管能防止溶液倒吸入装置Ⅰ中(或安全瓶);SO3的沸点是44.8°C,当温度高于44.8°C时SO3为气体状态,把试管浸泡在50℃的热水浴中能防止SO3液化或凝固,故答案为:防止溶液倒吸入装置Ⅰ中(或安全瓶);防止SO3液化或凝固;
(2)根据FeSO4分解的气体产物可能为SO3,也可能是SO3和SO2的混合物,SO3遇到钡离子生成白色沉淀,所以用0.5 mol.L -1 BaCl2检验SO3;SO2能使高锰酸钾或溴水褪色,所以选用0.01 mol.L-1 酸性 KMnO4 溶液(或0.0l mol.L-1 溴水)检验SO2;若则溶液紫色(或橙色)褪去,证明气体产物中含有SO2,若溶液紫色(或橙色)无明显变化,证明气体产物中不含SO2;故答案如下:
(3)①能使硫氰化钾溶液变红,证明溶液中有Fe3+,故反应的离子方程式为:Fe3++3SCN-
考查方向
通过二氧化硫和二氧化硫的检验考查了考生实验仪器的使用以及实验方案的设计能力与实验探究能力。
解题思路
(1)Ⅰ中产生的气体极易和溶液反应时,会产生倒吸,所以装置II的试管能防止溶液倒吸入装置Ⅰ中(或安全瓶);SO3的沸点是44.8°C,当温度高于44.8°C时SO3为气体状态,把试管浸泡在50℃的热水浴中能防止SO3液化或凝固;
(2)根据FeSO4分解的气体产物可能为SO3,也可能是SO3和SO2的混合物,SO3遇到钡离子生成白色沉淀,SO2能使高锰酸钾或溴水褪色;
(3)①向第一份溶液中滴加硫氰化钾溶液,变红,证明溶液中有Fe3+②酸性高锰钾溶液褪色只能证明在溶液里存在Fe2+;
易错点
不能准确提取题中有效信息(数据信息和装置图中信息),不了解酸性 KMnO4 溶液检验Fe2+的来源。
知识点
扫码查看完整答案与解析