- 化学用语
- 共784题
9.类比思维是化学解题中常用的一种思维方法,下列有关离子方程式推理正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列离子方程式书写正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.一定浓度NaHCO3溶液与CuSO4溶液中反应后生成了蓝绿色颗粒状沉淀。就沉淀成分提出了如下三种假设:假设一:沉淀是CuCO3; 假设二:沉淀是Cu(OH)2; 假设三:沉淀是CuCO3和Cu(OH)2的混合物
(1)写出假设二沉淀是Cu(OH)2生成的理由( )(用离子方程式表示)
(2)为了探究沉淀的成分,取出了一部分沉淀,滴加稀盐酸,有气体放出。凭此现象,判断沉淀中含有( )
(3)为了进一步探究沉淀的成份,进而确定假设中何种假设成立,设计实验,装置图如下:
①研究沉淀物组成前,须将沉淀从溶液中分离并净化。具体操作依次为( ) 、洗涤、干燥;
②装置E中药品的名称是 ( ) ,作用为( )
③实验过程中有以下操作步骤:
a.打开K1、K3,关闭K2、K4,通入过量空气。此步骤的作用是( )
b.关闭K1、K3,打开K2、K4,充分反应( )
c.再通入过量空气时,活塞处于打开的是( ) ,关闭的是( )
④若沉淀样品的质量为m g,装置D的质量增加了n g;若沉淀样品为纯净物,m、n之间的关系为n=( ) 若假设三成立,则Cu(OH)2的质量分数为( ) ;若不进行步骤C,则会使测得结果 ( ) 填“偏高”“无影响”“偏低”)
正确答案
答案已在路上飞奔,马上就到!
解析
知识点
28.以钡矿粉(主要成份为BaCO3,含有Ca2+、Fe2+、Fe3+、Mg2+等)制备BaCl2·2H2O的流程如下:
(1)氧化过程主要反应的离子方程式为( )。
(2)沉淀C的主要成分是Ca(OH)2和( )。由图可知,为了更好的使Ca2+沉淀,还应采取的措施为( )。
(3)用BaSO4重量法测定产品纯度的步骤为:
步骤1:准确称取0.4~0.6 g BaCl2·2H2O试样,加入100 ml 水,3 ml 2 mol·L-1 的HCl溶液加热溶解。
步骤2:边搅拌,边逐滴加入0.1 mol·L-1 H2SO4溶液。
步骤3:待BaSO4沉降后,( ),确认已完全沉淀。
步骤4:过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。
步骤5:将折叠的沉淀滤纸包置于( )中,经烘干、炭化、灰化后在800℃灼烧至恒重。称量计算BaCl2·2H2O中Ba2+的含量。
①步骤3所缺的操作为( )。
②若步骤1称量的样品过少,则在步骤4洗涤时可能造成的影响为( )。
③步骤5所用瓷质仪器名称为( )。滤纸灰化时空气要充足,否则BaSO4易被残留的炭还原生成BaS,该反应的化学方程式为( )。
④有同学认为用K2CrO4代替H2SO4作沉淀剂效果更好,请说明原因 ( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.下表所列各组第Ⅰ栏中的化学反应与第Ⅱ栏中的化学反应,都可以用第Ⅲ栏中的离子方程式表示的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.在复杂体系中,确认化学反应先后顺序有利于解决问题。下列反应先后顺序判断正确的( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.下列反应的离子方程式正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
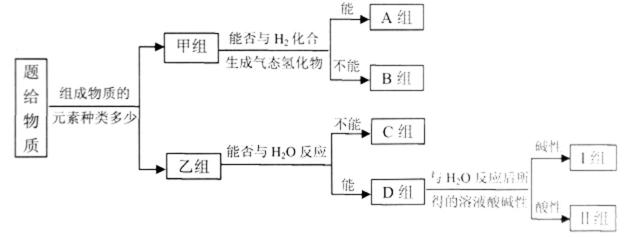
26.现有 NH3、CO、Na、Na202、Fe、NO、NO2, F2、SO2.SOCl2 等中学化学教材中出现过的物质,根据它们的组成及性质进行如下分类
请回答下列问题
(1)图中所示的分类方法叫_______________
(2)淡黄色固体最终位于_______组,它的电子式为_______。
(3)C组有一种气体常用作工业上冶炼铁的还原剂,写出高温下它还原Fe2O3的化学方程式_________。
(4)写出II组的某种物质与水发生氧化还原反应的离子方程式__________。
(5)B组中有一种物质在高温下能与水蒸气反应,若该反应过程中有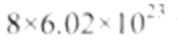
(6)II组另有一种物质滴入水中后与水激烈反应,液面上有酸雾形成,并有能使品红溶液褪色的气体逸出,该反应的化学方程式为______________
正确答案

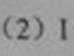

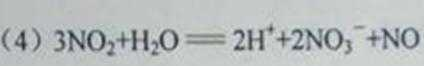
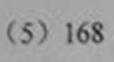
解析
解析已在路上飞奔,马上就到!
知识点
8.多硫化钠Na2Sx(X≥2)在结构上与Na2O2、FeS2等有相似之处。Na2Sx在碱性溶液中与NaClO反应可生成Na2SO4,下列说法不正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.下列离子方程式正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析