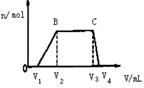- 化学用语
- 共784题
28.1L某混合溶液,可能含有的离子如下表:
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)
与加入NaOH溶液的体积(V)的关系如右图所示。
则该溶液中一定不含有的离子是_________。
(2)BC段离子方程式为( ) 。
(3)V1 、V2、 V3、 V4之间的关系*( ) 。
(4)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的
Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为___________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为____________________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)写出N2H62+在碱性溶液中反应的离子方程式( ) 。
(2)NH2-的电子式为( )。
(3)N3-有 ( )个电子。
(4)写出二种由多个原子组成的含有与N3-电子数相同的物质的化学式( ) 、( )。
(5)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列解释事实的化学方程式或离子方程式,不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9. 著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。 下列说法正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列评价及离子方程式书写正确的是:( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列离子方程式正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.下列离子方程式表达正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.下列离子方程式书写正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.解释下列现象的化学用语不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点

已知:
①常温下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4
②BaCO3的相对分子质量是197;BaCl2·2H2O的相对分子质量是244
回答下列问题:
(1)SiCl4发生水解反应的化学方程式为_______________________________________
(2)用H2还原SiCl4蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59KJ热量,则该反应的热化学方程式为_____________________________________________
(3)加钡矿粉并调节pH=7的目的是① ( ),② ( )
(4)过滤②后的滤液中Fe3+浓度为 ( )(滤液温度25℃,Ksp[Fe(OH)3]=2.2×10-38)
(5)生成滤渣A的离子方程式__________________________________________
(6)列式计算出10吨含78.8% BaCO3的钡矿粉理论上最多能生成BaCl2·2H2O的质量为多少吨?
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析