- 化学平衡的计算
- 共48题
硼酸(H3BO3)在食品、医药领域应用广泛。
(1)请完成B2H6气体与水反应的化学方程式:B2H6 + 6H2O=2H3BO3 +________。
(2)在其他条件相同时,反应H3BO3 +3CH3OHB(OCH3)3 +3H2O中,H3BO 3的转化率(
① 温度对应该反应的反应速率和平衡移动的影响是_______.
② 该反应的
(3)H3BO 3溶液中存在如下反应:
H3BO 3(aq)+H2O(l)=[B(OH)4]-( aq)+H+(aq).已知0.70 mol·L-1 H3BO 3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2. 0 × 10-5mol·L-1,c平衡(H3BO 3)
正确答案
(1)B2H6 + 6H2O=2H3BO3 +6H2
(2) ①升高温度,反应速率加快,平衡正向移动
② >
(3)解依题意 H3BO 3(aq)+H2O(l)= [B(OH)4]-( aq)+H+(aq)
解析
略
知识点
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
①Ni(S)+4CO(g)

完成下列填空:
(1)在温度不变的情况下,要提高反应(1)中Ni(CO4)的产率,可采取的措施有 、 。
(2)已知在一定条件下的2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如下图所示。Ni(CO)4在0~10min的平均反应速率为 。
(3)若反应(2)达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 。
A.平衡常数K增大
B.CO的浓度减小
C.Ni的质量减小
D.v逆[Ni(CO)4]增大
(4)简述羰基法提纯粗镍的操作过程。
正确答案
(1)增大CO浓度,加压。
(2)0.05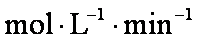
(3)bc。
(4)把粗镍和CO放于一个水平放置的密闭的玻璃容器中,然后在低温下反应,一段时间后在容器的一端加热。
解析
(1)反应(1)是正向气体体积缩小的放热反应,因此,根据平衡移动原理在温度不变的情况下采取可增大CO浓度,加压的方法提高产率;
(2)根据题意,反应的Ni为1mol,则生成

(3)反应(2)正向气体体积增大的吸热反应,降低温度平衡逆向移动,平衡常数K、CO的浓度、Ni的质量、v逆[
(4)根据反应①②的特点可提纯粗镍。
知识点
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量CO2)直接制备二甲醚,其中主要过程包括下列四个反应:
甲醇合成反应:
(i)CO(g)+2H2(g)=CH3OH(g) △H1=-90.1 kJ/mol
(ii)CO2(g)+3H2(g)=CH3OH(g)+H2O △H2=-40.9 kJ/mol
水煤气变换反应:
(iii)CO(g)+H2O(g)= CO2(g)+H2(g) △H3=-41.1 kJ/mol
二甲醚合成反应:
(iv)2CH3OH(g)= CH3OCH3(g)+H2O △H4=-24.5 kJ/mol
回答下列问题:
(1)Al2O3是合成气直接制备二甲醚反应催化剂主要成分之一。工业上从铝土矿制备高纯Al2O的主要工艺流程是 。(用化学方程式表示)
(2)分析二甲醚合成反应(iv)对CO转化率的影响 。
(3)由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为 。根据化学反应原理,增加压强对直接制备二甲醚的反应的影响 。
(4)有研究者在催化剂(含Cu-Zn-Al-O、Al2O3)、压强在5.0Mpa条件下,由H2和CO直接制备二甲醚,结果如图所示。其中CO转化率随温度升高而降低的原因是 。
(5)二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度高于甲醇直接燃料电池(5.93 kW·h·kg-1)。若电解质为酸性,二甲醚直接燃料电池的负极反应为 。一个二甲醚分子经过电化学氧化,可以产生 个电子的电量:该电池理论输出电压为1.20V,能量密度E= (列式计算,能量密度=电池输出电能/燃料质量)。
正确答案
(1)Al2O3+2NaOH+3H2O=2NaAl(OH)4
NaAl(OH)4+CO2=Al(OH)3+NaHCO3、2 Al(OH)3
(2)消耗甲醇,促进甲醇合成反应(i)平衡向右移,CO转化率增大:生成的水通过水煤气变换反应(iii)消耗部分CO。
(3)2CO(g)+4H2(g)=CH3OCH3(g)+H2O △H=-204.7 kJ/mol;该反应分子数减小,压强升高使平衡右移,CO和H2转化率增大,CH3OCH3产率增加,压强升高使CO和H2浓度增大,反应速率加快。
(4)反应放热,温度升高,平衡左移。
(5)CH3OCH3+3H2O=2CO2+12H++12e-;12;
解析
略
知识点
在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应:
反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为 。
平衡时A的转化率为_ ,列式并计算反应的平衡常数K 。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总= mol,n(A)= mol。
②下表为反应物A浓度与反应时间的数据,计算a=
正确答案
答案:
(1)升高温度、降低压强
(2)
(3)
②0.051;每间隔4小时,A的浓度为原来的一半。0.013
解析
(1)根据反应是放热反应特征和是气体分子数增大的特征,要使A的转化率增大,平衡要正向移动,可以采用升高温度、降低压强的方法。
(2)反应前气体总物质的量为0.10mol,令A的转化率为α(A),改变量为0.10α(A) mol,根据差量法,气体增加0.10α(A)mol,由阿伏加德罗定律列出关系:
平衡浓度C(C)=C(B)=0.1×94.1%=0.0941mol/L,C(A)=0.1-0.0941=0.0059mol/L,
(3)

每间隔4小时,A的浓度为原来的一半。
当反应12小时时,C(A)=0.026/2=0.013mol/L
知识点
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)
下列说法正确的是
正确答案
解析
略
知识点
扫码查看完整答案与解析