- 物质结构与性质
- 共518题
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为 。
②NO3-的空间构型 (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化成CO2,HCHO被氧化成CO2和H2O。
①根据等电子原理,CO分子的结构式为 。
②H2O分子中O原子轨道的杂化类型为 。
③1molCO2中含有的σ键数目为 。
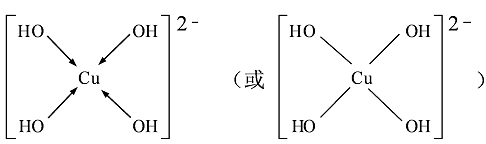
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 。
正确答案
见解析。
解析
(1)①1s22s22p63s23p63d5(或[Ar]3d5)
②平面三角形
(2)①C≡O ②sp3 ③2×6.02×1023个(或2mol)
(3)
本题科学研究铜锰氧化物作背景,考查学生对电子排布、原子轨道杂化类型与空间构型、等电子体原理、[Cu(OH)4]2-结构等《选修三》基础知识的掌握和应用能力。本题基础性较强,重点特出。
知识点
(1)依据第2周期元素第一电离能的变化规律,参照右图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:
2NH3+3F2 
①上述化学方程式中的5种物质所属的晶体类型有 (填序号)。
a。离子晶体 b。分子晶体 c,原子晶体 d。金属晶体
②基态铜原子的核外电子排布式为 。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
①晶体Q中各种微粒间的作用力不涉及 (填序号)。
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.范德华力
②R中阳离子的空间构型为 ,阴离子的中心原子轨道采用 杂化。
(4)已知苯酚(

正确答案
见解析。
解析
(1)
(2)①a、b、d ②1s22s22p63s23p63d104s1或[Ar]3d104s1
(3)①a、d ②三角锥型 sp3
(4)< 
知识点
碳族元素包括C 、Si、Ge .Sn、Pb
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过___________杂化与周围碳原子成键,多层碳纳米管的层与层之间靠___________结合在一起。
(2)CH4共用电子对偏向C,SiH4中偏向H,则C、Si、H的电负性由大到小的顺序为___________。
(3)用阶层电子对互斥理论推断SnBr2分子中Sn—Br键的键角__________120○ (填“>、<、=”)
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞定点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心。该化合物化学式为____________,每个Ba2+与________个O2-配位。
正确答案
(1)sp2 范德华力
(2)C>H >Si
(3) <
(4)PbBaO3,12。
解析
(1)石墨的每个碳原子用sp2杂化轨道与邻近的三个碳原子以共价键结合,形成无限的六边形平面网状结构,每个碳原子还有一个与碳环平面垂直的未参与杂化的2p轨道,并含有一个未成对电子,这些平面网状结构再以范德华力结合形成层状结构。因碳纳米管结构与石墨类似,可得答案。
(2)共用电子对偏向电负性大的原子,故电负性:C>H >Si。
(3) SnBr2分子中,Sn原子的价层电子对数目是(4+2)/2=3,配位原子数为2,故Sn原子含有故对电子,SnBr2空间构型为V型,键角小于120°。
(4)每个晶胞含有Pb4+:8×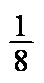
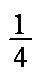
PbBaO3。Ba2+处于晶胞中心,只有1个,O2-处于晶胞棱边中心,共12个,
故每个Ba2+与12个O2-配位
知识点
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如下图所示。
①在1个晶胞中,X离子的数目为 。
②该化合物的化学式为 。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是 。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 。
(4)Y 与Z 可形成YZ2-
①YZ2-的空间构型为 (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式: 。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
正确答案
见解析。
解析
(1)①4 ②ZnS
(2)sp3
(3)水分子与乙醇分子之间形成氢键
(4)① 正四面体 ②CCl4 或SiCl4 等
(5)16 mol 或16伊6. 02×1023个
知识点
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为________,1mol Y2X2含有σ键的数目为________。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是________。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是________。
(4)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是________,它可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,反应的化学方程式为________。
正确答案
(1)sp杂化;3mol或3×6.2×10 个
(2)NH3分子存在氢键
(3)N2O
(4)CuCl;CuCl+2HCl=H2CuCl3 (或CuCl+2HCl=H2[CuCl3])
解析
略。
知识点
(一)下列描述中正确的是
A.CS2为V形的极性分子
B.Cl0— 3 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO2— 3 的中心原子均为sp3杂化
(二)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为______________________________;
(2)Ni0、Fe0的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO ________ FeO(填“<”或“>”);
(3)Ni0晶胞中Ni和O的配位数分别为_______________、_______________;
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_______________;
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是
②该结构中,氧氢之间除共价键外还可存在_______________;
③该结构中,碳原子的杂化轨道类型有_______________。
正确答案
(一)CD
(二)(1)1s22s22p63s23p63d 84s2
(2)>
(3)6、6
(4)LaNi5
(5)①一个
②氢键
③sp2、sp3
解析
(一)依据价层电子对互斥理论可知CS2为直线形的非极性分子,A错误;由价层电子对互斥理论可知Cl0— 3中中心原子的孤电子对数是1/2×(8-3×2)=1,所以Cl0— 3是三角锥形,B错误;硫原子最外层有6个电子,和氟原子之间有6对完全相同的成键电子对,C正确;SiF4和SO2— 3 的空间构型分别为正四面体和三角锥形,但中心原子均采用的是sp3杂化,D正确。
(二)(1)镍属于28号元素,根据构造原理可以写出该原子的核外电子排布式,Ni的核外电子排布式是1s22s22p63s23p63d 84s2
(2)Ni0、Fe0的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高。由于Ni2+的离子半径小于Fe2+的离子半径,属于熔点是NiO>FeO。
(3)因为Ni0、Fe0的晶体结构类型均与氯化钠的相同,而氯化钠中阴阳离子的配位数均为6,所以Ni0晶胞中Ni和O的配位数也均为6。
(4)晶胞中镧原子数=8×1/8=1;镍原子数=1+8×1/2=5,所以化学式为LaNi5
(5)①双键是由一个
知识点
X、Y、Z、R为前四周期元素且原子序数依次增大。X的单质与氢气可以化合生成气体G,其水溶液pH>7;Y单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。Y、Z分别与钠元素可以形成化合物Q和J,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M。
请回答下列问题:
(1)M固体的晶体类型是 。
(2)Y基态原子的核外电子排布式是 ;G分子中X原子的杂化轨道的类型是 。
(3)L的悬浊液加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是 。
(4)R的一种含氧酸根RO42-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是 。
正确答案
见解析。
解析
(1)M的晶体类型,M为NH4Cl,属离子晶体;
(2)Y基态原子的电子排布:1s2 2s2 2p6 3s2 3p4,G分子中X原子的杂化轨道类型为sp3杂化;
(3)AgCl悬浊液中加入Ag2S,Ksp(AgCl)<Ksp(Ag2S),则溶液中的AgCl转化为Ag2S,由白色沉淀变为黑色沉淀;
(4)R的含氧酸跟RO42-为FeO42-,向其钠盐溶液中加入硫酸,溶液变黄,说明生成Fe3+,并有无色气体生成,反应中Fe的化合价降低,只能是O元素的化合价升高,则无色气体比为O2,反应的离子方程式为:4FeO42-+20H+==4Fe3++3O2↑+10H2O
①气体G可溶于水且水溶液呈碱性,知气体G为NH3,气体G由X的单质与H2化合得到,则X为N元素。
②Y的单质为黄色晶体,知Y为S元素。
③R的3d轨道电子数为为4s轨道的三倍,则R为第四周期元素,4s轨道电子数为2,3d轨道为6,R原子的电子排布为1s2 2s2 2p6 3s2 3p6 3d6 4s2,则R为Fe元素。
④Z的原子序数大于Y,且能与Na化合,则X为Cl元素。
⑤则Q为Na2S,J为NaCl,I为AgCl,M为NH4Cl
知识点
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
(1)基态硼原子的电子排布式为_________。
(2)关于这两种晶体的说法,正确的是_________(填序号)。
a. 立方相氮化硼含有σ键和π键,所以硬度大
b. 六方相氮化硼层间作用力小,所以质地软
c. 两种晶体中的B-N键均为共价键
d. 两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为_________,其结构与石墨相似却不导电,原因是_________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为_________。该晶体的天然矿物在青藏高原在下约300Km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是_________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1mo NH4BF4含有_________mol配位键。
正确答案
(1)1s22s22p1
(2)b、c
(3)平面三角形;层状结构中没有自由移动的电子
(4)sp3;高温、高压
(5)2
解析
略。
知识点
早期发现的一种天然二十面体准晶颗粒由AI.Cu.Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体.准晶体和非晶体。
(2)基态 Fe原子有 个未成对电子,Fe3+的电子排布式为 可用硫氰化钾检验Fe3+,形成的配合物的颜色为_ 。
(3)新制备的Cu(OH)2可将乙醛〔CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为_ ,1mol乙醛分子中含有的σ健的数目为_ 。乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_ 个铜原子。
(4)Al单质为面心立方晶体,,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_ 。列式表示Al单质的密度_ g·cm-3〔不必计算出结果)。
正确答案
(1)X-射线衍射
(2)4 
(3)

6

16
(4) 12

解析
略
知识点
氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为_______个。
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为_______。

(3)H+可与H2O形成H3O+,H3O+原子采用_______杂化。H3O+中H-O-H键角比H2O中H-O-H键角大,原因为_______。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为a g·cm-3, NA表示阿伏伽德罗常数,则CaO晶胞体积为_______cm3
正确答案
(1) 2
(2)O—H键、氢键、范德华力;

(3)sp3;H2O中O原子有两对孤对电子,H3O+中O原子只有一对故对电子,排斥力较小
(4)
解析
(1)氧元素的基态核外电子排布式为:1s22s22p4,4个电子在三个轨道中排布,故未成对的电子个数是两个。
(2)化学键是强烈的相互作用;氢键的作用力比化学键弱,但比范德华力的作用力要强。

(3) H3O+的空间构型为三角锥型,故O原子的杂化方式为sp3;H3O+中O原子只有一对故对电子,排斥力较小,使得键角变大。
(4)根据NaCl的晶胞可知,一个晶胞含有4个CaO,设晶胞的体积为V,则:

知识点
石墨烯(如图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图乙)。
(1)图甲中,1号C与相邻C形成σ键的个数为_______。
(2)图乙中,1号C的杂化方式是_______,该C与相邻C形成的键角_______(填“>”“<”或“=”)图甲中1号C与相邻C形成的键角。
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有_______(填元素符号)。石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为_______,该材料的化学式为_______。
正确答案
(1)3;
(2)
(3)O、H;
(4)12;M3C60。
解析
略。
知识点
已知X,Y,Z,Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+离子只有三个电子层且完全充满电子。回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)X元素为____,X、Y、Z中第一电离能最大的是____
(2)已知Y2Q2分子存在如图所示的两种结构(球棍模型,短线不一定代表单键):
该分子中Y原子的杂化方式是____
(3)X与Y元素可以形成一种超硬新材料,其晶体部分结构如图所示,有关该晶体的说法正确的是_____(填正确答案编号)。
A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时破坏共价键
(4)有一种AB型分子与Y单质分子互为等电子体,它是一种常用的还原剂,其化学式
为______
(5)R的基态原子的电子排布式为_____,R与Z形成的某离子晶体的晶胞结构如图,则该晶体的化学式为____,该晶体的密度为
正确答案
解析
略
知识点
(1)下列分子中,属于非极性的是_______。
A. SO2
B. BeCl2
C. BBr3
D. COCl2
(2)铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为_______;
2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______;
3)SO42-的立体构型是_______,其中S原子的杂化轨道类型是_______;
4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为_______;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______;该晶体中,原子之间的作用力是_______;
5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为_______。
正确答案
(1)BC
(2)1)Cu+2H2SO4(浓)
解析
(1)根据价层电子对互斥理论(VSEPR)可得四种分子的结构如下:
(2)本题各小题内容考查点相互的联系不大,仍属于“拼盘”式题。3)硫酸根中心原子的价层电子对为:孤对电子数6-2×4+2=0,成键电子对数4,所以为正四面体结构,中心原子为sp3杂化;4)Au电子排布或类比Cu,只是电子层多两层,由于是面心立方,晶胞内N(Cu)=6×

知识点
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图为 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥结构的酸是 。(填化学式)
(4)c和e形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 。
(5)这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是 ,判断理由是 。
正确答案
(1)N
(2) 

(3)

(4) +1
(5)




解析
略
知识点
碳、氮、氧是构成生命物质的三种主要元素。
(1)碳、氮、氧三种元素中,原子核外电子未成对电子数最多的是_________(用元素符号表示)。
(2)已知CN-与N2结构相似,则HCN分子中

(3)H2O2分子中氧原子的杂化方式为_________。
(4)与NO2+互为等电子体的微粒有_________、_________(举2例),NO3-的空间构型是_________。
(5)已知元素A的氧化物的晶胞结构如图所示,则该氧化物的化学式为_________。
正确答案
(1)N
(2)1:1
(3)sp3
(4)CO2、N2O、CNO-、SCN-等;平面三角形
(5)AO2
解析
略。
知识点
扫码查看完整答案与解析