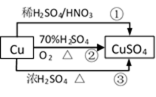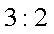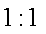- 氧化还原反应的计算
- 共67题
CuSO4是一种重要的化工原料,其有关制备途径如右图所示。下列说法不正确的是( )(已知:2Cu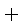
正确答案
解析
略
知识点
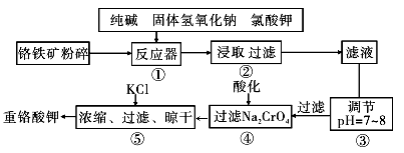
重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3,杂质为SiO2、Al2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下图。涉及的主要反应是: 6FeO·Cr2O3+24NaOH+7KClO3=12Na2CrO4+3Fe2O3+7KCl+12H2O。
(1)碱浸前将铬铁矿粉碎的目的是________。
(2)步骤③调节pH后过滤得到的滤渣是________。
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式________。
(4)用简要的文字说明操作⑤加入KC1的原因________________。
(5)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4 ·7H2O将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于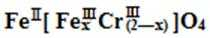
A. x =0.5 ,a =8
B. x =0.5 ,a = 10
C. x = 1.5 ,a =8
D. x = 1.5 ,a = 10
正确答案
(1)增大接触面积,增大反应速率。
(2)Al(OH)3;H2SiO3
(3)2CrO42-+2H+ 
(4)温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,利用复分解反应可以得到重铬酸钾。
(5)D
解析
略。
知识点
用A.b两个惰性电极电解0.2L一定浓度的硫酸铜溶液,当a极上产生4.48L(标况)气体时,b极上只有固体析出。然后将电源反接,当b极产生4.48L(标况)气体时,溶液质量共减少45.4克。下列说法正确的是( )
正确答案
解析
略
知识点
铜和镁的合金2.3克完全溶于浓硝酸,若反应中硝酸被还原只产生2.24升NO2和168mlN2O4(标况下),在反应后的溶液里,加入足量的氢氧化钠,产生沉 淀的质量为
正确答案
解析
略
知识点
某体系中存在如下反应:
① H2S+4H2O-8e → SO42-+10H+ ② 2IO3-+12 H++10e → I2+6H2O
(1)反应①中H2S做__________剂,反应②属于___________ 反应(填“氧化”或“还原”)。
(2)若在反应①中失去0.2 mol 电子,则反应②中可生成 g 碘。
(3) 写出并配平碘酸钾与硫化氢反应的化学方程式,同时标出电子转移的方向和数目:
_______________________________________________________________________。
(4)由上述反应可推知 。
a.氧化性:K2SO4 > KIO3 b.酸性:HIO3 > H2SO4
c.还原性: H2S > I2 d.反应过程中溶液的酸性逐渐减弱
正确答案
(1)还原,还原。
(2) 5.08 g 碘。
(3)
(4) c
解析
略
知识点
为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理使钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。其过程
① 3Fe



② Na2FeO2



③ Na2FeO2



(1)配平化学方程式②。
(2)上述反应①中还原剂为 ,被还原的是 。若有1mol Na2FeO2生成,则反应中有 mol电子转移。
(3)关于形成“发蓝”的过程,下列说法正确的是
A,该生产过程不会产生污染
B,反应③生成的四氧化三铁具有抗腐蚀作用
C,反应①②③均是氧化还原反应
D,反应①②中的氧化剂均为NaNO2
(4)当NaOH溶液浓度过大,“发蓝”的厚度会变小,其原因是: 
正确答案
(1) 6,1,5,3,1,7
(2)Fe 
(3)BD
(4)反应③可逆,氢氧化钠浓度过大,平衡向逆反应方向移动
解析
略
知识点
已知:硝酸铜受热易分解。
170℃时,2Cu (NO3)2


(其中2NO2→N2O4,2NO2

800℃时,4CuO

(1)取5.64g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分吸收后,还有逸出的气体是 (填分子式),体积(标准状况)为 ;
将吸收液加水稀释到100mL,此溶液中
(2),取5.64g无水硝酸铜加热至某温度分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是 。
实验证明,当温度达到1800℃时,Cu2O也会发生分解:2Cu2O

(3),取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,通过计算求出反应后剩余固体中各成分的物质的量之比。
(4)取8.00g CuO,通入一定量H2并加热,使其部分还原为Cu和Cu2O,且其中
n (Cu2O)





充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
正确答案
(1)O2,0.168L,0.6mol/L
(2)3.48g或2.32g
(3)n(Cu2O):n(Cu)=3:4
(4)nCuO=0.1—(y+2xy)/64(1+x)
解析
略
知识点
双氧水可作为采矿业废液的处理剂,如用来消除采矿废液中的氰化物,反应方程式如下:
KCN


正确答案
解析
略
知识点
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,他在潮湿的环境中会发生下列反应:3NF3+5H2O→2NO+HNO3+9HF,有关该反应说法正确的是
正确答案
解析
略
知识点
向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu (NO3)2。在所得溶液中加入l.0 mol/L的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2 g。下列有关说法错误的是
正确答案
解析
略
知识点
扫码查看完整答案与解析