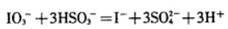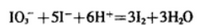- 氧化还原反应的计算
- 共67题
28.碳和氮的化合物与人类生产、生活密切相关。
(1)在一恒温、恒容密闭容器中发生反应: Ni(s)+4CO(g)

A.增加Ni的量可提高CO的转化率,Ni的转化率降低
B.缩小容器容积,平衡右移,减小
C.反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低
D.当4vNi(CO)4=v(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态
(2)CO与镍反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫。
已知:C(s)+O2(g)==CO(g) H= -Q1 kJ·mol-1
C(s)+ O2(g)==CO2(g) H= -Q2 kJ·mol-1
S(s)+O2(g)==SO2(g) H= -Q3 KJ·mol-1
则SO2(g)+2CO(g)==S(s)+2CO2(g) H= kJ·mol-1 。
(3)金属氧化物可被一氧化碳还原生成金属单质和二氧化碳。图(1)是四种金属氧化物(Cr2O3、SnO2、PbO2、Cu2O)被一氧化碳还原时与温度(t)的关系曲线图。
700oC时,其中最难被还原的金属氧化物是 (填化学式),用一氧化碳还原该金属氧化物时,若反应方程式系数为最简整数比,该反应的平衡常数(K)数值等于 。
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如上图(2)所示。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为 。
若该燃料电池使用一段时间后,共收集到20mol Y,则理论上需要消耗标准状况下氧气的体积为 L。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.现有44g Mg、Al、Zn、Fe多种活泼金属粉末的混合物与体积为1L,质量分数为20%的硫酸溶液恰好完全反应,得到无水盐140g,则下列说法正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.做实验时不小心粘在皮肤上的高锰酸钾会形成黑斑,很久才能消除,若用乙二酸的稀溶液擦洗黑斑,黑斑可以迅速褪去,其离子反应方程式为:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9. 在浓盐酸中

下列关于该反应的说法中,错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
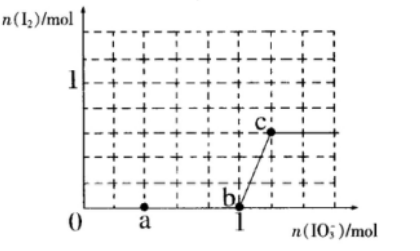
28.已知溶液中,还原性: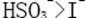
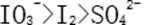
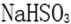
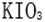
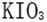
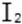
(1)a点处的氧化产物是( )(用离子符号填写,下同),还原产物是( ),a点对应的离子方程式为( )。
(2)当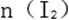
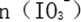
(3)当溶液中的I-为0.4mol时,加入的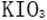
(4)若往100mL 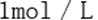
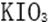
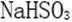
正确答案
(1)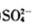
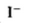
(2)1.2;
(3)1.12或0.4
(4)
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析