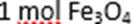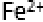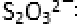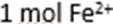- 氧化还原反应的计算
- 共67题
13.MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:(1)软锰矿、闪锌矿与硫酸共热:

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.节能减排是当今社会的热门话题,研发混合动力汽车对于中国汽车业的未来具有重要的战略意义。混合动力汽车持续工作时间长,动力性好的优点,无污染、低噪声的好处,汽车的热效率可提高10%以上,废气排放可改善30%以上,某种混合动力汽车的动力系统由“1.6L汽油机十自动变速器十20kW十200V镍氢电池”组成。
①混合动力汽车所用的燃料之一是乙醇,lg乙醇完全燃烧生成CO2气体和液态H2O放出30.0kJ热量,写出乙醇燃烧的燃烧热的热化学方程式( )。

③常温下,同浓度的Na2CO3溶液和NaHCO3溶液的pH都大于7,两者中哪种的pH更大,其原因是 ( )。0.1mol·L-1 Na2CO3中阴高子浓度大小关系是( ),向0.1mol·L-1 Na2CO3溶液中滴入少量氢氧化钡溶液,则发生反应的离子方程式为:( )。
(2)二氧化锰、锌是制备干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)
联合生产二氧化锰、锌的工艺如下:
①操作Ⅰ需要的玻璃仪器是( ) 。
②软锰矿(含MnO2)和闪锌矿与硫酸反应的化学方程式为( ),上述电解过程中,当阴极生成6.5g B时阳极生成的MnO2的质量为( ) 。
③利用铝热反应原理,可以从软锰矿中提取锰,发生的化学方程式为( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.将1.92g铜粉投入到一定量的浓硝酸中反应,当铜完全作用时,生成的气体颜色越来越浅,共672ml(标况下),将盛有此气体的容器倒扣在水槽中,通入标准状况下的一定体积的氧气,恰好溶于水,则所通入氧气的体积为( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13. 用惰性电极电解某金属元素R的硝酸盐R(NO3)n溶液,通电一段时间后,阳极产生气体V L(标准状况)时,阴极质量增加m g,若R的相对原子质量为M,设NA 为阿伏加德罗常数的值,下列叙述中不正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.将19.2g的铜屑投入到400mL浓度均为

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.水热法制备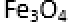
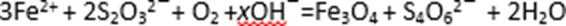
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
33.化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。写出制取Cl2的离子方程式( );某小组要从该混合物中回收MnO2并提取MnCl2晶体,则要多次用到的玻璃仪器是( )。
(2)下图A~G都是常见的与气体制备、收集、尾气吸收有关的装置。例如,B、C都可以收集H2、CH4、NH3、Cl2等。如果收集Cl2并进行尾气处理,不能选用 ( );如用B收集Cl2,应该从( )(甲、乙)端进气。
(3)工业常用Cl2从海水中制备Br2,反应离子方程式是( ) 。实验室模拟该实验,分离出Br2的操作是:取混合溶液于分液漏斗中,加入CCl4,振荡 ,静置分层,( ) 。
(4)次氯酸盐有强氧化性,如NaClO 可以氧化NH3制备高能燃料N2H4,反应方程式是:(
)。现有14.9g NaClO 最多可以制备( )mol N2H4。





正确答案
(1)
(2)DF ; 乙
(3)
(4)
解析
解析已在路上飞奔,马上就到!
知识点
13.用石墨作电极电解0.1mol/L的CuSO4溶液,当有0.4mol电子通过电路时,阴极增重6.4g,
则要使电解后的溶液恢复到原始状态,则应向电解后的溶液中加入( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.新型纳米材料MFe2Ox (3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。
常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下:
则下列判断正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析