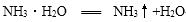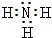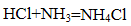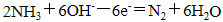- 电极反应和电池反应方程式
- 共352题
用A.b两个惰性电极电解0.2L一定浓度的硫酸铜溶液,当a极上产生4.48L(标况)气体时,b极上只有固体析出。然后将电源反接,当b极产生4.48L(标况)气体时,溶液质量共减少45.4克。下列说法正确的是( )
正确答案
解析
略
知识点
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
正确答案
解析
略
知识点
能源的开发和利用是当前科学研究的重要课题。
(1)利用二氧化铈(CeO2)在太阳能作用下可实现如下变废为宝的过程:
上述过程的总反应是_________,该反应将太阳能转化为_________。
(2)CO、O2和KOH溶液构成的燃料电池的负极电极反应式为_________。该电池反应可获得





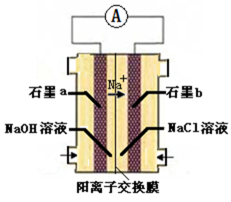
(3)氯碱工业是高耗能产业,下列将电解池与燃料电池相组合的工艺可以节能30%以上。
①电解过程中发生反应的离子方程式是_________,阴极附近溶液pH_________(填“不变”、“升高”或“下降”)。
②如果粗盐中

a.Ba(OH)2
b.Ba(NO3)2
c.BaCl2
现代工艺中更多使用
③图中氢氧化钠溶液的质量分数a%_________b%(填“>”、“=”或“<”),燃料电池中负极上发生的电极反应为_________。
正确答案
(1)H2O + CO2 =H2 + CO + O2;化学能
(2)CO – 2e- +4OH- = CO32- + 2H2O;×10-4 mol·L-1
(3)①2Cl-+2H2O 
解析
略。
知识点
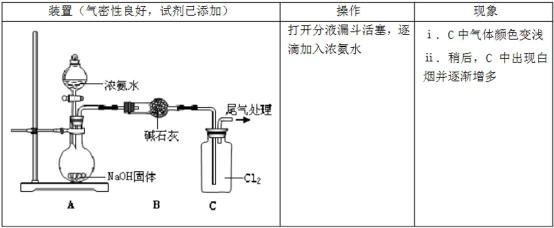
某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
(1)A中反应的化学方程式是 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) H= —456 kJ·mol-1
已知:
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,NH3中的H-N键比HCl中的H-Cl键(填“强”或“弱”) 。
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
若该装置能实现设计目标,则
② 石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
正确答案
见解析。
解析
(1)
(2)①
②40 弱
(3)
(4)①还原
②
知识点
储氢合金表面镀铜过程发生反应
正确答案
解析
略。
知识点
扫码查看完整答案与解析