- 分液和萃取
- 共25题
12.下列各组混合物,使用氢氧化钠溶液和盐酸两种试剂不能分离的是
正确答案
解析
试题分析:A.MgO是碱性氧化物与NaOH不能反应,而Al2O3是两性氧化物,可以与NaOH发生反应产生NaAlO2,过滤后洗涤,就得到纯净的MgO,错误;B.向溶液中加入过量的NaOH溶液,氯化铁变为Fe(OH)3沉淀,氯化铝变为NaAlO2,过滤,然后向溶液中加入适量的盐酸,当沉淀达到最大值中,过滤,得到Al(OH)3,再分别向两种物质的沉淀中加入适量的盐酸溶解,就得到氯化铝溶液,除去了杂质,错误;C.二氧化硅是酸性氧化物,可以与NaOH发生反应,而氧化铁与NaOH不能发生反应。加入过量的NaOH,然后过滤洗涤,就得到纯净的氧化铁,错误;D.二者都可以与NaOH发生反应,当再向得到的沉淀中加入盐酸时,二者都溶解,不能分离、提纯二者,正确。
考查方向
解题思路
氧化铝是两性氧化物,既溶于氢氧化钠溶液又溶于盐酸。
易错点
没有熟练掌握了各物质的性质,特别是“与众不同的个性”。
知识点
桥梁基础钻孔灌注桩的清孔方法,应根据设计要求、( )、机具设备和土质条件决定。
A.钻孔方法
B.钻孔原则
C.钻孔深度
D.钻孔直径
正确答案
A
解析
暂无解析
下图是某同学研究铜与浓硫酸的反应装置:
完成下列填空:
35.写出A中发生反应的化学方程式 。
采用可抽动铜丝进行实验的优点是 。
36.反应一段时间后,可观察到B试
37.从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是 、
。(要求填一种化合物和一种单质的化学式)
38.反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是 。该黑色不溶物不可能是CuO,理由是 。
39.对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:

正确答案

解析
浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓)
考查方向
浓硫酸的性质
解题思路
浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,据此写出反应的化学方程式,抽动铜丝可以控制铜丝与浓硫酸接触面积
易错点
抽动铜丝的优点
教师点评
本题考查浓硫酸的性质,明确物质的性质是解题关键,题目难度不大
正确答案
变红
解析
反应生成二氧化硫,二氧化硫为酸性氧化物,能够与水反应生成亚硫酸,溶液显酸性,遇到石蕊显红色
考查方向
SO2的性质
解题思路
依据二氧化硫酸性氧化物的性质解答
易错点
SO2为酸性氧化物
教师点评
本题考查SO2的性质,明确物质的性质是解题关键,题目难度不大
正确答案
NH3 Cl2
解析
向BaCl2溶液中通入另一种气体,产生白色沉淀,是因为二氧化硫不与氯化钡溶液反应,通入的气体需要满足把二氧化硫转化为盐或把二氧化硫氧化为硫酸,如碱性气体NH3、做氧化剂的气体如Cl2、O2、O3、NO2、Cl2O等
考查方向
SO2的性质
解题思路
二氧化硫不与氯化钡溶液反应,通入的气体需要满足把二氧化硫转化为盐或把二氧化硫氧化为硫酸
易错点
将二氧化硫转化为盐的气体
教师点评
本题考查SO2的性质,明确物质的性质是解题关键,题目难度较大
正确答案
过滤(1分) CuO会溶于稀硫酸中(2分)
解析
将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离固体与液体可以采用过滤法;氧化铜与酸反应生成铜离子与水,所以黑色固体不可能为氧化铜
考查方向
物质的分离、CuO的性质
解题思路
分离固体与液体用过滤,氧化铜与酸反应生成铜离子与水,据此解答
易错点
CuO的性质应用
教师点评
本题考查物质的分离、CuO的性质,题目难度不大
正确答案
(1)硫(1分) (2)Cu2S(2分)
解析
黑色固体通入氧气反应生成气体能够使品红褪色,说明生成二氧化硫,含有硫元素;
若该黑色不溶物由两种元素组成且在反应前后质量保持不变,可知除了含有硫元素外还含有铜,物质为硫化亚铜,化学式:Cu2S
考查方向
物质成分的确定
解题思路
黑色固体通入氧气反应生成气体能够使品红褪色,说明生成二氧化硫,含有硫元素;
若该黑色不溶物由两种元素组成且在反应前后质量保持不变,可知除了含有硫元素外还含有铜,物质为硫化亚铜
易错点
反应前后质量保持不变条件的应用
教师点评
本题考查物质成分的确定,注意推理的严密性,题目难度中等
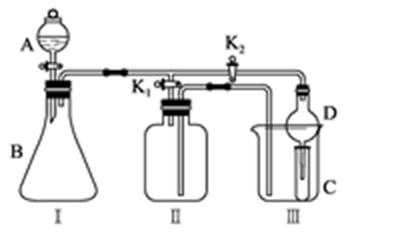
某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质。
打开K1关闭K2,可制取某些气体。打开K2关闭K1,能比较一些物质的性质。
34.甲同学认为装置Ⅰ可用于制取H2、NH3、O2,但装置Ⅱ 只能收集H2、NH3,不能收集O2。其理由是__________。乙同学认为在不改动装置Ⅱ仪器的前提下,对装置Ⅱ进行适当改进,也可收集O2。你认为他的改进方法是______________________。
35.丙同学设计实验比较氧化性:KClO3>Cl2>Br2。在A中加浓盐酸后一段时间,观察
到C中的现象是_____________________;仪器D在该装置中的作用是______________。
在B装置中发生反应的离子方程式为_______________________________________。
丁同学用石灰石、醋酸、苯酚钠等药品设计了另一实验。他的实验目的是 。
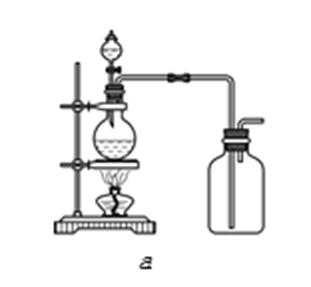
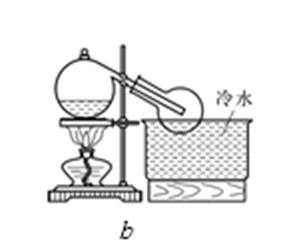
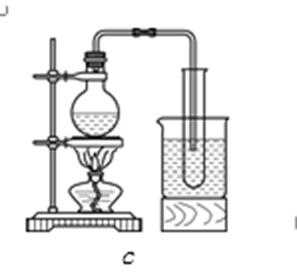
实验室常用浓H2SO4与硝酸钠反应制取HNO3
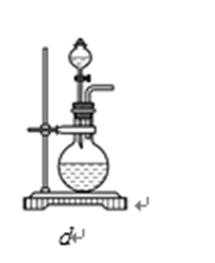
36.下列装置中最适合制取HNO3的是 。
37.实验室里贮存浓硝酸的方法是 。
正确答案
氧气的密度比空气大 (1分) 将装置Ⅱ中装满水(1分)
解析
甲同学:Ⅱ装置中进气管短,出气管长,为向下排空气法,O2的密度大于空气的密度,则氧气应采用向上排空气法收集,乙同学:O2 不能与水发生反应,而且难溶于水,所以能采用排水法收集;所以改进方法是将装置Ⅱ中装满水
考查方向
气体的收集方法
解题思路
氧气密度比空气大,用排空气法收集,需用向上排空气法收集,Ⅱ装置中进气管短,出气管长,为向下排空气法;用排水法可以收集O2等气体
易错点
装置改进
教师点评
本题考查气体的收集方法,题目难度中等,注意把握气体的性质及密度选择相应的收集方法
正确答案
溶液呈橙色(1分) 防止倒吸(1分)ClO3-+6H++5Cl-→3Cl2↑+3H2O (2分)
比较醋酸、碳酸和苯酚的酸性强弱(实证酸性:CH3COOH>H2CO3>C6H5OH,2分)
解析
根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,如要设计实验证明氧化性KClO3>Cl2>Br2,装置Ⅰ、Ⅲ验证物质的性质(K2打开,K1关闭),则I中发生KClO3和浓盐酸的氧化还原反应,Ⅲ中发生氯气与NaBr的氧化还原反应,由氧化性为氧化剂>氧化产物,则A中为浓盐酸,B中为KClO3固体,C中为NaBr溶液,观察到C中的现象为溶液呈橙色,仪器D为干燥管,有缓冲作用,所以能防止倒吸,在B装置中氯酸根离子和氯离子在酸性条件下发生价态归中反应生成氯气,反应为:ClO3-+6H++5Cl-=3Cl2↑+3H2O,石灰石和醋酸反应生成二氧化碳,二氧化碳和苯酚钠反应生成硅酸沉淀,所以B中固体溶解,产生无色气体,C试管中产生白色沉淀,实验的目的是比较碳酸、醋酸、苯酚的酸性强弱(实证酸性:CH3COOH>H2CO3>C6H5OH)
考查方向
性质实验方案设计
解题思路
装置Ⅰ、Ⅲ验证物质的性质(K2打开,K1关闭).根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,如要设计实验证明氧化性KClO3>Cl2>Br2,则I中发生KClO3和浓盐酸的氧化还原反应,Ⅲ中发生氯气与NaBr的氧化还原反应,有缓冲作用的装置能防止倒吸,在B装置中+5价的氯离子和-1价的氯离子在酸性条件下发生氧化还原反应生成氯气,根据强酸制弱酸,石灰石和醋酸反应生成二氧化碳,二氧化碳和苯酚钠反应生成苯酚,据此分析实验目的
易错点
装置的作用
教师点评
本题考查性质实验方案设计,侧重于考查学生对实验原理的把握和对仪器的使用,题目难度中等
正确答案
b
解析
硝酸的制取原理是:固体和液体微热制取,故d错误,该反应符合难挥发性的酸来制取挥发性的酸,硝酸易挥发,不能用排空气法收集,故a、c错误;所以硝酸的挥发性注定了选择的收集方法是b装置所示
考查方向
气体的制取
解题思路
根据化学反应原理,硝酸的制取原理是:固体和液体微热制取,难挥发性的酸来制取挥发性的酸,据此选择装置
易错点
硝酸的制取原理
教师点评
本题考查HNO3的制取,侧重于考查学生对实验原理的把握和对仪器的使用,题目难度中等
正确答案
盛装在带玻璃塞的棕色细口玻璃瓶中,放置在阴凉处(阴暗低温的地方)
解析
纯净的硝酸或浓硝酸在常温下见光或受热就会分解生成二氧化氮、氧气、水,保存时需要低温且使用棕色的试剂瓶
考查方向
物质的贮存
解题思路
根据硝酸的性质选择合适的贮存方法,硝酸见光分解,保存是不能见光,常温下即可分解,需要低温保存
易错点
HNO3的性质
教师点评
本题考查物质的贮存方法,题目难度不大
幕墙的性能设计应根据建筑物的类别、高度、体形以及建筑物所在地的地理、气候、环境等条件由()确定。
A.建设单位
B.施工单位
C.监理单位
D.设计单位
正确答案
D
解析
暂无解析
扫码查看完整答案与解析