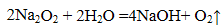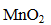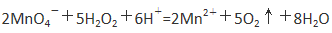- 化学实验方案的设计与评价
- 共98题
某同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
Ⅰ. 将光亮铜丝插入浓硫酸,加热;
Ⅱ. 待产生大量黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ. 冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用。
(1)步骤Ⅱ产生的气体是______。
(2)步骤Ⅲ中,“从反应后的混合物中分离出黑色沉淀”的操作是______。
(3)该同学假设黑色沉淀是CuO。检验过程如下:
查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6] 溶液,若产生红褐色沉淀,证明有Cu2+。
① 将CuO放入稀硫酸中,一段时间后,未见明显现象,再滴加K4[Fe(CN)6] 溶液,产生红褐色沉淀。
② 将黑色沉淀放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6] 溶液,未见红褐色沉淀。
由该检验过程所得结论是 。
(4)再次假设,黑色沉淀是铜的硫化物。实验如下:
① 现象2说明黑色沉淀具有______性。
② 产生红棕色气体的化学方程式是______。
③ 能确认黑色沉淀中含有S元素的现象是 ,相应的离子方程式是 。
④ 为确认黑色沉淀是“铜的硫化物”,还需进行的实验是_____。
(5)以上实验说明,黑色沉淀中存在铜的硫化物。进一步实验后证明黑色沉淀是CuS与Cu2S的混合物。将黑色沉淀放入浓硫酸中加热一段时间后,沉淀溶解,其中CuS溶解的化学方程式是______。
正确答案
见解析。
解析
(1)SO2
(2)将反应后的混合物倒入装有冷水的烧杯中,冷却后过滤
(3)黑色沉淀中不含有CuO
(4)① 还原性
② 2NO +O2==2NO2
③ B试管中出现白色沉淀
NO2 + SO2 + Ba2+ + H2O == BaSO4↓+ NO↑+ 2H+
④ 取冷却后A装置试管中的溶液,滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+,说明黑色沉淀是铜的硫化物
(5)
知识点
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:小水制作
方案I:取25.00 mL上述溶液,加入过量的盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1 g 。
方案Ⅱ:取25.00 mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2 g 。
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、胶头滴管、药匙和__________________、_________________。
(2)写出Na2SO3固体氧化变质的化学方程式__________________________________。
(3)方案I加入过量的盐酸酸化的BaCl2溶液,目的是_____________________________,在过滤前,需要检验是否沉淀完全,其操作是___________________________。
(4)方案I中,若滤液浑浊,将导致测定结果____________(选填“偏高”或“偏低”)。
(5)若操作正确,则m1_____ m2(选填“>”、“<”或“=”),原因是________________。
(6)取25.00 mL上述溶液,用滴定的方法测定Na2SO3的纯度。下列试剂可作为标准溶液进行滴定的是________。
a.酸性KMnO4溶液 b.H2O2溶液 c.Br2水 d.FeCl3溶液
Na2SO3固体的纯度可表示为: _____________(注明你的表达式中所用的有关符号的含义和单位)。
正确答案
(1)电子天平;250 mL的容量瓶
(2)2Na2SO3+ O2→ 2Na2SO4。
(3)使SO32-充分转化为气体,使SO42-完全沉淀,静置,在上层清液中再滴入氯化钡溶液,观察是否继续有沉淀生成。
(4) 偏高
(5)<,方案II中盐酸提供H+,Ba(NO3)2提供NO3- 形成稀HNO3,将一部分SO32-氧化成SO42-,导致BaSO4质量增大。
(6)a,
解析
略
知识点
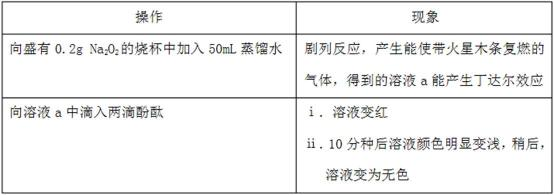
某小组通过实验研究Na2O2与水的反应。
(1)Na2O2与水反应的化学方程式是 。
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应。
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂 (填化学式),有气体产生。
Ⅱ.乙同学查阅资料获悉:用KMnO4 (被还原为Mn2+)可以测定H2O2的含量。
取3 mL溶液a稀释至15mL,用稀H2SO4酸化,再逐滴加入0.0045 mol·L-1 KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗10 mL KMnO4溶液。
①KMnO4与H2O2反应的离子方程式是 。
②溶液a中c(H2O2)= mol·L-1。
③溶液褪色速率开始较慢后变快的原因可能是 。
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅰ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1mol·L-1 NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色,该过程无明显热效应。
Ⅱ.向0.1mol·L-1 NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入氧气,溶液颜色无明显变化。
② 从实验Ⅰ和Ⅱ中,可得出的结论是 。
②同学们进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应。实验方案是:取少量溶液a于试管中, 。
正确答案
见解析。
解析
(1)
(2)Ⅰ.
Ⅱ.①
②0.0375
③反应生成的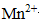
(3)①碱性条件下,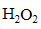
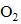
②加入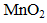
知识点
为测定碳酸氢钠纯度(含少量氯化钠),某学生拟用如图实验装置,以下实验设计正确的是
正确答案
解析
略
知识点
10.一溴乙烷在制药,杀虫剂,汽油抗震液中铅的消除剂中有着广泛的应用。工业上和实验室中都可用如下过程制备一溴乙烷。
某同学在实验室中模拟整个生产过程,查阅资料如下:
生产原理:NaBr+H2SO4=HBr↑+NaHSO4
正确答案
解析
(1)使反应平稳进行,防止乙醇、HBr大量挥发,充分蒸出一溴乙烷。
(2)SO42-,取少量水层1的溶液于试管中,加入足量稀盐酸化,再滴加少量的BaCl2溶液。
(3)
(4)67%
知识点
为探究SO2与可溶性钡盐能否反应生成白色BaSO3沉淀,甲、乙两同学用下图所示装置进行实验(夹持装置、加热装置已略,气密性已检验)
实验操作和现象:
(1) A中反应的化学方程式是 ________________ 。
(2) C中可溶性钡盐溶液X为___________ 。实验过程中,发现液体Y不能很顺利地滴下,则可如何改进: ______________- 。
(3)分析B中不溶于稀盐酸的沉淀的产生原因,甲同学认为是 __________ ,乙同学认为是白雾参与反应。
为证实各自的观点,在原实验基础上;甲同学在原有操作之前,先通N2一段时间。乙同学则在A、B间增加盛有饱和NaHSO3溶液的洗气瓶D。
甲、乙各自进行实验,B中现象分别如右表:由此得出的结论是 __________ 。
(4) 丙将甲乙两同学的方案进行联合试验,发现B中无沉淀生成,而C中产生白色沉淀,但无红棕色气体。C中反应的化学方程式是______________ 。
(5)丁同学认为丙选择的两种钡盐比较相似,于是丁在丙的基础上将B、C中的钡盐分别换成过量新制的醋酸钡溶液、Ba(AlO2)2溶液,发现B、C中均立即产生大量白色沉淀,该沉淀可溶于稀盐酸,并产生能使澄清石灰水浑浊的气体。C中沉淀为________。实验室里欲获得该沉淀,所需要的玻璃仪器是 ____________- 。
(6) 结合实验目的,根据四位同学的实验操作和实验现象,你得出的结论是_______________。
正确答案
(1)
(2)硝酸钡
将分液漏斗改为恒压漏斗(其他合理说法也给分)
(3)空气参与了反应;
空气、白雾均是产生白色沉淀的原因,其中白雾是主要原因。
(4)3SO2+ 2H2O+ 3Ba(NO3)2 + →3BaSO4↓+2NO↑+ 4H NO3
(5)BaSO3、氢氧化铝; 烧杯、漏斗、玻璃棒;
(6)SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀,SO2与可溶性钡的弱酸盐能反应生成BaSO3沉淀。
解析
略
知识点
28.已知:①Br2与Cl2一样能氧化氨气。
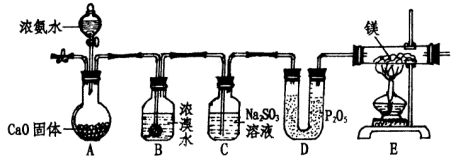
②镁条能在N2中燃烧生成黄绿色固体,遇水剧烈反应生成两种碱。
`某化学学习小组设计下列装置来制取氨气并完成相关实验。
(1)实验步骤:
①点燃E处酒精灯;
②打开A中分液漏斗活塞;
③连接装置,检查装置气密性;
④通入惰性气体,排出装置内空气;
⑤装入各仪器药品。
其操作顺序是( )。(填序号)
(2)A处固体CaO的作用是( );
(3)写出B处反应方程式 ( );
(4)C处亚硫酸钠的作用是:( )(用文字及相关离子方程式叙述);
(5)能说明反应过程有N2生成的现象是( );
(6)此装置不足之处是 ( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.已知:①


②镁条能在N2中燃烧生成黄绿色固体,该固体遇水剧烈反应生成两种碱。
某化学学习小组设计下列装置来制取氨气并完成相关实验。
(1)实验步骤:
①点燃E处酒精灯;
②打开A中分液漏斗活塞;
③连接装置,检查装置气密性;
④通入惰性气体,排出装置内空气;
⑤将药品装入各仪器装置内。
其正确的操作顺序是( )(填序号)。
(2)A处固体CaO的作用是 ( ) 。
(3)分别写出B处、E处反应的化学方程式( ), ( )。
(4)C处亚硫酸钠溶液的作用是:( )(用文字及相关离子方程式叙述);
(5)能说明反应过程中有N2生成的现象是( ) 。
(6)此装置不足之处是( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.Ⅰ、下面a~e是中学化学实验中常见的几种定量仪器:
a、量筒 b、容量瓶 c、滴定管 d、托平天平 e、温度计
(1)上述仪器中标有0刻度的玻璃仪器是( )(填序号)。
(2)若用上述仪器测定中和热,则缺少的玻璃仪器为烧杯、( ) 。
Ⅱ、某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
请按要求填空:
(1)利用B装置可制取的气体有( )(写出两种即可)。
(2)A、B、E相连后的装置可用于制取Cl2并进行相关的性质实验。
若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行如下①、②两个实验,实验操作、现象、结论如下:
请你评价实验①、②的结论是否合理?( );若不合理,请说明理由:( ) 。
(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(铜片放在有孔塑料板上),制得NO2后,进行以下实验。
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹( ),再打开止水夹( ),使烧杯中的水进入试管丁的操作是( )。
②试管丁中的NO2与水充分反应后,若向试管内缓缓通人一定量的O2,直至试管全部充满溶液,则原NO2与通人O2的物质的量之比为( )。
③尾气吸收的装置是( )(填序号)。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.下列实验方案能达到预期目的的是( )
①实验室保存FeCl3溶液应加少量稀盐酸,并且放入少量的Fe粉
②氢氧化钠溶液保存在配有橡胶塞的细口瓶中
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤工业上可用金属铝与V2O5在高温下冶炼V(钒),铝作还原剂
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析