- 根据化合价正确书写化学式(分子式)
- 共24题
16.将足量SO2通入下列各溶液中,所含离子还能大量共存的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9. 下列有关说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
17.在K2CO3样品中含Na2CO3、KNO3、Ba(NO3) 2中的一或两种杂质。将13.8 g该样品溶于足量水中得到澄清溶液,再加入过量CaCl2溶液,可得9.0 g沉淀,则原样品中( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
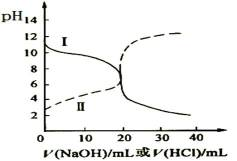
9.25oC时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
4.捕碳技术是指从空气中捕获CO2的技术。目前NH3已经被用作工业捕碳剂。下列物质中不能作为捕碳剂的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.减少污染、保护环境是全世界最热门的课题。
(1)为了减少空气中SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)==H2O(g) ΔH1=-241.8 kJ·mol-1
C(s)+1/2O2(g)===CO(g) ΔH2=-110.5 kJ·mol-1
则焦炭与水蒸气反应生成CO的热化学方程式为____________________。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是__________(填序号):
a.Ca(OH)2 b.CaCl2
c.Na2CO3 d.NaHSO3
(2)CO在催化剂作用下可以与H2反应生成甲醇:CO(g)+2H2(g) 
在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如图所示。
①M、N两点平衡状态下,容器中总物质的物质的量之比为:n(M)总:n(N)总=_____________。
②若M、N、Q三点的平衡常数KM、KN、KQ的大小关系为___________。
(3)催化硝化法和电化学降解法可用于治理水中硝酸盐的污染。
①催化硝化法中,用H2将NO还原为N2,一段时间后,溶液的碱性明显增强。则该反应离子方程式为__________。
②电化学降解NO的原理如图所示,电源正极为________(填“a”或“b”);若总反应为4NO3-+4H+====5O2↑+2N2↑+2H2O,则阴极反应式为_______________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.下列叙述不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列有关化学用语,正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
19.某溶液含有NO3-、CH3COO-、A1O2-、S2-,若向其中加入过量的盐酸,充分搅拌,再加入过量的 NaOH溶液,溶液中大量减少的离子是( )
正确答案
解析
每小题有一个或两个正确选项,只有一个正确选项的,多选不给分;有两个正确选项的,选对一个给2分,选错一个该小题不给分。
知识点
24.从2014年4月15日零点开始,上海市空气质量实时发布系统将以实时空气质量指数替代原来的AQI指数。燃煤烟气和汽车尾气是引发AQI指数上升的主要污染源。因此,对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的。
汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g) 
(1)该热化学反应方程式的意义是____________________________。
一定条件下用气体传感器测得该反应在不同时间的NO和CO浓度如下表:
(2)前2s内的平均反应速率υ(N2)_________(保留两位小数);CO的平衡转化率为_________。
(3)下列描述中能说明上述反应已达平衡的是________________。
a.2υ正(NO)=υ逆(N2)
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中CO的转化率不再发生变化
(4)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,并获得铵盐。
其中脱硫的总反应式:SO2+O3+2NH3+H2O → (NH4)2SO4+O2;
在(NH4)2SO4溶液中存在水解反应,常温下该水解反应的平衡常数表达式可表示为K=_________;
有三种铵盐溶液:①NH4Cl ②(NH4)2SO4 ③NH4HSO4 ,若它们的物质的量浓度相等,c(NH)由大到小的顺序是____________________(填序号,下同);若它们的pH值相等,c(NH)由大到小的顺序是____________________。
正确答案
(1)2mol NO气体和2mol CO气体完全反应生成1mol N2和2 mol CO2气体放热Q kJ
(2)1.88×10-4 mol/(L·s) ; 25%
(3)bd
(4)
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析