- 化学平衡常数的含义
- 共77题
据报道,在一定条件下,由CO2和H2合成乙醇已成为现实,该合成对解决能源问题具有重大意义。
(1)CO2和H2合成乙醇的化学方程式为:
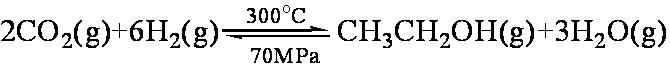
如果只是压强增大,则该反应的化学平衡常数K将 (填:“增大”、“减小”或“不变”);
②从上图可知,该平衡正向的ΔH 0(填“>”、“<”或“=”)。
(2)对于该化学平衡,为了提高H2的转化率,可采取的措施有 。
A.加压
B.升温
C.加催化剂
D.增加CO2的浓度
(3)已知25oC、101 kPa条件下,1 g乙醇燃烧生成CO2和液态水时释放出a kJ热量,请写出该条件下乙醇燃烧热的热化学反应方程式: 。
(4)现有甲装置为原电池(a电极通氧气,b电极通乙醇),乙装置为电解池:
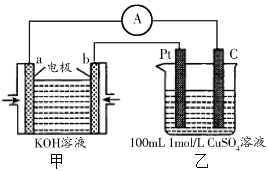
② 若甲中有0.01mol CH3CH2OH参加反应,则乙装置中生成的气体在标准状况下的体积共为 L 。
正确答案
见解析。
解析
(1)① 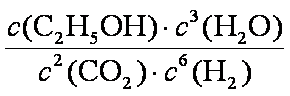
(2)A、D ;
(3)C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH=-46a kJ/mol ;
(4)①C2H5OH-12e-+16OH-=2CO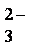
②0.672 。
知识点
降低太气中

(1)将燃煤废气中的

①某温度下,将2。0mol
则











②一定条件下,上述反应在密闭容器中达平衡。当仅改变影响反应的一个条件,引起的下列变化能说明平衡一定向正反应方向移动的是________。
a. 反应物的浓度降低
b. 容器内压强增大
c. 正反应速率大于逆反应速率
d. 化学平衡常数K增大
(2)碳酸氢钾溶液加水稀释,

a.
b.
c. 降低温度,
正确答案
(1) ①>;<;57.14%;② cd
(2)增大;b
(3)2Fe3+ +3CO32-+3H2O=2Fe(OH)3(胶体)+3CO2↑
解析
略。
知识点
大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+ O3(g)= IO-(aq)+O2(g)△H1
②IO-(aq)+H+(aq) 
③HOI(aq) + I-(aq) + H+(aq) 
总反应的化学方程式为________,其反应△H=________。
(2)在溶液中存在化学平衡:I2(aq) + I-(aq) 
(3) 为探究Fe2+ 对O3氧化I-反应的影响(反应体如图13),某研究小组测定两组实验中I3-浓度和体系pH,结果见图14和下表。
①第1组实验中,导致反应后pH升高的原因是________。
②图13中的A为__ ___,由Fe3+生成A的过程能显著提高Ⅰ-的转化率,原因是________。
③第2组实验进行18s后,I3-浓度下降。导致下降的直接原因有(双选)________。
A. c(H+)减小
B. c(I-)减小
C. I2(g)不断生成
D. c(Fe3+)增加
(4)据图14,计算3-18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字)。
正确答案
(1) O3+2Ⅰ—+2H+=Ⅰ2+ O2+ H2O,△H=△H1+△H2+△H3。
(2)
(3)反应过程中消耗氢离子,溶液酸性减弱,pH增大,水电离出氢离子参与反应破坏水的电离平衡,氢氧根浓度增大,溶液呈碱性,pH增大;Fe3+,该过程是非氧化还原;BD
(4)(计算过程略)5.5×10—4 mol/L·s
解析
略。
知识点
运用化学反应原理研究氮、氯等单质及其化合物的反应有重要意义。
(1)科学家研究在一定条件下通过下列反应制备NH3:
①在其他条件相同时,反应中NH3的体积分数(a)在不同温度下随反应时间(t)的变化如图。该反应的平衡常数表达式K=________,该反应中的ΔH________0(填“>”“<”或“=”)。
②某温度下,在2L容积不变的密闭容器中加入1molN2和6molH2O(l)发生反应,转化率随时间(f)变化如图。15-20min内,v(NH3)=________。若其他
(2) 25℃时,某同学将O.lmol


(3) 25℃时,向O.lmol




正确答案
(1)①
(2)>;>
(3)白色沉淀逐渐变成红褐色;Mg2++2NH3·H2O=Mg(OH)2↓+2NH4+;2Fe3+(aq)+3Mg(OH)2(s)=2Fe(OH)3(s)+3Mg2+(aq)
解析
略。
知识点
火力发电厂释放出大量气体会造成环境污染。对燃煤废气进行处理,可实现绿色环保、废物利用等目的。
(1)CO可以与H2O(g)发生反应:CO(g) + H2O(g) 
在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0。
①该反应的平衡常数表达式为 。
②平衡时,丙容器中H2O的物质的量是 mol,甲容器中CO的转化率是 ,
容器中CO的转化率:乙 甲(填“>”、“=”或“<”)。
③丙容器中,其他条件不变时,温度 (填“升高”或“降低”),CO的平衡转化率升高。
(2)除去氮氧化物:
① 利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为__________
② 也可用氨气与之发生反应:NOx+NH3→N2+H2O。
现有NO2和NO的混合气体3.0 L,跟3.4 L(同温同压下)NH3反应,恰好使其全部转化为氮气,则原混合气体中,NO2与NO的体积比是__________。
正确答案
见解析。
解析
(1)①
②0.1 50% >
③ 降低
(2)①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol (3分)
② 7 : 3
知识点
扫码查看完整答案与解析