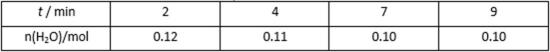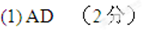- 化学平衡常数的含义
- 共77题
28.工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) 
(1)不同温度下的平衡转化率与压强的关系如图所示。
① 该反应ΔH________(填“>”或“<”,下同)0,ΔS________0,则该反应________(填“一定能”“一定不能”或“不一定”)自发进行。
② 实际生产条件控制在250℃、1.3×l04kPa左右,选择此压强的理由是( )。
(2)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.1mol/L。
① 该反应的平衡常数K=( )。
② 在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是( )(填字母)。
a. 氢气的浓度减少
b. 正反应速率加快,逆反应速率也加快
c. 甲醇的物质的量增加
d. 重新平衡时,n(H2)/n(CH3OH)增大
③ 若保持同一反应温度将起始物质改为amol CO、bmol H2、cmol CH3OH,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为____________________,且欲使开始时该反应向逆反应方向进行,c的取值范围是( )。
正确答案
(1)①<<不一定②该压强下,CO转化率已较高(90%左右),再增大压强,CO转化率提高不大,且生产成本增加
(2)① 6.25 ② bc ③ a+c=2和b+2c=6或b=2+2a1.8<c≤2
解析
解析已在路上飞奔,马上就到!
知识点
31. Ⅰ.已知:4Al(s)+3O2(g) = 2Al2O3(s) △H=-2834.9KJ•mol-1
写出铝与氧化铁发生铝热反应的热化学方程式( ) 。
Ⅱ.在2L密闭容器内,800℃时反应:
(1) 写出该反应的平衡常数表达式:K= ( ); 用

(2)下列研究目的和示意图相符的是( )。
III.科学家制造出一种使用固体电解质的高效燃料电池。一个电极通入空气,另一个电极通入燃料蒸汽。其中固体电解质是掺杂了


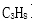
(1)电池的负极反应式为( );
(2)放电时固体电解质里的
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
下列说法不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26. 碳及其化合物有广泛的用途。
(1)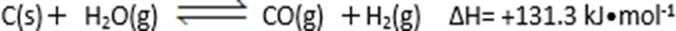
A.升高温度 B.增加碳的用量 C.加入催化剂 D.用CO吸收剂除去CO
(2)又知,
则
(3)CO与H2在一定条件下可反应生成甲醇,甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为( ) 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:



正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.(I)某氮肥厂氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。在微生物作用下,NH4+经过两步反应被氧化成NO3-,两步反应的能量变化示意图如下:
(1)1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是 ________。
(2)在一定条件下,向废水中加入CH3OH,将HNO3还原成N2,若该反应消耗32gCH3OH转移6mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
(Ⅱ)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO
某温度下用气体传感器测得不同的时间的NO和CO浓度如下表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H _____ 0(填写“>”、“<”、“=”)
(2)前2s内的平均反应速率v(N2)= ______;
(3)在该温度下,反应的平衡常数K= _______(只写出计算结果);
(4)某同学设计了三组实验,分别验证温度、催化剂比表面积对化学反应速率的影响规律,部分实验条件如下表:
该同学画出了表中三个实验条件下,混合气体中NO浓度随时间变化的趋势曲线图,请在图上标明各条曲线的实验编号;
(5)有人认为:催化剂比表面积增大,会提高NO和CO的反应效率,从而使污染物NO和CO的转化率提高。请用化学基本理论对此观点进行评价:________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析