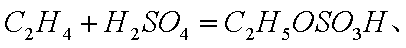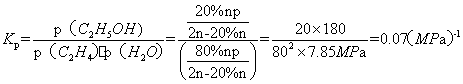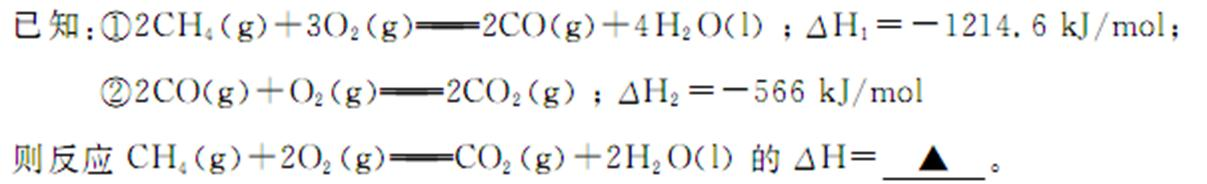- 盖斯定律的计算
- 共35题
氢气是清洁的能源,也是重要的化工原料。
(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:
N2(g)+3H2(g)=2NH3(g) △H=―92.40 kJ·mol-1
2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=―159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O (l) △H=+72.49 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为 。
(2)CO在催化剂作用下可以与H2反应生成甲醇CO(g)+2H2(g) 
①M、N两点平衡状态下,容器中总物质的物质的量之比为:n(M):n(N)= 。
②若M、N、Q三点的平衡常数KM、KN、KQ的大小关系为 。
(3)已知叠氮酸(HN3)不稳定,同时也能与活泼金属反应,反应方程式为:
2HN3=3N2↑+H2↑ 2HN3+Zn=Zn(N3)2+H2↑
则2 mol HN3与一定量Zn完全反应,在标准状况下生成67.2 L气体,其中N2的物质的量为 。
(4)已知H2S高温热分解制H2的反应为: H2S(g)

(5)用惰性电极电解煤浆液制H2的反应为: C(s)+2H2O(l)=CO2(g)+2H2(g) 现将一定量的1 mol·L-1 H2SO4溶液和适量煤粉充分混合,制成含碳量为0.02 g·mL-1~0.12g·mL-1的煤浆液,置于上图2所示装置中进行电解(两电极均为惰性电极),则A极的电极反应式为 。
正确答案
(1)
(2)① 5:4 ②KM=KN>KQ
(3)2 mol
(4) 0.4c/t mol·L-1·min-1;温度升高,反应速率加快,达到平衡所需的时间缩短(合理答案均可)
(5)C+2H2O-4e-=CO2↑+4H+
解析
略
知识点
乙醇是重要的有机化工原料.可由乙烯气相直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇写出相应反应的化学方程式 。
(2)已知:
甲醇脱水反应:2CH3OH(g)= CH3OCH3(g)+ H2O(g) △H1=-23.9KJ·mol-1
甲醇制烯经反应:2CH3OH(g)= C2H4(g)+2 H2O(g) △H2=-29.19KJ·mol-1
乙醇异构化反应: C2H5OH(g)= CH3OCH3(g) △H3=+50.7KJ·mol-1
则乙烯气相直接水合反应:C2H4(g)+ H2O(g)= C2H5OH(g)的△H= KJ·mol-1与间接水合法相比,气相直接水合法的优点是_
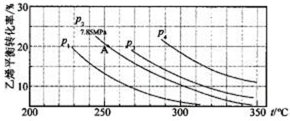
(3)下图为气相直接水合法中乙烯的平衡转化率与温度.压强的关系[其中N(H2O):N(C2H4)=l:1]。
①列式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②图中压强(P1.P2.P3.P4)的大小顺序为_ ,理由是_ .
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃.压强69MPa:气。N(H2O):N(C2H4)=0.6 :1。乙烯的转化率为5%.若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有 . 。
正确答案
(1)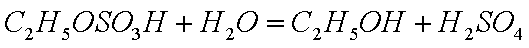
(2)-45.5 污染小、腐蚀性小等
(3)①
②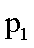
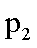
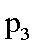
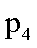
③将产物乙醇液化移去 增加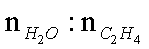
解析
略
知识点
火力发电厂释放出大量气体会造成环境污染。对燃煤废气进行处理,可实现绿色环保、废物利用等目的。
(1)CO可以与H2O(g)发生反应:CO(g) + H2O(g) 
在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0。
①该反应的平衡常数表达式为 。
②平衡时,丙容器中H2O的物质的量是 mol,甲容器中CO的转化率是 ,
容器中CO的转化率:乙 甲(填“>”、“=”或“<”)。
③丙容器中,其他条件不变时,温度 (填“升高”或“降低”),CO的平衡转化率升高。
(2)除去氮氧化物:
① 利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为__________
② 也可用氨气与之发生反应:NOx+NH3→N2+H2O。
现有NO2和NO的混合气体3.0 L,跟3.4 L(同温同压下)NH3反应,恰好使其全部转化为氮气,则原混合气体中,NO2与NO的体积比是__________。
正确答案
见解析。
解析
(1)①
②0.1 50% >
③ 降低
(2)①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol (3分)
② 7 : 3
知识点
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用焦炭与水蒸气在高温下的反应产物(水煤气)合成二甲醚。请回答下列问题:
(1)制水煤气的主要化学反应方程式为: 。
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为: 。
(3)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g)


② 2CH3OH(g)


③ CO(g)



总反应:3H2(g)




一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
(填字母代号)。
a,低温高压 b,加入催化剂 c,减少CO2的浓度 d,增加CO的浓度
(4)已知某温度下反应②2CH3OH(g)

比较此时正、逆反应速率数值(单位相同)的大小:

反应开始时

该时间内的平均反应速率

该温度下反应的平衡常数值为 。(精确到0.01)
正确答案
(1)C +H2O 
(2)H2S+Na2CO3 →NaHS + NaHCO3
(3)246.4 a c
(4) > 1.64 mol·L-1 0.12mol/L·min 1.86
解析
略
知识点
25℃、101kPa 下:
①2Na(s)+1/2O2(g)→Na2O(s)+414KJ
②2Na(s)+O2(g)→Na2O2(s)+511KJ下列说法正确的是()
正确答案
解析
略
知识点
11.现在科学家正在寻求将太阳能转化成化学能,其中办法之一就是利用太阳能将H2O分解成H2,再将化学能转化为其它能源。下面是有关的能量循环示意图,下列有关说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.新的《环境空气质最标准》(GB3095-2012)将于2016年1月1日在我国全面实施。据此,环境空气质量指数(AQI)日报和实时报告包括了SO2、NO2、CO、O3、PM10、PM2.5等指标,为公众提供健康指引,引导当地居民合理安排出行和生活。
(1)汽车排出的尾气中含有CO和NO等气体,用化学方程式解释产生NO的原因____。
(2)汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物转化为无毒的大气循环物质。已知:
则反应
该反应的△S_____________0(填“>”、“<”或“=”)。
(3)将0.20molNO和0.10 molCO充入一个容积恒定为1L的密闭容器中,在不同条件下反应过程中部分物质的浓度变化状况如图所示。
①计算产物N2在6~9min时甲均反应速率v(N2)= ______mol·L-1·min-1;
②第12min时改变的反应条件为 ________(填“升温”、“降温”)
③计算反应在第24min时的平衡常数K=_________。若保持温度不变,再向容器中充入CO、N2各0.060mol,平衡将____移动(填“正向”、“逆向”或“不”)。
(4)环境监测中还可用沉淀法测定空气中含有较高浓度SO2的含量,经查得一些物质在20℃的数据如下表:
④吸收SO2最合适的试剂是___________[填“Ca(OH)2”或“Ba(OH)2”]溶液:
②在20℃时,向CaSO3悬浊液中滴加适最的BaCl7溶液,当CaSO3向BaSO3的转化达到平衡时,溶液中的
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.用CH4催化还原NO,可以消除氮氧化物的污染。例如:

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.汽车安全气囊在初次发生猛烈碰撞后的几十毫秒内迅速打开,可有效缓冲驾驶员和前排乘客所遭受的冲击力度,保护其头部不受伤害。汽车安全气囊中含有MYn和红棕色金属氧化物、SiO2等物质。M、Y为短周期元素,其最外层电子数之和等于氧原子的最外层电子数,且可发生下图的转化关系。
(1)在2L密闭容器中投入2molY2和3.5molH2发生反应Ⅱ,测得YH3的物质的量在温度T1、 T2下随时间的变化如表所示:
① 已知该反应△H<0,则T1 T2 (填“>”、“<”或“=”);
②在温度T2下,达到平衡时YH3的平均速率v(YH3)= ( );平衡常数为( )(保留两位有效数字)。
③T2温度下达到平衡后,将容器的容积压缩到原来的1/2.在其他条件不变的情况下,对平衡体系产生的影响是 ( ) 。(填字母)。
A.c(H2)减少 B.正反应速率加快,逆反应速率减慢
C.YH3的物质的量增加 D.重新平衡时c(H2)/c(YH3)减小
(2) Y2H4是一种可燃性的液体,可用作火箭燃料。
①已知:N2(g)+2O2(g)==2NO2(g);△H= +67.7 kJ·mol-1
2N2H4(g)+2NO2(g) = 3N2(g) + 4H2O(g) △H=-1135.7 kJ·mol-1
计算反应:N2H4(g)+O2(g)==N2(g)+2H2O(g)△H=( ) kJ·mol-1
②水的电离方程式也可写为:H2O+H2O H3O++OH-,若液态Y2H4能够按照类似方式电离,请写出电离方程式:___________________________________。
③传统制备Y2H4的方法,是以MClO氧化YH3制得。反应Ⅲ的离子方程式是__________。
(3)Y2H4-空气燃料电池是一种高能电池,用20%-30%的KOH充当电解质溶液,则电池放电时的负极的电极反应式是 ( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.(Ⅰ)碳和碳的化合物在人类生产、生活中的应用非常广泛。“低碳生活”不再只是一种理想,更是一种值得期待的生活方式。
(1)甲烷燃烧时放出大量的热,可作为能源应用于人类的生产和生活。
(2)将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。
其负极电极反应式是:叁一。
(3)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应:

①实验1中,以v( H2)表示的平均反应速率为:( )。
②该反应的正反应为( )(填“吸”或“放”)热反应;
③若要实验3达到与实验2相同的平衡状态(即各物质的体积分数分别相等),则a、b应满足的关系是( )(用含a、b的数学式表示)。
(Ⅱ)某小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2 SO4溶液。
①该电解槽中通过阴离子交换膜的离子数( )(填“>”“<”或“一”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为( );
③电解一段时间后,B出口与C出口产生气体的质量比为( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析