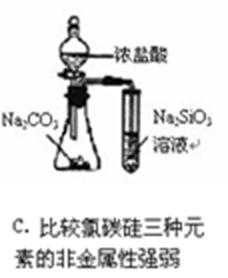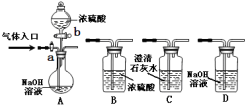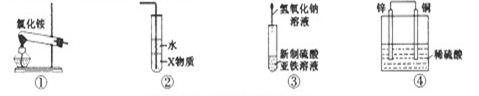- 连接仪器装置
- 共17题
化工厂铬渣中含有Na2SO4及少量Cr2O72-、Fe3+,下面是从铬渣提取Na2SO4和利用副产品制取FeCl3的工艺流程。已知:Fe3+、Cr3+完全沉淀(c≤1.0×10-5mol•L-1)时pH分别为3.6和5。
(1)①操作C加硫酸酸化而不选用盐酸的原因是________。
②酸化后Cr2O72-可被SO32-还原成Cr3+,离子方程式为________。
③根据溶解度(S)∽温度(T)曲线,操作B的最佳方法为________(填字母序号)。
A. 蒸发浓缩,冷却结晶,过滤
B. 蒸发浓缩,趁热过滤
④温度相同时Ksp[Cr(OH)3]________Ksp[Fe(OH)3](填“>”或“<”)
(2)已知FeCl3从溶液中析出的是FeCl3•6H2O,在空气中直接加热FeCl3•6H2O晶体得不到纯的无水FeCl3,原因是________(用化学方程式表示)。由FeCl3•6H2O晶体得到纯的无水FeCl3的合理方法是________。
(3)下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是________。
A. a—b—c—d—e—e—f—g—h
B. a—c—b—d—e—h—i—f
C. a—d—e—c—b—h—i—g
D. a—e—d—c—b—h—i—g
若以KMnO4和浓盐酸为原料来制取Cl2,并希望能控制反应速率,下列最适合的装置是________(已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2
正确答案
(1)①酸性环境Cl-被Cr2O72-氧化生成Cl2污染环境,引入NaCl杂质导致产品不纯;②3SO32-+Cr2O72-+8H+=2Cr3++3SO42-+4H2O;③B;④>
(2)FeCl3•6H2O
(3) D;④
解析
略。
知识点
亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:① NO+NO2+2OH-=2NO2-+H2O
② 气体液化的温度:NO2 21℃ 、 NO –152℃
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接):
A 、 C 、 、 、
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是 。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是 。
②装置E的作用是 。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为 。
如果没有装置C,对实验结论造成的影响是 。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是 。
正确答案
见解析。
解析
(1) E 、 D 、 B
(2) 防止可能生成的NO被完全氧化成NO2 ,造成对A中反应气体产物检验不完全
(3)① D中出现红棕色气体 ② 冷凝使NO2完全液化
(4) 4NO2 + O2 + 4NaOH = 4NaNO3 +2 H2O
水蒸气存在,会与NO2反应产生NO,造成对NO来源于哪里的认识不清
(5) 2NaNO2 + H2SO4 = Na2SO4 + NO2↑ + NO↑+ H2O
知识点
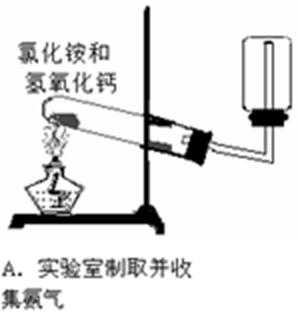
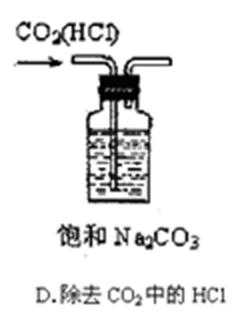
9.下列实验中,能够达到实验目的的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
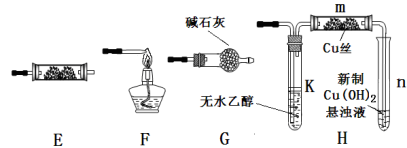
29.下图为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去,已知乙醇的沸点为78.5℃),请根据要求完成下列问题(仪器装置可任意选用,必要时可重复选择,a、b为旋钮)。
(1)若A中气体入口通入CO和CO2的混合气体,E内放置CuO,欲得到纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为( )(填写装置代号)。能验证CO氧化产物的实验现象是( )。
(2)完成(1)实验后,将A中a旋钮关闭,并在E内放置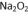
①为获得氧气,关闭a旋钮后,首先需进行的操作是( )。
②为得到平稳的乙醇蒸气流,提高反应效率,可采取的措施是(用文字简述)( );m中发生反应的化学方程式是( )。
③若想观察到试管n中有红色沉淀出现,还需要进行的操作是( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.关于下列各装置图的叙述中,正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析