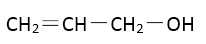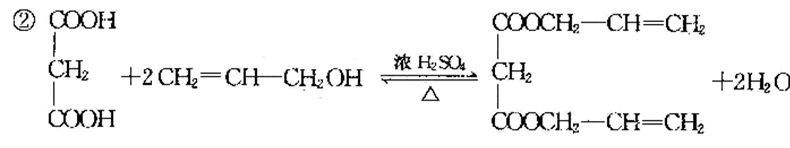- 常见有机物及其应用
- 共1422题
36.请从36-38题中任选一题作答。
36.【化学—选修2:化学与技术】
生态工业园区的建设,不仅仅是体现环保理念更要依据循环经济理论和充分考虑经济的可持续发展。如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产三大生态产业链流程图。
根据上述产业流程回答下列问题:
(1)从原料、能源、交通角度考虑该企业应建在( )
A.西部山区 B.沿海地区 C.发达城市 D.东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式①( ),②( ),③ ( ),④( ),⑤ ( )。
(3)沸腾炉中发生反应的化学方程式 ( ),磷肥厂的产品是普钙,其主要成份是( )(填化学式)。
(4)热电厂的冷却水是( ),该流程中浓缩盐水除提取盐以外还可提取的物质有( )(写出一种即可)。
(5)根据生态园区建设理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想( ),( )(请写出两点)。
37.【化学—选修3物质结构与性质】
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用。
(1)N位于周期表中第__________周期__________族,与N3-含有相同电子数的三原子分子的空间构型是__________。
(2)C、N、O三种元素的第一电离能由大到小的顺序为( )。
(3)Cu+的电子排布式为___________,其在酸性溶液中不稳定,可发生歧化反应生成Cu2+和Cu,但CuO在高温下会分解成Cu2O,试从结构角度解释高温下CuO为何会生成Cu2O____________________。
(4)在Cu的催化作用下,乙醇可被空气氧化为乙醛,乙醛分子中碳原子的杂化方式是______,乙醛分子中H—C—O的键角__________乙醇分子中的H—C—O的键角。(填“大于”、“等于”或“小于”)
(5)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被Cl-取代有两种不同的结构,试画出[Cu(H2O)2(Cl)2]具有极性的分子的结构式__________。
(6)Cu3N的晶胞结构如右图,N3-的配位数为__________,Cu+半径为a pm,N3-半径为bpm,Cu3N的密度__________g/cm3。(阿伏加德罗为常数用NA表示)(1pm=10-10cm)
38.【化学—选修5:有机化学基础】
有机物D是一种合成抗高血压药的重要通用中间体,其合成路线如下:(已知A是一种芳香酸)
(1)A、C的结构简式分别是( )、( ) 。D中含有的含氧官能团名称是 ( )。
(2)C→D的反应类型是 ( )。
(3)加热条件下,C在足量NaOH水溶液中反应的化学方程式是 ( ) 。
(4)E是一种相对分子质量比A小14的芳香酸。写出满足下列条件的E的所有同分异构体的结构简式:( ) 。
①能发生银镜反应 ②一定条件下可发生水解反应 ③分子的核磁共振氢谱中有四组峰。
(5)F是B在碱溶液中水解后再酸化的产物。F在一定条件下可聚合成高分子化合物,写出该反应的化学方程式 ( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
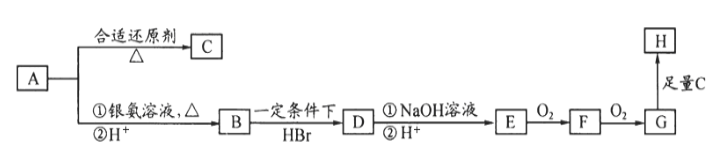
30.有机物A为常用药中的主要成分,A(
(1)反应①、②都属于取代反应。其中①是( )反应,②是( ) 反应(填有机反应名称)。
(2)B有两种同分异构体,且都能在一定条件下发生银镜反应,写出这两种同分异构体的结构简式( ) 、( ) 。
(3)写出A与
(4)C的结构简式是:( )。
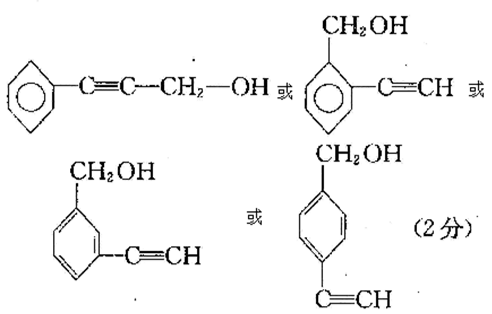
(5)同时符合下列四个要求的C的同分异构体共有( )种。
①含有苯环;
②能发生银镜反应,不能发生水解反应;
③在稀


④只能生成两种一氯代产物
(6)从(5)确定的同分异构体中任选一种,写出与银氨溶液反应的方程式( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.I.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。结构简式如图:
(1)对羟基肉桂酸的分子式为 ,其所含氧官能团的名称是( )。
Ⅱ,芳香族化合物A有如下的转化关系:
已知E能使Br2的CCl4溶液褪色。
(2)有机物A中氧元素的百分含量为( ),B的结构简式为( )。有机物D不能发生的反应是(填写代号)( )。
A.氧化反应 B.消去反应 C.加成反应 D.水解反应
(3)若有机物F与C互为同分异构体且与有机物B互为同系物,F分子中有四种空间位置不同的氢原子,则符合条件的F的结构简式为( )。
(4)请写出D→E反应的化学方程式:( )。在D→E反应过程中,还会生成另一种高分子化合物,其结构简式为( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.芳香酯类化合物A、B互为同分异构体,均含C、H、O三种元素。并且各有机物间存在如下转化关系:
其中C能发生银镜反应,F经连续氧化可生成C;C与D是相对分子质量相同的不同类有机物。
(1)C中所含官能团的名称是( )。
(2)A的分子式是( )。B的结构简式是 ( )。
(3)完全燃烧时,1 mol D与1 mol 下列( )的耗氧量相同(填字母代号)。
a.


(4)C与F反应的化学方程式是( ),反应类型是( )。
(5)水杨酸
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.丙二酸是有机合成的重要原料,可通过下列途径制备:
请回答下列问题:
(1)A的名称(系统命名)是( ) 。丙二酸与草酸(HOOC-COOH)的关系是( ) 。
(2)写出A—B的化学方程式: ( ) 。
(3)已知C中只含一种官能团,写出C的结构简式:( )。
(4)丙二酸用于合成治疗偏头痛的药物阿魏酸钠的路线如下:
①根据流程中的反应,写出下列反应中有机产物的结构简式:
②1 mol F与溴水反应,可消耗 mol Br2。无机试剂X是( )(填化学式)。
③D有多种同分异构体,写出其中含有苯环、能发生水解反应和银镜反应、能与钠反应生成氢气但不具有酸性的一种同分异构体的结构简式:( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
36.请从36~38题中任选一题作答
36.[化学——选修2:化学与技术]
以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是(可多选)
A.CH2=CH2+HCl
B.CH3CH2OH+HCl
C.CH3CH3+Cl2
D.CH2=CHCl+H2
由上述四个反应可归纳出,原子经济性高的是( )反应(填反应类型)。
(2)有毒物质的无害化也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,还可将废水中少量的S2-、NO2- 和CN-等有毒有害的还原性酸根离子氧化除去。请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式( ),并说明该方法的优点 ( )。
(3)下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图:
活性炭的作用是 ( );O3消毒的优点是( ) A、B中放置的物质名称分别是:A( ) B( ) 。
37.[化学一选修3:物质结构与性质]
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1) 太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的外围电子排布式__________,它位于周期表____________区。
(2) 富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如上图,分子中碳原子轨道的杂化类型为________;1 mol C60分子中σ键的数目为____________个。
(3) Cu单质晶体中原子的堆积方式如上图甲所示,其晶胞特征如上图乙所示,原子之间相互位置关系的平面图如上图丙所示。晶胞中Cu原子的配位数为____________,一个晶胞中Cu原子的数目为________。
(4)设Cu晶体的密度为
(5)Fe(CO)5常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________(填晶体类型);Fe(CO)5是配合物,配体.配位数分别是________.________。
38.[化学——选修5:有机化学基础]
已知碳碳双键可以被臭氧氧化:
有机物A可以发生如下图所示的变化,其中E不能发生银镜反应,D能发生银镜反应,1molD与足量的新制的银氨溶液反应最多可产生4mol的银;M的分子内含有七元环状结构。
(1)A的结构简式_______________________________。
(2)A~M中,互为同系物的是____________(填字母代号)。
(3)B的同分异构体中,具有链状结构(即不是环状结构,可以有支链)的酯类物质有_____种,请写出其中一种物质的结构简式____________。
(4)写出下列反应的化学方程式。
①F→G:____________ 。
②C+L→M:____________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.有机物A是重要的合成原料,在医药、染料、香料等行业有着广泛的应用。由A可以制得麻黄碱和其他很多物质。现有如下转化关系图(略去了由A→G,G→麻黄碱的部分反应物和条件):
请回答下列问题:
(1)关于麻黄碱下列说法正确的是 ( )(填字母)。
a.麻黄碱的分子式为C10H15NO
b.1mol麻黄碱可以对应消耗1molHCl或NaOH
c.麻黄碱可以发生消去和酯化反应
d.麻黄碱属于芳香烃
(2)已知有机物A的相对分子质量为106,A中含碳、氢、氧的质量之比为42:3:8,
则A的含氧官能团名称是( );检验该官能团的实验是 ( ) 。
(3)反应①~⑤中属于取代反应的是( )(填序号)。
(4)写出D—B的化学方程式 ( )。
(5)F可作多种香精的定香剂,请写出B和C反应生成F的化学方程式( ) 。
(6)写出符合下列条件的同分异构体的结构简式( ) 。
①与中间产物G互为同分异构体
②既能发生消去反应,又能发生酯化反应
③苯环上的一氯取代物只有两种,分子结构中没有甲基
(7)已知:
A可以由E制取,制取工艺中得到的是A、E混合物,分离该混合物的方法是( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.某种对苯二甲酸酯常用作塑料增塑剂,其结构简式如图所示。(R表示相同的烃基)
I.甲同学通过燃烧法确定某对苯二甲酸酯M的含氧量(质量分数)为23.0%。请回答下列问题:
(1)请确定M的分子式为( ) 。
(2)有关对苯二甲酸酯M的说法正确的是( )。
A.M能与稀硫酸溶液反应生成醇和羧酸
B.1mol M在催化剂、加热的条件下最多与5 mol
C.M能发生氧化反应
D.
II.乙同学研究工业合成对苯二甲酸酯的性质如下:
已知M与NaOH溶液反应生成两分子的C,而且E不能发生银镜反应。
请回答下列问题:
(1)请写出E的结构简式:E( )。
(2)写出下列反应的化学方程式:D与足量NaHCO3溶液的反应( )。C生成E的反应( )。
(3)D物质的环上一氯代物有( )种。
(4)N物质是比D物质少一个羧基的化合物,请写出N所有的同分异构体(含苯环)结构简式( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
29.如下图所示:
已知:①相对分子质量的关系: M(F)=M(I) , M(B)>M(C)
②-OH和-Cl不能连接在同一个碳原子上。
③八元环酯(J)的结构简式为
请回答:
(1)B中所含官能团的名称:_________________;
(2)写出下列物质的结构简式:H_______________,I______________;
(3)与C互为同类物质的同分异构体结构简式为__________________________(写出一种即可);
(4)写出下列反应的化学方程式和反应类型:
F → G_________________________;______ ___反应
A → D + E_____________________;___________反应
正确答案
29.(1)羧基
(2) 
(3)
(4)

解析
解析已在路上飞奔,马上就到!
知识点
30.对-甲乙苯(
已知:①1molD与足量钠反应可生成1mol氢气;
②D、E、F每种分子中均只含有一种含氧官能团。
③G是一种有机高分子化合物。
回答下列问题:
(1)A的结构简式为____________。
(2)A→B的反应类型为___________;F中含氧官能团的名称为____________。
(3)C在引发剂的作用下,可生成高分子化合物,该高分子化合物为__________。
(4)1molE和足量银氨溶液反应,生成沉淀的物质的量为___________。
(5)
(6)H比D相对分子质量小14,H的同分异构体能同时满足如下条件:
①苯环上有两个取代基;②遇氯化铁溶液显紫色;
③苯环上一氯代物只有2种
写出H的这种同分异构体的简式___________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.聚酯纤维在服装、室内装饰和工业领域中有广泛应用。下图是合成某种聚酯纤维H的流程图。
已知:①A、D为烃;
②G的相对分子质量为166,其中含碳57.8%,含氢3.6%,其余为氧;G能与
(1)①、③ 的反应类型依次为( ) 、( );
(2)B的名称为:( );E的结构简式为:( );
(3)写出下列化学方程式:
②( );
⑥ ( );
(4)F有多种同分异构体,写出同时符合下列条件的所有同分异构体的结构简式 ( );
a.含有苯环且苯环上只有2个取代基
b.能与NaOH溶液反应
c.在Cu催化下与O2反应的产物能发生银镜反应
正确答案
(4)
解析
解析已在路上飞奔,马上就到!
知识点
36.请从36~38题中任选一题作答
36.【化学—选修2:化学与技术】
硫酸铅广泛应用于制造蓄电池。利用锌冶炼过程中的铅浮渣生产硫酸铅的流程如下:
已知铅浮渣的主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。25℃时,Ksp(CaSO4)=4.9×10-5,Ksp(PbSO4)=1.6×10-8。
(1)已知步骤Ⅰ有NO产生,浸出液中含量最多的阳离子是Pb2+。分别写出PbO、Pb参加反应的离子方程式( )、( )。
(2)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,目的是( )。
(3)母液可循环利用于步骤Ⅰ,其溶质主要是( )(填一种物质化学式),若母液中残留的SO42-过多,循环利用时可能出现的问题是 ( ) 。
(4)产品PbSO4还需用Pb(NO3)2溶液多次洗涤,目的是除去( ) 。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为( )。
37.【化学—选修3:物质结构与性质】
人类使用铜和它的合金具有悠久的历史,铜及其化合物在电子工业、材料工业、工农业生产及日常生活方面用途非常广泛。试回答下列问题。
(1)Cu+的核外电子排布式为( )。
(2)铜镁合金是一种储氢材料,某种铜镁互化物晶胞结构如图,则该互化物的化学式为( )。
(3)叠氮化铜[Cu(N3)2]是一种紫黑色粉末,易爆炸,与N互为等电子体的分子有( )(举2例)。
(4)丁炔铜是一种优良的催化剂,已知:CH≡CH+2HCHO
(5)若向盛有CuSO4溶液的试管里加入氨水,首先形成蓝色难溶物,继续加入氨水,难溶物溶解,变成蓝色透明溶液,这时得到一种称为硫酸四氨合铜的物质,该物质的化学式______________,其中含有的化学键类型有( )。
38.【化学—选修5:有机化学基础】
现有分子式为C10H10O2Br2的芳香族化合物X,X中苯环上有四个取代基,苯环上的一氯代物只有一种,其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1261,在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。
已知:
①在稀碱溶液中,连在苯环上的溴原子不易发生水解
②两个羟基同时连在同一碳原子上的结构是不稳定的,它将自动发生脱水反应:
CH3CH(OH) 2→CH3CHO +H2O
回答下列问题:
(1)C的结构简式为( );F→H的反应类型是( )。
(2)E不具有的化学性质( )(选填序号)
a、取代反应
b、消去反应
c、氧化反应
d、1molE最多能与2mol NaHCO3反应
(3)写出下列反应的化学方程式:
① X与足量稀NaOH溶液共热的化学方程式:( );
② A→B的化学方程式:( );
(4)同时符合下列条件的E的同分异构体共有( )种,
a、苯环上的一氯代物有两种
b、不能发生水解反应
c、遇FeCl3溶液不显色
d、1molE最多能分别与1molNaOH和2molNa反应
其中核磁共振氢谱为六组峰,且峰面积比为322111的一种结构简式为 ( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.已知某烃的含氧衍生物A能发生如下所示的变化。在相同条件下,A的密度是H2的28倍,其中碳和氢元素的质量分数之和为71.4%,C能使溴的四氯化碳溶液褪色,H的化学式为C9H12O4。
(1) A中含氧官能团的名称 ( );C的结构简式为( )。
(2)D可能发生的反应为 ( )(填编号);
①酯化反应 ②加成反应 ③消去反应 ④加聚反应
(3)写出下列反应的化学方程式
① A与银氨溶液:( );
② G
(4)某芳香族化合物M,与A含有相同类型和数目的官能团,且相对分子质量比A大76。则:
①M的分子式为( );
②符合下述条件的M的同分异构体有( )种:i属于芳香族化合物;ii不与FeCl3溶液发生显色反应,但能与Na反应。写出其中1种的结构简式 ( ) 。
正确答案
(1)醛基 ;
(2)①③
(3)①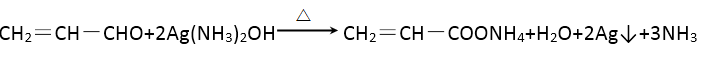
(4)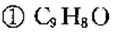

解析
解析已在路上飞奔,马上就到!
知识点
28.芳香酯类化合物A、B互为同分异构体,在一定条件下均可生成水杨酸,且均含C、H、O三种元素。相同状况下,A、B蒸气对氢气的相对密度是97,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍。
(1)A的分子式是( )。
已知各有机物间存在如下转化关系:
其中C能发生银镜反应,F经过连续氧化可生成C;C与D是相对分子质量相同的但不同类别的有机物。
(2)B的结构简式是__________________________。
(3)有机物C、D、E、F各mg完全燃烧,将产物全部通入Na2O2中,充分反应后Na2O2增重质量等于m g的为 ( ),大于m g的为( ),小于m g的为( )。
(4)写出下列反应的化学反应方程式:
水杨酸与小苏打( )。
C与F反应( )。
A与NaOH溶液共热( ) 。
(5)同时符合下列要求的同分异构体。即:
①与水杨酸互为同分异构体; ②可以水解;
③苯环上有两个取代基,且苯环上的一氯代物只有2种。
可能的同分异构体与新制Cu(OH)2共热的化学反应方程式为:( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
36.请从36~38题中任选一题作答
36.[化学—选修化学与技术]
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:
(1)ClO2中所有原子( )(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用
A.饱和食盐水
B.碱石灰
C.浓硫酸
D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是( )
A.二氧化氯可广泛用于工业和饮用水处理
B.二氧化氯的消毒效率比氯气的消毒效率高
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备。化学反应方程式为 ( )。缺点主要是产率低、产品难以分离,还可能污染环境。
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是( ),此法相比欧洲方法的优点是( )。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为( )。此法提高了生产及储存、运输的安全性,原因是 ( )。
37.[化学——选修物质结构与性质]
MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的核外电子排布式( )。
(2)CoTiO3晶体结构模型如图。在CoTiO3晶体中1个Ti原子、1个 Co原子,周围距离最近的O原子数目分别为( )个、( )个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂, 常用于污水处理。O2在其催化作用下,可将CN—氧化成CNO—,进而得到N2。与CNO—互为等电子体的分子、离子化学式分别为( )、( )(各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图。 三聚氰胺分子中氮原子轨道杂化类型是( );1 mol三聚氰胺分子中 σ键的数目为( )。
38.[化学——选修有机化学基础]
已知有机物A~I之间的转化关系如图所示:
①A与D、B与E、I与F互为同分异构体
②加热条件下新制Cu(OH)2悬浊液分别加入到有机物I、F中,I中无明显现象,F中变砖红色。
③C的最简式与乙炔相同,且相对分子质量为104
④B的一种同分异构体与FeCl3发生显色反应。
根据以上信息,回答下列问题:
(1)C中含有的官能团名称为( )
(2)H的结构简式为( )
(3)反应①~⑨中属于取代反应的是( )
(4)写出反应⑥的化学方程式( )
(5)写出 F与新制Cu(OH)2悬浊液反应的化学方程式( )
(6)苯环上含有两个取代基且能与NaOH溶液反应,但不与FeCl3发生显色反应的G的同分异构体有( )种。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析