- 物质的分离、提纯和检验
- 共229题
高锰酸钾是一种常用的氧化剂。下图是利用软锰矿(主要成分为MnO2)制备高锰酸钾的一种工艺(流程中部分产物已略去):
相关物质不同温度下的溶解度(单位:g)数据如下表:
18.“熔融”步骤反应的化学方程式为 。
19.K2MnO4溶液中加入冰醋酸发生反应的离子方程式为: 。
20.操作2是 、 、 。
21.图中可以直接进行循环利用的物质是(填化学式) 。
22.KMnO4粗晶体中的主要杂质(填化学式)有 和 ,若用硫酸代替图中的冰醋酸,则导致的问题及原因是 。
正确答案
3MnO2 +KClO3 +6KOH
解析
3MnO2 +KClO3 +6KOH
考查方向
本题主要考查了考查物质制备工艺流程图分析。
解题思路
1、化工流程中的实验分析化工流程的命题来源很广,与各个知识模块的结合点较多,因此分析工业生产化工流程题时,应将流程路线、试题设问和理论知识有机结合起来,它常常结合工艺流程考查基本化学实验问题,可以说它是无机框图题的创新。流程的呈现形式有:①操作流程;②物质变化流程;③装置流程。制备装置的识图技巧①明确目的;②所制备物质是否有特殊性质(即是否需要特殊保护);③制备过程中是否产生有毒气体等;④进入每一装置的物质是什么,吸收了什么物质或生成了什么物质。
2、解题时首先要明确原料和产品(包括副产品),即箭头进出方向,其次依据流程图分析反应原理,紧扣信息,搞清流程中每一步发生了什么反应——知其然,弄清有关反应原理,明确目的(如沉淀反应、除杂、分离)——知其所以然,最后联系储存的知识,有效地进行信息的利用,准确表述和工整书写。由于化工流程常与溶液的配制、物质的分离及定量测定等基本操作有机结合起来,所以只有复习时牢固掌握实验基础知识,才能有效结合题中的信息,准确答题。
易错点
1、氧化还原方程式的配平。
2、离子方程式定量的书写。
正确答案
3MnO42-+4CH3COOH=2MnO4-+MnO2↓+2H2O+4CH3COO-。
解析
3MnO42-+4CH3COOH=2MnO4-+MnO2↓+2H2O+4CH3COO-。氧化还原反应的实质是反应过程中发生了电子转移,而氧化剂得电子总数(或元素化合价降低总数)必然等于还原剂失电子总数(或元素化合价升高总数),根据这一原则可以对氧化还原反应的化学方程式进行配平。配平的步骤:
(1)标好价:正确标出反应前后化合价有变化的元素的化合价
(2)列变化:列出元素化合价升高和降低的数值。
(3)求总数:求元素化合价升高和降低的总数,确定氧化剂、还原剂、氧化产物、还原产物的化学计量数
(4)配系数:用观察法配平其他各物质的化学计量数。
(5)细检查:利用“守恒”三原则(即质量守恒、得失电子守恒、电荷守恒),逐项检查配平的方程式是否正确。失误防范 配平氧化还原反应方程式的关键是正确标出化合价,找准1“分子”氧化剂化合价降低总数,1“分子”还原剂化合价升高总数,在计算时,往往容易忽略氧化剂、还原剂中的粒子个数。
考查方向
本题主要考查了考查物质制备工艺流程图分析。
解题思路
1、化工流程中的实验分析化工流程的命题来源很广,与各个知识模块的结合点较多,因此分析工业生产化工流程题时,应将流程路线、试题设问和理论知识有机结合起来,它常常结合工艺流程考查基本化学实验问题,可以说它是无机框图题的创新。流程的呈现形式有:①操作流程;②物质变化流程;③装置流程。制备装置的识图技巧①明确目的;②所制备物质是否有特殊性质(即是否需要特殊保护);③制备过程中是否产生有毒气体等;④进入每一装置的物质是什么,吸收了什么物质或生成了什么物质。
2、解题时首先要明确原料和产品(包括副产品),即箭头进出方向,其次依据流程图分析反应原理,紧扣信息,搞清流程中每一步发生了什么反应——知其然,弄清有关反应原理,明确目的(如沉淀反应、除杂、分离)——知其所以然,最后联系储存的知识,有效地进行信息的利用,准确表述和工整书写。由于化工流程常与溶液的配制、物质的分离及定量测定等基本操作有机结合起来,所以只有复习时牢固掌握实验基础知识,才能有效结合题中的信息,准确答题。
易错点
1、氧化还原方程式的配平。
2、离子方程式定量的书写。
正确答案
蒸发浓缩(或加热浓缩)、冷却结晶(或降温结晶)、过滤。
解析
蒸发浓缩(或加热浓缩)、冷却结晶(或降温结晶)、过滤。
考查方向
本题主要考查了考查物质制备工艺流程图分析。
解题思路
1、化工流程中的实验分析化工流程的命题来源很广,与各个知识模块的结合点较多,因此分析工业生产化工流程题时,应将流程路线、试题设问和理论知识有机结合起来,它常常结合工艺流程考查基本化学实验问题,可以说它是无机框图题的创新。流程的呈现形式有:①操作流程;②物质变化流程;③装置流程。制备装置的识图技巧①明确目的;②所制备物质是否有特殊性质(即是否需要特殊保护);③制备过程中是否产生有毒气体等;④进入每一装置的物质是什么,吸收了什么物质或生成了什么物质。
2、解题时首先要明确原料和产品(包括副产品),即箭头进出方向,其次依据流程图分析反应原理,紧扣信息,搞清流程中每一步发生了什么反应——知其然,弄清有关反应原理,明确目的(如沉淀反应、除杂、分离)——知其所以然,最后联系储存的知识,有效地进行信息的利用,准确表述和工整书写。由于化工流程常与溶液的配制、物质的分离及定量测定等基本操作有机结合起来,所以只有复习时牢固掌握实验基础知识,才能有效结合题中的信息,准确答题。
易错点
1、氧化还原方程式的配平。
2、离子方程式定量的书写。
正确答案
MnO2
解析
图中可以直接进行循环利用的物质是MnO2(操作1中分离的滤渣可重新作为原料投入生产)。
考查方向
本题主要考查了考查物质制备工艺流程图分析。
解题思路
1、化工流程中的实验分析化工流程的命题来源很广,与各个知识模块的结合点较多,因此分析工业生产化工流程题时,应将流程路线、试题设问和理论知识有机结合起来,它常常结合工艺流程考查基本化学实验问题,可以说它是无机框图题的创新。流程的呈现形式有:①操作流程;②物质变化流程;③装置流程。制备装置的识图技巧①明确目的;②所制备物质是否有特殊性质(即是否需要特殊保护);③制备过程中是否产生有毒气体等;④进入每一装置的物质是什么,吸收了什么物质或生成了什么物质。
2、解题时首先要明确原料和产品(包括副产品),即箭头进出方向,其次依据流程图分析反应原理,紧扣信息,搞清流程中每一步发生了什么反应——知其然,弄清有关反应原理,明确目的(如沉淀反应、除杂、分离)——知其所以然,最后联系储存的知识,有效地进行信息的利用,准确表述和工整书写。由于化工流程常与溶液的配制、物质的分离及定量测定等基本操作有机结合起来,所以只有复习时牢固掌握实验基础知识,才能有效结合题中的信息,准确答题。
易错点
1、氧化还原方程式的配平。
2、离子方程式定量的书写。
正确答案
KCl,CH3COOK;反应生成K2SO4,而K2SO4在常温下的溶解度也较小,析出后从而导致产品的纯度降低。或答:硫酸酸性太强,导致MnO4-将Cl-氧化,产生有毒的Cl2,KMnO4损失且纯度降低。
解析
KMnO4粗晶体中的主要杂质(填化学式)有KCl,CH3COOK;,若用硫酸代替图中的冰醋酸,则导致的反应生成K2SO4,而K2SO4在常温下的溶解度也较小,析出后从而导致产品的纯度降低。或答:硫酸酸性太强,导致MnO4-将Cl-氧化,产生有毒的Cl2,KMnO4损失且纯度降低。
考查方向
本题主要考查了考查物质制备工艺流程图分析。
解题思路
1、化工流程中的实验分析化工流程的命题来源很广,与各个知识模块的结合点较多,因此分析工业生产化工流程题时,应将流程路线、试题设问和理论知识有机结合起来,它常常结合工艺流程考查基本化学实验问题,可以说它是无机框图题的创新。流程的呈现形式有:①操作流程;②物质变化流程;③装置流程。制备装置的识图技巧①明确目的;②所制备物质是否有特殊性质(即是否需要特殊保护);③制备过程中是否产生有毒气体等;④进入每一装置的物质是什么,吸收了什么物质或生成了什么物质。
2、解题时首先要明确原料和产品(包括副产品),即箭头进出方向,其次依据流程图分析反应原理,紧扣信息,搞清流程中每一步发生了什么反应——知其然,弄清有关反应原理,明确目的(如沉淀反应、除杂、分离)——知其所以然,最后联系储存的知识,有效地进行信息的利用,准确表述和工整书写。由于化工流程常与溶液的配制、物质的分离及定量测定等基本操作有机结合起来,所以只有复习时牢固掌握实验基础知识,才能有效结合题中的信息,准确答题。
易错点
1、氧化还原方程式的配平。
2、离子方程式定量的书写。
仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的的是
正确答案
解析
本题 涉及的实验全部取材于课本,主要考查常见实验仪器的使用方法、溶液pH与c(H+)的换算,同时考查考生对基本化学实验的操作能力及其教材实验的再现能力。让真正做过实验的考生能发挥其优势。
A选项:乙酸乙酯和乙醇是互溶不分层的液体,不能用分液漏斗分液。欲从乙酸乙酯和乙醇的混合物中分离出乙 醇,通常需要蒸馏分离(由于乙酸乙酯和乙醇的沸点相差很小,乙酸乙酯的沸点77.06℃,乙醇的沸点78℃,通常要加足量无水CaCl2吸收乙醇后,再蒸馏,对得到的醇和物蒸馏收集得到乙醇)。
B选项:由0. 1 mol •L-1的盐酸配制100 mL 0. 01 mol •L-1的盐酸,需要用酸式滴定管(或移液管)准确量取10.0 mL0. 1 mol •L-1的盐酸,而提供玻璃仪器缺少量具。
C选项:只用试管、胶头滴管就可证明溴水、淀粉-KI溶液比较Br2与I2的氧化性强弱。故C项正确。
D选项:实验室中用NH4Cl固体和Ca(OH)2固体制备并收集NH3需要用到的玻璃仪器有大试管、酒精灯、导管、集气瓶,而提供玻璃仪器缺少制备NH3的大试管。
知识点
下列试验中,所选装置不合理的是( )
正确答案
解析
A项,乙酸乙酯难溶于碳酸钠溶液,已分层,可以用分液法分离,选择③装置,A项错误;B项,用四氯化碳萃取碘水中的碘,选择装置③,B项正确;C项,⑤装置可以用作洗气瓶,用氯化亚铁溶液吸收氯气,C项正确;D项,粗盐提纯需要过滤、蒸发结晶,选择①和②装置正确,D项正确。
知识点
下列选项中所采取的分离方法与对应原理都正确的是
正确答案
解析
A错,萃取的原则之一是两种溶剂互不相溶,但乙醇易溶于水中,故不能分离;
B错,分液原理是分离互不相溶的液体,乙酸乙酯和乙醇均为液体有机物,可以互溶;
C错,重结晶可以分离KNO3中混杂的NaCl是因为KNO3的溶解度随温度变化比NaCl大。
知识点
下列有关实验装置进行的相应实验,能达到实验目的的是
正确答案
解析
本题属于基础实验与基本实验操作的考查范畴。
A图1所示装置中氢氧化钠会与Cl2反应。
B NH4Cl晶体受热分解,会“假升华”。
C纯碱是可溶性固体,不能用此装置,改在圆底烧瓶和分液漏斗的组合中进行。
D用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层,有机层从下口放出,水层从上口倒出,实现分液。
本题以常见气体制取、蒸干、除杂、萃取、分液为实验操作为素材,考查学生对实验操作的熟悉程度和实验原理的应用能力,试图引导中学化学教学关注化学实验操作的真实性。
知识点
下列图示实验正确的是
正确答案
解析
略
知识点
按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物:
下列说法错误的是
正确答案
解析
步骤(1)是分离固液混合物,其操作为过滤,A项正确;步骤(2)分离互不相溶的液体混合物,需进行分液,要用到分液漏斗,B项正确;步骤(3)是从溶液中得到固体,操作为蒸发,需要蒸发皿,C项错误;步骤(4)是从有机化合物中,利用沸点不同采取蒸馏得到甲苯,D项正确。
知识点
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
①Ni(S)+4CO(g)

完成下列填空:
(1)在温度不变的情况下,要提高反应(1)中Ni(CO4)的产率,可采取的措施有 、 。
(2)已知在一定条件下的2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如下图所示。Ni(CO)4在0~10min的平均反应速率为 。
(3)若反应(2)达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 。
A.平衡常数K增大
B.CO的浓度减小
C.Ni的质量减小
D.v逆[Ni(CO)4]增大
(4)简述羰基法提纯粗镍的操作过程。
正确答案
(1)增大CO浓度,加压。
(2)0.05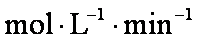
(3)bc。
(4)把粗镍和CO放于一个水平放置的密闭的玻璃容器中,然后在低温下反应,一段时间后在容器的一端加热。
解析
(1)反应(1)是正向气体体积缩小的放热反应,因此,根据平衡移动原理在温度不变的情况下采取可增大CO浓度,加压的方法提高产率;
(2)根据题意,反应的Ni为1mol,则生成

(3)反应(2)正向气体体积增大的吸热反应,降低温度平衡逆向移动,平衡常数K、CO的浓度、Ni的质量、v逆[
(4)根据反应①②的特点可提纯粗镍。
知识点
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:
甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是的 。
②萃取用到的分液漏斗使用前需 并洗净,分液时有机层在分液漏斗的 填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是 ;用饱和食盐水洗涤的目的是 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是 (填字母)。
a,蒸馏除去乙醚 b,,重结晶 c,过滤除去干燥剂 d,加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先 ,再 。
正确答案
见解析。
解析
(1)①蒸馏② 检查是否漏水 上
(2)除去HCl 除去少量NaHCO3 且减少产物损失
(3)dcab
(4)拆去连接抽气泵和吸滤瓶的橡皮管 关闭抽气泵
知识点
下列叙述错误的是
正确答案
解析
钠和乙醇反应有气泡产生,而钠和乙醚不反应;3-己烯可以使高锰酸钾酸性溶液褪色,而己烷不能;苯的密度比水小,而溴苯的密度比水的密度大;甲酸甲酯分子结构中也含有醛基,故用新制的银氨溶液不能区分甲酸甲酯和乙醛,故D项错误。
知识点
扫码查看完整答案与解析