- 热化学方程式
- 共127题
9.下列叙述与对应图式正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
15.砷(As)广泛分布于自然界,其原子结构示意图是
(1)砷位于元素周期表中( )族,其气态氢化物的稳定性比NH3 ( )(填“强”或“弱”)。
(2)砷的常见酸性氧化物有As2O3和As2O5,根据下图写出As2O5分解为As2O3的热化学方程式:( )。
(3)砷酸盐可发生如下反应:AsO


① A中盛有棕色的KI和I2的混合溶液,B中盛有无色的Na3AsO4和Na3AsO3的混合溶液,当连接开关K,并向B中滴加浓盐酸时发现灵敏电流计G的指针向右偏转。此时C2上发生的电极反应式为 ( ) 。
② 一段时间后,当电流计指针回到中间“0”位时,再向B中滴加过量浓NaOH溶液,可观察到电流计指针( )(填“不动”、“向左偏”或“向右偏”)。
正确答案
(1)
(2)
(3)① 
解析
解析已在路上飞奔,马上就到!
知识点
23.甲、乙、丙、丁四种物质转化关系如右图。已知甲是地壳中含量最高的元素组成的单质,化合物乙、丙、丁均含有第三周期一种相同元素。
(1)若乙是难溶于水的酸性氧化物。
①乙的一种重要用途是( );
②丙溶液中通入少量CO2生成丁的离子方程式是( )。
(2)若2乙(g) + 甲(g) 
①该反应的△H( )0(填“>”、“<”或“=”,下同);
②若400℃和500℃的化学平衡常数分别为K1、K2,则K1 ( ) K2。
(3)若丙是离子化合物,且阴离子含金属元素R。
①R的原子结构示意图是( );
②已知:R(s) + 

Mn(s) + O2(g) = MnO2(s) △H=-520.9 kJ·mol -1
写出R的单质与MnO2反应的热化学方程式( ) 。
正确答案
(1)①制造光导纤维或生产玻璃等(其他合理答案均给分)
(2)
(3)
解析
解析已在路上飞奔,马上就到!
知识点
31. Ⅰ.已知:4Al(s)+3O2(g) = 2Al2O3(s) △H=-2834.9KJ•mol-1
写出铝与氧化铁发生铝热反应的热化学方程式( ) 。
Ⅱ.在2L密闭容器内,800℃时反应:
(1) 写出该反应的平衡常数表达式:K= ( ); 用

(2)下列研究目的和示意图相符的是( )。
III.科学家制造出一种使用固体电解质的高效燃料电池。一个电极通入空气,另一个电极通入燃料蒸汽。其中固体电解质是掺杂了


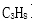
(1)电池的负极反应式为( );
(2)放电时固体电解质里的
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
回答下列问题:
(1)组成单质Z的元素在周期表中的位置是( ); R的化学式是( );
(2)E、Z的晶体类型均属于( )晶体。E、Z结构中最小的环上原子个数之比为( )。B为一元强碱,焰色反应为紫色,则B的电子式为( )。
(3)写出下列反应的化学方程式:
①单质Z与 NaOH的反应:( ),
②工业上由E制取粗Z:( ),
(4)已知A与1 mol Al反应转化为X时(所有物质均为固体),放出a kJ 热量,写出该反应的热化学方程式:( )。
(5)向A与X的混合物中加入100 mL 1mol / L盐酸恰好使混合物完全溶解,放出标准状况下的气体224 mL,在溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的混合物,能得到单质的质量为( ) 。
正确答案
(1)第三周期IVA族 ;
(2)原子 ; 2:1 ;
(3)
(4)
(5)2.8g
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析





















