- 热化学方程式
- 共127题
11.下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②向100 mL0.1 mol/L 的溴化亚铁溶液中通入0.05 mol的氯气时发生反应的离子方程式:
2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
③斜长石KAlSi3O8的氧化物形式可表示为:K2O•Al2O3•3SiO2
④酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:
IO3-+5I-+3H2O=I2+6OH-
⑤碳酸氢根离子的电离方程式可表示为:
⑥元素周期表中,从上到下,卤族元素的非金属性逐渐减弱,氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放
热19.3kJ,其热化学方程式为:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.已知2H+ + 2NO2— = NO↑ + NO2↑ + H2O。现用下图所示仪器(夹持装置已省略)及药品,检验亚硝酸钠与硫酸反应生成的气体产物。
★NO和NO2部分性质如下表所示:
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(从左向右连接):A→
→______→_______→_______;组装好仪器后,接下来进行的操作是( )
(2)打开弹簧夹,通一会儿N2,目的是( )
(3)关闭弹簧夹,打开分液漏斗活塞,滴入70%的硫酸后
①确认A中产生气体含有NO2,依据的现象是_____________________________
②确认A中产生气体含有NO,依据的现象是_____________________________
③装置E的作用是______________________________________________________
(4)如果没有装置C,对实验结论造成的影响是______________________________
(5)工业生产中氮氧化物的排放会造成环境污染,可采用如下方法处理氮氧化物:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5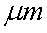
请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含离子的化学组分及其浓度如下表:
根据表中数据判断试样的pH=( )。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H20 (g) △H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g) △H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:( )。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是( ) 。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中有NOx和CO的生成及转化
① 若1mol空气含0.8molN2和0.2molO2,汽缸中的化学反应式为
1300℃时将1mol空气放在密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K=( ) 。
汽车启动后,汽缸温度越高,单位时间内NO排放量越大,其原因是 ( ) 。
②目前,在汽车尾气系统中装置催化转化器可减少CO和NOx的污染,其化学反应方程式为 ( ) 。
③ 汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO,
2CO(g)=2C(s)+O2(g)
已知该反应的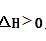
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26
根据以上叙述,回答下列问题:
(1)A与B形成的液态化合物M是曾经用过的一种火箭燃料,已知M与C的单质的摩尔质量相等,则M的结构式为( )。
(2)A和C可以形成一种液态化合物N,该化合物有氧化性。N能与M恰好完全反应,产生两种无毒又不污染环境的物质X
已知1molM与氧气反应生成X和Y放出的热量为Q1kJ,N生成1 molC单质吸热Q2kJ。M与N反应的热化学方程式 ( )。
(3)A与B还可以形成另一种非常常见气态化合物Z,则Z是 ( ) 分子(填“极性”或“非极性”)。
(4)元素C与元素D形成的多种化合物中,其中C与D按原子个数比1:1所形成的化合物的电子式为( )。
(5)六种元素中其中三种元素组成的某种盐,水溶液显碱性,是家用消毒剂的主要成分,请用离子方程式解释该盐溶液呈碱性的原因( ) 。
(6)2008年5月12日,四川发生了里氏8.0级地震,导致饮用水被污染。其中E与F形成的化合物P可用于饮用水的净化,P的水溶液能净化饮用水的原因( )。
(7)A单质与C的单质可以组成新型燃料电池,该电池在新能源开发中有重要地位,可作未来新型汽车动力的电池,若该电池以KOH为电解质溶液,写出该燃料电池的负极反应式( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.工业合成氨反应:
(1)若降低温度,会使上述平衡向生成氨的方向移动,生成每摩尔氨的反应热数值是46.2KJ/mol,则该反应的热化学方程式为( ) 。
(2)若在恒温条件下,将N2与H2按一定比例混合的气体通入一个容积为2升固定容积的密闭容器中,5分钟后反应达平衡时,n(N2)=1.2mol, n(H2)=1.2mol, n (NH3)=0.8mol,则反应速率V(N2)=( ) mol·L-1·min-1,H2的转化率=( ),平衡常数=( )。若保持容器的温度和容积不变,将上述平衡体系中的混合气体的浓度增大1倍,则平衡( )(填向左﹑向右或不移动)移动。
(3)若在恒温恒压条件下,将1 molN2与3 molH2的混合气体通入一个容积可变的容器中发生反应,达平衡后,生成a molNH3,这时N2的物质的量为( )mol,(用含a的代数式表示);若开始时只通入N2与H2 ,达平衡时生成3amolNH3,则开始时应通入N2 3mol,H2 =( )mol(平衡时NH3 的质量分数与前者相同);若开始时通入x molN2﹑6molH2 和2mol NH3,达平衡后,N2和NH3的物质的量分别为y mol和3a mol,则x=( )mol,y=( )mol(用含a的代数式表示)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析









