- 化学反应原理
- 共2396题
8.通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=206.1kJ·mol–1
正确答案
知识点
4.己知丙烷的燃烧热△H=-2215kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为
正确答案
解析
依据:C3H8(g)+5O2(g)=3CO2(g) + 4H2O(l) △H=-2215kJ·mol-1
4×18 g 2215 kJ
知识点
氨是合成硝酸.铵盐和氮肥的基本原料,回答下列问题:
25.氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的pH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
26.硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
27.由N2O和NO反应生成N2和NO2的能量变化如图所示,
正确答案
NH3•H2O
解析
有电离平衡体系:NH3•H2O
考查方向
解题思路
依据弱电解质电离平衡原理。
易错点
加入明矾对铵离子浓度的影响判断——碱与盐的反应。
正确答案
NH4NO3
解析
依据“硝酸铵加热分解可得到N2O和H2O”,直接书写配平:NH4NO3(s)
考查方向
解题思路
依据氧化还原反应中化合价“归中”原理、及平衡常数公式。
易错点
平衡常数表达式、及电子转移数。
正确答案
-139。
解析
能量过程图看出:N2O(g)+NO(g)=N2(g)+NO2(g) ,这就是生成1 mol N2的反应,故其△H=(+209 - 348)kJ·mol-1= —139 kJ·mol-1。注意:反应物断键吸热取正值(+)、生成物成键放热取负值(—)。
考查方向
解题思路
依据图示反应过程的能量变化计算。
易错点
焓变数值没有正负号。
15.在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+c(s)
正确答案
解析
A.由气体的化学计量数增大可知△S>0,由图中温度高平衡时c(CO2)小,则升高温度平衡正向移动,可知△H>0,故A错误;B.分别加入0.1molCO2和0.2molCO2,曲线I为加入0.1molCO2,曲线II为加入0.2molCO2,若平衡不移动,体系的总压强为P总(状态Ⅱ)=2P总(状态Ⅰ),但加压CO2(g)+C(s)⇌2CO(g)平衡逆向移动,为使c(CO2)相同,则加热使平衡正向移动,则体系的总压强为P总(状态Ⅱ)>2P总(状态Ⅰ),故B正确;C.状态II、状态Ⅲ的温度相同,状态II看作先加入0.1molCO2,与状态Ⅲ平衡时CO的浓度相同,再加入0.1molCO2,若平衡不移动,Ⅱ状态CO的浓度等于2倍Ⅲ,但再充入CO2,相当增大压强,平衡右移,消耗CO,则c(CO,状态Ⅱ)<2c(CO,状态Ⅲ),故C正确;D.状态I、状态Ⅲ的温度不同,温度高反应速率快,则逆反应速率为V逆(状态Ⅰ)<V逆(状态Ⅲ),故D错误;
故选BC.
考查方向
解题思路
A.由气体的化学计量数增大可知△S,由图中温度高平衡时c(CO2)小可知△H;B.分别加入0.1molCO2和0.2molCO2,曲线I为加入0.1molCO2,曲线II为加入0.2molCO2,加压CO2(g)+C(s)⇌2CO(g)平衡逆向移动;C.状态II、状态Ⅲ的温度相同,状态II看作先加入0.1molCO2,与状态Ⅲ平衡时CO的浓度相同,再加入0.1molCO2,若平衡不移动,Ⅱ状态CO的浓度等于2倍Ⅲ,但再充入CO2,相当增大压强,平衡右移,消耗CO;D.状态I、状态Ⅲ的温度不同,温度高反应速率快.
易错点
本题考查化学平衡及平衡的建立,为高频考点,把握平衡移动的影响因素、图象分析为解答的关键,选项BC为解答的难点,题目难度中等.
知识点
10.(15分)催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g)
CO2(g)+ H2(g)
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K= ;反应II的ΔH2= kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有 。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是 。
(4)在右图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图。
(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在极,该电极反应式是 。
正确答案
(1)
(2)CD
(3)表中数据表明此时反应未达到平衡,不同的催化剂对反应Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响。
(4)
(5)阴 CO2+6H++6e-==CH3OH+H2O
知识点
6.油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:
C37H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8104kJ,油酸甘油酯的燃烧热 为
正确答案
知识点
8.通过以下反应均可获取H2。下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=206.1kJ·mol–1
正确答案
解析
A.反应①中光能转化为化学能,错误。B.反应②为吸热反应,错误。C.反应③使用催化剂,ΔH3不变。错误。D.由反应情况看反应①是太阳能转化为电能,反应②是吸热反应焓变不随催化剂而改变,ABC说法都是错误的;根据盖斯定律,③-②得CH4(g)=C(s)+2H2(g)其焓变ΔH=206.1-131.3=74.8kJ·mol–1。D选项正确。
考查方向
解题思路
方程式怎么相加减,ΔH就怎么相加减。
易错点
不会应用盖斯定律进行反应热的简单计算。
知识点
height
正确答案
institution
正确答案
10.煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s) + CO(g)
CaSO4(s) + 4CO(g)
假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
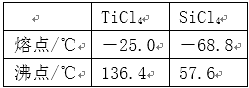
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生。
2Fe3++Fe=3Fe2+
2TiO2+(无色) +Fe+4H+=2Ti3+(紫色) +Fe2++2H2O
Ti3+(紫色) +Fe3++H2O=TiO2+(无色) +Fe2++2H+
加入铁屑的作用是____________。
(2)在②→③工艺中需要控制条件以形成TiO2·n H2O溶胶,该分散质颗粒直径大小在_______范围。
(3)若把③中制得的固体TiO2·n H2O用酸清洗除去其中的Fe (OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe (OH)3+3H+
(4)已知:TiO2 (s) +2 Cl2 (g)=TiCl4(l) +O2(g) △H=+140KJ·mol-1
2C(s) +O2(g)=2CO(g) △H=-221KJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:_____________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是_____________(只要求写出一项)。
(6)依据右表信息,要精制含少量SiCl4杂质的TiCl4 ,可采用_____________方法。
正确答案
见解析。
解析
(1)根据题意给出方程式分析铁屑的作用就是作为还原剂的,即:将Fe3+还原为Fe2+,另外浸出液显紫色,说明含有Ti3+,防止Ti3+被Fe3+氧化成TiO2+。参考答案中“生成Ti3+保护Fe2+不被氧化。”有点让人费解,能不能说成“防止Ti3+被Fe3+氧化成TiO2+”或者说“将TiO2+还原成Ti3+”。
(2)形成TiO2·n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10- 7m(或1nm—100nm);
(3)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH—)=2.79×10—39,25℃时,c(H+)×c(OH—)=Kw=1×10—14;反应Fe (OH)3+3H+
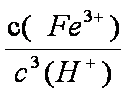
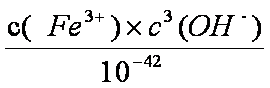

(4)涉及盖斯定律计算,比较常规,按要求写出方程式相加即可得出答案:
TiO2(s)+ 2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g) △H=—81KJ·mol-1
(5)依据绿色化学理念,该工艺流程中存在的不足之处产生了废气,废液,废渣等。
(6)右表信息可以看出,SiCl4,TiCl4两者的沸点相差较大,要精制含少量SiCl4杂质的TiCl4可用蒸馏(或分馏)等方法。
知识点
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中。然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固。由此可见
正确答案
解析
略
知识点
下表列出了3种燃煤烟气脱硫方法的原理。
(1) 方法Ⅰ中氨水吸收燃煤烟气中
能提高燃煤烟气中
a增大氨水浓度 b升高反应温度
c使燃煤烟气与氨水充分接触 d通入空气使
采用方法Ⅰ脱硫,并不需要先出去燃煤烟气中大量的
(2) 方法Ⅱ重要发生了下列反应:







(3) 方法Ⅲ中用惰性电极电解
正确答案
(1)a c HCO3- +SO2= CO2+HSO3-
(2)S(g)+O2(g) = SO2 (g) ⊿H=-574.0kJ·mol-1
(3)O2、 SO2
解析
略
知识点
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时:
①HF(aq) + OH—(aq) == F—(aq) + H2O(l) △H = - 67.7 kJ•mol-1
②H+ (aq) + OH—(aq) == H2O(l) △H = - 57.3 kJ•mol-1
在20 mL 0. 1 mol•L-1氢氟酸中加入V mL 0. 1 mol•L-1NaOH溶液。下列有关说法正确的是
正确答案
解析
本题考查盖斯定律的应用、酸碱中和反应及溶液中离子浓度大小的比较,旨在考查考生对所学生所学知识的整合及应用能力。。
根据盖斯定律,将①式减去②式经整理可得:
HF(aq) 
由反应①放热比反应②多,亦可判断氢氟酸的电离为放热,本题要求突破“弱电解质电离都是吸热”的思维定势。故A选项错误。
当V=20时,两者恰好完全反应生成NaF,溶液中存在质子守恒关系:
c(OH-) = c(HF)+c(H+)
质子守恒式有两种方法推得:
(1)直接推得:因F-水解结合H2O电离出的H+生成HF并提供与HF等量的OH—,且H2O本身电离出H+和OH—;
(2)由NaF溶液的电荷守恒式和物料守恒式求得:NaF溶液的电荷守恒式:
c(Na+) + c(H+) = c(F-) + c(OH-)
NaF溶液的物料守恒式:c(Na+) = c(HF) + c(F-)
消去2个式子中的c(Na+)可得出其质子守恒式 。
因F-水解,故溶液中存在:c(F-)<c(Na+) = 0.05 mol•L-1 ,故B选项正确,C选项错误。
D选项:溶液中离子浓度的大小取决于V的大小,离子浓度大小关系可能为c(F-)>c(H+)>c(Na+)>c(OH-)或c(F-)>c(Na+)>c(H+)>c(OH-)或c(Na+) = c(F-)>c(OH-) = c(H+)或c(Na+)>c(F-)>c(OH-)>c(H+),故D选项错误。
为了更清晰明确D选项的问题,不妨进行如下分析:
影响溶液中各离子浓度的因素有2个:(1)离子的物质的量;(2)溶液的体积。
根据这2个因素的影响,可绘制出下图:
根据上图,并结合离子的变化,可以得到下表离子浓度的大小比较:
知识点
已知C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1,2C(s)+O2(g)=2CO(g),ΔH=-220kJ·mol-1,H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为( )
正确答案
解析
略
知识点
扫码查看完整答案与解析