- 卤素原子结构及其性质的比较
- 共92题
4.下列说法正确的是()
正确答案
解析
A.液氨汽化时要吸收大量的热,使温度降低,可用作制冷剂,故A正确;B.常温下能用铝制容器盛放浓硝酸和浓硫酸,是因为反应生成了致密的氧化膜阻止进一步反应,故B错误;C.明矾溶于水生成胶状物可吸附悬浮于水中的杂质,不能除掉可溶性杂质和细菌等,不能起消毒杀菌的作用,故C错误.D.能置换出氧化铁中的铁,发生铝热反应,可以用来焊接钢轨,钢铁工业炼铁是利用还原法得到,一氧化碳还原氧化铁得到金属铁,故D错误;
故选A
考查方向
解题思路
A.液氨汽化时要吸收大量的热,使温度降低;B.常温下能用铝制容器盛放浓硝酸和浓硫酸,是因为反应生成了致密的氧化膜阻止进一步反应;C.明矾可用于净水,是因为明矾溶于水生成胶状物可吸附悬浮于水中的杂质;D.铝能置换出氧化铁中的铁,发生铝热反应,钢铁工业炼铁是利用还原法得到,一氧化碳还原氧化铁得到金属铁;
易错点
化学反应原理及化学方程式掌握不熟练
知识点
13.下列设计的实验方案能达到实验目的是()
正确答案
解析
A.新制Cu(OH)2悬浊液常用来检验醛基,应加碘水看是否变蓝,故A错误; B.碳酸钠能除掉氯化钙,过量的碳酸钠可用盐酸除去,故B正确;C.试管中先加入无水乙醇,再依次加入一定量浓硫酸、适量冰醋酸,然后加热制取乙酸乙酯,最后用饱和碳酸钠吸收,故C错误;D.炭与浓硫酸反应生成二氧化硫,同样能生成白色沉淀,故D错误.
故选B
考查方向
解题思路
A.新制Cu(OH)2悬浊液常用来检验醛基; B.碳酸钠能除掉氯化钙;C.浓硫酸在乙醇之后加入;D.炭与浓硫酸反应生成二氧化硫.
易错点
忽略实验步骤的先后顺序,干扰气体的排除
知识点
甲苯(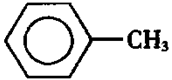
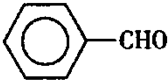
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶
中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和
2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧
化氢,在此温度下搅拌反应3小时。
16.装置a的名称是_________,主要作用是___________。
三颈瓶中发生反应的化学方程式为_________________,
此反应的原子利用率理论上可达______________。
17.经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是________________。
18.反应完毕后,反应混合液经过自然冷却至室温时,还应经过________、________(填操作名称)等操作,才能得到苯甲醛粗产品。
19.实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯 甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是_______(按步骤顺序填字母)。
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加人盐酸调节pH=2
d.与适量碳酸氢钠溶液混合震荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000moL/KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为________。下列情况会使测定结果偏低的是__________(填字母)。
a.滴定时俯视读取耗碱量
b.KOH标准液长时间接触空气
c.配置KOH标准液时仰视定容
d.将酚酞指示剂换为甲基橙溶液
正确答案
球形冷凝管 冷凝回流,防止甲苯的挥发而降低产品产率
解析
因反应需持续加热,又为防有机物挥发,形球形冷凝管起冷凝回流,防止甲苯的挥发而降低产品产率。因为是用甲苯制苯甲醛,所以需用H2O2作氧化剂在催化剂作用下将其氧化,故化学方程式为: 
考查方向
有机化学实验与原理
解题思路
认真审题,充分把握题干上的信息,理清实验的操作及原理。
易错点
滴定误差分析、化学计算
正确答案
H2O2在较高温度时分解速度加快,使实际参加反应的H2O2减少,影响产量
解析
因为H2O2热不稳定性,受热易发生分解,因此随温度升高时,分解率增大,产率随之降低。
考查方向
解题思路
认真审题,充分把握题干上的信息,理清实验的操作及原理。
易错点
滴定误差分析、化学计算
正确答案
过滤 蒸馏
解析
反应完毕后,反应体系中有除苯甲醛外还含有固体催化剂、醋酸、甲苯等,先进行过滤,再利用各组分的沸点不同,进行蒸馏分离。
考查方向
解题思路
认真审题,充分把握题干上的信息,理清实验的操作及原理。
易错点
滴定误差分析、化学计算
正确答案
①dacb ②87.84﹪ ad
解析
①将苯甲醛中混有的苯甲酸分离,可以先在混合体系中加入碳酸氢钠,将苯甲酸转化成可溶于水的盐,再进行分液,在水相中加入酸调节溶液PH重新制得苯甲酸,因苯甲酸在水中溶解度不大,大部分结晶析出,再过滤分离。
②滴定过程中苯甲酸与KOH按1:1反应:滴定过程中消耗n(KOH)=1.8

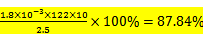
考查方向
解题思路
认真审题,充分把握题干上的信息,理清实验的操作及原理。
易错点
滴定误差分析、化学计算
7.下列指定反应的离子方程式正确的是()
正确答案
解析
A.正确;B.Na2SiO3是强电解质,在书写离子方程式的时候应拆开,错误;C.此时为AgCl悬浊液,悬浊液在离子方程式不能拆开,错误;D.Al3+只有在强碱中才生成AlO2-,此离子方程式为Al3++3NH3.H2O==Al(OH)3↓ +3NH4+,错误。
考查方向
解题思路
注重物质在离子方程式改写问题
易错点
反应原理理解不清晰,物质在离子方程式改写
知识点
14.已知:乙二酸(H2C2O4)是二元弱酸。向10 mL 0.1 mol·L-1 Na2C2O4溶液中逐滴加入a mL 0.1 mol·L-1盐酸(混合前后溶液体积变化可忽略
正确答案
解析
A.当a=5时反应得到等物质的量浓度的Na2C2O4溶液、NaHC2O4溶液、NaCl溶液的混合溶液,溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(Cl-)+2c(C2O42-),c(H2C2O4)≠c(HC2O4-)+c(Cl-),故A错误;B.当a=10时反应得到NaHC2O4溶液、NaCl溶液的混合溶液,溶液中电荷守恒为:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(Cl-)+2c(C2O42-),物料守恒2c(HC2O4-)+2c(H2C2O4)+2c(C2O42-)=c(Na+),带入计算得到c(Cl-)+c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4),故B正确;C.当a=15时反应得到H2C2O4溶液、NaHC2O4溶液、NaCl溶液的混合溶液,溶液中存在物料守恒,c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.04mol•L-1,故C正确;D.当a=20时反应得到H2C2O4溶液、NaCl溶液的混合溶液,且氯化钠是草酸的2倍,草酸是二元弱酸分步电离c(Na+)>c(H+),故D错误。
故选BC
考查方向
解题思路
A.当a=5mL时,溶液中溶质为等物质的量浓度的Na2C2O4、NaCl、NaHC2O4,溶液中存在电荷守恒,根据电荷守恒判断;B.当a=10mL时,二者恰好完全反应生成等物质的量浓度的NaHC2O4、NaCl,溶液中存在电荷守恒、物料守恒,根据电荷守恒和物料守恒判断;C.当a=15时,反应得到H2C2O4溶液、NaHC2O4溶液、NaCl溶液的混合溶液,溶液中存在物料守恒;D.当a=20时,反应得到H2C2O4、NaCl的混合溶液,且氯化钠浓度是草酸的2倍.
易错点
计算错误
知识点
扫码查看完整答案与解析