- 化学科学特点
- 共348题
1.下列表述符合化学事实的是()
正确答案
解析
A.任何物质都由化学物质组成,没有不含任何化学物质的物质,A错误;
B.“洁厕灵”与“漂白精”不能混用,因为二者混合后能产生一种有毒的气体,其反应的化学方程式为:NaClO+2HCl═NaCl+Cl2↑+H2O,B错误;
C.根据“绿色化学”的特征:反应物中原子全部转化为欲制得的产物,即原子的利用率为100%,即生成物质全部是目标产物,C正确;
D.新核素可能只是原子核内中子数的变化,质子数不变,不意味着新元素的合成,D错误。
故选C。
考查方向
解题思路
A.任何物质都由化学物质组成,没有不含任何化学物质的物质;
B.“洁厕灵”与“漂白精”不能混用,因为二者混合后能产生一种有毒的气体;
C.根据“绿色化学”的特征:反应物中原子全部转化为欲制得的产物,即原子的利用率为100%;
D.新核素可能只是原子核内中子数的变化,质子数不变。
易错点
解题的易错点是D中新核素不一定就是新元素,质子数不同元素种类不同。
知识点
7.化学与人类社会的生产、生活有着密切联系。下列叙述中正确的是( )
正确答案
解析
A、铜的活泼性小于H,所以铜制品不能发生析氢腐蚀。
B、铝制品由于表面有致密的氧化膜,可以稳定存在于空气中。
C、苹果放在空气中久置变黄是发生了氧化还原反应,而纸张久置变黄是SO2的漂白属于短暂漂白,原理不同。
D、高纯度的Si对光有很好的折射和全反射作用,可以制成光电池将光能直接转化为电能。
考查方向
解题思路
A、铜的活泼性小于H。
B、铝制品表面与氧气反应生成氧化铝。
C、苹果放在空气中久置变黄是发生了氧化还原反应。
D、高纯度的Si可以制成光电池将光能直接转化为电能。
易错点
铜的活泼性小于H,所以铜制品不能发生析氢腐蚀。
知识点
7.中华民族有着光辉灿烂的发明创造史,下列古代的技术应用中不涉及化学反应的是( )
正确答案
解析
A. 制陶瓷的原料是粘土,发生化学变化生成硅酸盐产品;
B. 湿法炼铜,由由CuSO4·5H2O→Cu,有新物质生成,属于化学反应;
C. 海水晒盐,没有新物质生成,不涉及化学反应。
D. 粮食酿酒,有新物质酒精生成,涉及化学反应。
考查方向
解题思路
没有新物质生成,不涉及化学反应;有新物质生成,涉及化学反应。
易错点
烧结粘土制陶瓷
知识点
7. 化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法不正确的是
正确答案
解析
A.油条的制作口诀是“一碱、二矾、三钱盐”,其中的“碱”是纯碱。
B.黑火药的最优化配方是“一硫二硝三木炭”, 其中的“硝”是硝酸钾。
C.过滤操作要领是“一贴二低三靠”,其中“贴”是指滤纸紧贴漏斗的内壁
D.“固体需匙或纸槽,一送二竖三弹弹;块固还是镊子好,一横二放三慢竖“。前一个固体一般指粉末状固体。
考查方向
解题思路
A.碱,矾,盐就是食用碱,明矾,食盐。
B.黑火药的一般配方是:硫磺、硝酸钾、碳粉。
C.过滤操作要领是一贴二低三靠。一贴:滤纸必须紧贴漏斗内壁(记住要保持湿的状态),二低:滤纸边缘必须低于漏斗口,而且过滤过程中,液面必须低于滤纸边缘,三靠:玻璃棒必须靠着滤纸,漏斗必须靠着容器壁,液体必须靠着玻璃棒缓缓流下。
D. “固体需匙或纸槽,一送二竖三弹弹;块固还是镊子好,一横二放三慢竖“。前一个固体一般指粉末状或者块状固体。
易错点
1、对化学物质俗称的理解。
2、实验基本操作的要领。
知识点
1.化学与环境、材料、信息、能源关系密切,下列说法正确的是
正确答案
解析
A.绿色化学是对环境友好型化学,要求原料物质中所有的原子完全被利用且全部转入期望的产品中,原子的利用率100%,无污染、无公害的化学,核心是利用化学原理从源头消灭污染,故A错误;
B.氢能、核能、太阳能等是清洁能源,可减少污染,使用新型电动汽车,可减少城市机动车尾气排放,故B正确;
C.PM2.5是指大气中直径小于或等于2.5um的颗粒物,PM2.5的直径大于胶体直径,所以不属于胶体,故C错误;
D.Si原子最外层电子为4个,既难得电子,也难失去电子,可做为半导体,可用于制造硅芯片,是计算机芯片的成分,故D错误;
考查方向
解题思路
本题考查化学与环境、材料、信息、能源关系密切相关的知识,为高频考点,侧重于基础知识的综合理解和运用的考查,注意绿色化学的核心高频考点。
A.绿色化学是无污染、无公害的化学,核心是利用化学原理从源头消灭污染;
B.开发高效氢能、太阳能等新型电动汽车,可以减少污染性气体的排放,改善空气质量;
C.胶体的微粒直径在1-100nm之间;
D.Si可做为半导体,可以有很多特殊的功能,二氧化硅是光导纤维的主要成分;
易错点
形成胶体的微粒直径在1-100nm之间。
知识点
7.在刚刚过去的一年中,发生了许多与化学相关的大事件。下列说法正确的是( )
正确答案
解析
根据绿色化学的核心是要利用化学原理从源头上减少和消除工业生产对环境的污染进行解答;
考查方向
本题主要考查了绿色化学;钠的化学性质;乙炔气体的实验室制取。
解题思路
A、绿色化学的核心是要利用化学原理从源头上减少和消除工业生产对环境的污染,故A正确;
B、金属钠、电石,用泡沫灭火器灭火时,要产生可燃性气体氢气和乙炔。
C、青蒿素属于烃的衍生物不属于烃类物质。
D、某品牌化妆品在广告中反复强调产品中不含任何化学成分,化学物质就是一种化学成分。
易错点
电石与水反应生成乙炔气体。
知识点
1.化学与科学、技术、社会、环境密切相关,下列叙述正确的是()
正确答案
解析
A、裂解是深度裂化,所以石油裂化的目的是为了提高汽油等轻质油的产量,裂解的目的是为了获得乙烯、丙烯等短链烃,错误;
B、目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,电子迁移速率快,所以可以取代硅用于制造更好的晶体管,正确;
C、催化剂只能降低反应的活化能,但不能改变平衡,所以不能提高反应的转化率,错误;
D、近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的,乙醇使蛋白质变性并非是将病毒氧化,高锰酸钾溶液和双氧水的消毒原理相同,都是利用二者的强氧化性;双氧水具有较强的氧化性,稀溶液能用于皮肤的消毒;次氯酸钠溶液中通入少量二氧化硫,发生氧化还原反应生成硫酸根和氯离子。
考查方向
解题思路
A、裂解是深度裂化,裂解的目的是为了获得乙烯、丙烯等短链烃;
B、单原子层锗,其电子迁移率是硅的10倍;
C、催化剂不能改变平衡;
D、乙醇使蛋白质变性,高锰酸钾溶液和双氧水具有强氧化性;
易错点
1. 裂解的含义及目的
2.各种消毒剂消毒的原理。
知识点
目前“低碳减排”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。
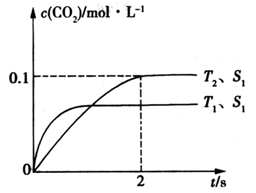
23.汽车尾气净化的主要原理为2NO(g)+2CO(g)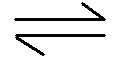
①该反应的△H_____________0(填“>”或“<”)。
②在T2温度下,0-2s内的平均反应速率v(N2) =____________mol/(L·s)。
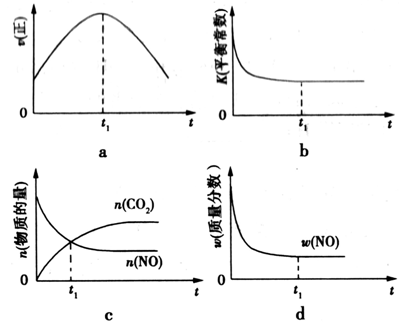
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是_______________(填代号)。
24.直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
2NO2(g)=N2O4(g) △H=-56.9kJ·mol-1
写出CH4(g)催化还原N2O4(g)的热化学方程式:
___________________________________。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2(g)和H2O(g)为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应为_________________。
③常温下0. 1 mol·L-1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=______________mol·L-1(填写最终计算结果)。
正确答案
①<
②0.025
③bd
解析
③a.反应达到平衡状态时,各物质的反应速率不再变化,故错误。
b.该反应在绝热、恒容的密闭体系中进行,相当于升高温度,当温度不变时,化学平衡常数不变,故正确。
c.二氧化碳和一氧化氮的物质的量相等时,该反应不一定达到平衡状态,故错误。
d.反应达到平衡状态时,各物质的质量分数不再发生变化,故正确。
考查方向
解题思路
(1)T1>T2,先拐先平温度高,温度越高,二氧化碳浓度越低,所以该反应是△H<0。具图分析先拐先平,定一议二。
(2)②+①得到CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g) △H=-810.1 kJ·mol-1,据此计算反应的焓变;电解反应中阴极上发生得电子的还原反应,根据反应原理来回答书写;
(3)电离常数K=
正确答案
①CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g) △H=-810.1 kJ·mol-1
②CO2+2H++2e-=HCOOH ③10-7
解析
①将第一个方程式减第二个方程式得:
CH4(g)+N2O4(g)
②催化剂b表面上二氧化碳得电子和氢离子反应生成甲酸,所以发生的电极反应式为:
CO2+2H++2e-
考查方向
解题思路
(1)T1>T2,先拐先平温度高,温度越高,二氧化碳浓度越低,所以该反应是△H<0。具图分析先拐先平,定一议二。
(2)②+①得到CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g) △H=-810.1 kJ·mol-1,据此计算反应的焓变;电解反应中阴极上发生得电子的还原反应,根据反应原理来回答书写;
(3)电离常数K=
6.2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行.能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是
正确答案
解析
A.地沟油、矿物油均能燃烧,不能区别,故A错误;
B.地沟油、矿物油均为混合物,没有固定沸点,不能区别,故B错误;
C.地沟油、矿物油均不溶于水,且密度均比水小,不能区别,故C错误;
D.加入足量氢氧化钠溶液共热,不分层的是地沟油,分层的为矿物油,现象不同,能区别,故D正确;
故选D.
考查方向
解题思路
A、地沟油属于油脂,含有C、H、O三种元素,矿物油中含有C、H元素,均可燃烧,错误;
B、矿物油为混合物,没有恒定的溶沸点,错误;
C、地沟油与矿物油的密度均小于水,都会浮在水面上,错误;
D、地沟油的主要成分为油脂,与NaOH可发生水解,矿物油不能与其反应,会浮在液面上方,正确;所以答案为D。
易错点
1、地沟油属于油脂,矿物油属于烃。
2、油脂与NaOH可发生水解,矿物油属于烃不能发生水解。
知识点
7.化学是材料科学发展的基础。下列说法正确的是
正确答案
解析
A.氧化铝纳米材料属于属于纯净物,胶体属于混合物,A错误;
B.聚乙炔是高分子材料,聚合物经溴或碘掺杂之后,导电性会提高到金属水平,可导电,B正确;
C.钢化玻璃、防弹玻璃均属于硅酸盐材料,有机玻璃是聚甲基丙烯酸甲脂,是有机物,C错误;
D.刚玉的成分是氧化铝而不是MgO,氧化铝熔点很高,可以作耐火材料,D错误。
故选B。
考查方向
解题思路
A.氧化铝纳米材料属于属于纯净物,胶体属于混合物;
B.聚乙炔是高分子材料,聚合物经溴或碘掺杂之后,导电性会提高到金属水平,可导电;
C.钢化玻璃、防弹玻璃均属于硅酸盐材料,有机玻璃是聚甲基丙烯酸甲脂,是有机物;
D.刚玉的成分是氧化铝而不是MgO,氧化铝熔点很高,可以作耐火材料。
易错点
本题考查了硅及其化合物的用途,明确物质的成分及其性质是解本题关键,了解常见元素化合物性质,性质决定用途,题目难度不大。
知识点
扫码查看完整答案与解析