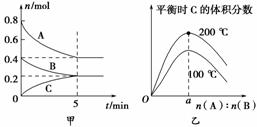- 化学反应速率与化学平衡图象的综合应用
- 共80题
在2 L的密闭容器中发生反应xA(g)+yB(g)
正确答案
解析
略
知识点
运用化学反应原理研究氮、氯等单质及其化合物的反应有重要意义。
(1)科学家研究在一定条件下通过下列反应制备NH3:
①在其他条件相同时,反应中NH3的体积分数(a)在不同温度下随反应时间(t)的变化如图。该反应的平衡常数表达式K=________,该反应中的ΔH________0(填“>”“<”或“=”)。
②某温度下,在2L容积不变的密闭容器中加入1molN2和6molH2O(l)发生反应,转化率随时间(f)变化如图。15-20min内,v(NH3)=________。若其他
(2) 25℃时,某同学将O.lmol


(3) 25℃时,向O.lmol




正确答案
(1)①
(2)>;>
(3)白色沉淀逐渐变成红褐色;Mg2++2NH3·H2O=Mg(OH)2↓+2NH4+;2Fe3+(aq)+3Mg(OH)2(s)=2Fe(OH)3(s)+3Mg2+(aq)
解析
略。
知识点
在恒容条件下发生反应
改变其他反应条件,在Ⅰ、Ⅱ阶段体系中各物质浓度随时间变化的曲线如下图所示,下列说法中正确的是
正确答案
解析
略
知识点
Ⅰ,甲醇是一种新型的能源。
(1)合成气(组成为H2和CO)是生产甲醇的重要原料,请写出由焦炭和水在高温下制取合成气的化学方程式 。
(2)已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为l L的密闭容器中,由CO和H2合成甲醇。在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
下列说法正确的是 (填序号)
A,温度为T1时,从反应开始到平衡,生成甲醇的平均速率为
v(CH3OH) =(mol·L-1·min-1)
B,该反应在T1时的平衡常数比T2时的大
C,该反应为吸热反应
D,处于A点的反应体系从T1变到T2,达到平衡时减小
(4)在T1温度时,将1 mol CO和2mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO转化率为a,则容器内的压强与起始压强之比为 ;
(5)在直接以甲醇为燃料的电池中,电解质溶液为碱性,负极的反应式为 ;假设原电解质为NaOH,且电池工作一段时间后溶质只有Na2CO3,此时溶液中各离子浓度大小关系为
Ⅱ,已知Ksp(AgCl)=1.56×10-10 ,Ksp(AgBr)=7.7×10-13 ,Ksp(Ag2CrO4)=9×10-11。某溶液中含有C1-, Br-和CrO42-,浓度均为0.010mo1·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 。
正确答案
答案:
Ⅰ(1)C+H2O
(2)CH3OH(l)+O2(g)= CO(g)+2H2O(l)H=-443.5kJ·mol-1
(3)AB
(4)1-
(5)CH3OH-6e-+8OH-=== CO32-+6H2O c(Na+)> c(CO32-)> c(OH-)>c(HCO3-)> c(H+)
Ⅱ Br-、C1-、CrO42-
解析
略
知识点
下列图示与对应的叙述相符的是
正确答案
解析
略
知识点
扫码查看完整答案与解析