- 性质实验方案的设计
- 共28题
hibernation
正确答案
heavily
正确答案
25.为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用的试剂:KSCN溶液、KMnO4溶液、氯水。
(1)请完成下表:
【实验结论】Fe的氧化产物为Fe2+和Fe3+
Ⅱ.AgNO3的热稳定性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束后,试管中残留固体为黑色。
(2)装置B的作用是___________。
(3)经小组讨论并验证该无色气体为O2,其
(4)【查阅资料】Ag2O和粉末状的A

【提出设想】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O。
【实验验证】该小组为验证上述设想,分别取少量黑色固体放入试管中,进行了如下实验。
【实验评价】根据上述实验,不能确定固体产物成分的实验是___________(填实验编号)。
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的产物有___________。
正确答案
(1)
①溶液呈红色
②K2[Fe(CN)6]溶液
③产生蓝色沉淀
(2)防倒吸
(3)用带火星的木条伸入集气瓶内,木条复燃,证明无色气体为O2
(4)① b ②Ag、NO2、O2
解析
解析已在路上飞奔,马上就到!
知识点
29.某校化学小组的同学开展测定

(1)甲同学用图1所示装置,把Xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是( )。
(2)乙同学用图2装置测定CO2的质量,该装置存在明显缺陷,从而导致实验误差,请你分析其中使测定结果可能偏大的主要原因 ( );使测定结果可能偏小的主要原因( ) 。(上述偏大、偏小的原因各写一条)
(3)丙同学用图3代替图1中的发生、收集装置,甲、乙两试管各有两根导管,用耐酸橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.甲、乙、丙、丁四位同学在探究“碱溶液与酚酞作用”的实验时,发现了一个意外现象:氢氧化钠溶液滴人酚酞试液,溶液变成了红色,一会儿红色就消失了。
[猜想]
甲:可能是酚酞变质造成的;
乙:可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
丙:可能是酚酞与空气中的氧气反应,使红色消失;
丁:可能与氢氧化钠溶液质量分数大小有关。
[理论分析]
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是:____________。
(2)丙同学认为乙同学的猜想也不正确,他的理由是_______________。
[实验设计]
(3)为证实丙同学的猜想,还需做如下实验,请完成下表:
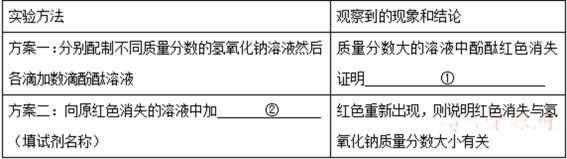
(4)通过以上实验,四位同学看到:溶液先变成红色,一会儿红色仍然消失。因此酚酞红色褪去与氧气无关。若丁同学的猜想正确,设计如下实验证明并完成有关问题:
正确答案
(1)若酚酞变质,遇NaOH溶液就不会显红色。
(2)因为NaOH与空气中的CO2反应后的产物是Na2CO3,溶液仍然呈碱性。
(3)① 除去溶液的氧气 ② 利用植物油隔绝空气
(4)① 红色消失与氢氧化钠的质量分数大小有关 ② 水
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析