- 定量实验与探究实验
- 共68题
16.过氧化氢是用途很广的绿色氧化剂,它的水溶液俗称双氧水,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:__________________________
(2)Na2O2,K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。则上述最适合的过氧化物是?
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛溶液依次加入到质量分数为30%﹣70%的过氧化氢溶液中,则该反应的化学方程式为______________。
过氧化氢比理论用量稍多,其目的是____________。
反应温度最好控制在30﹣70℃,温度不易过高,其主要原因是___________。
(4)如图1是硼氢化钠一过氧化氢燃料电池示意图.该电池工作时,正极附近溶液的pH___(填“增大”、“减小”或“不变”)
(5)Na2CO3.xH2O2可消毒、漂白.现称取100g的Na2CO3.xH2O2晶体加热,实验结果如图2所示,则该晶体的组成为_____________
正确答案
(1)H2O2+2H++2Fe2+═2Fe3++2H2O
(2)BaO2
(3)Ca(OH)2+2HCHO+2H2O2═Ca(HCOO)2+4H2O;使甲醛充分氧化,提高甲醛的利用率和产品纯度
(4)增大
(5)Na2CO3•1.5H2O2
解析
解析已在路上飞奔,马上就到!
知识点
19. ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用图1所示装置模拟工业制取并收集ClO2。
(1)A装置电动搅拌棒的作用是 。A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、 。
(2)B装置必须放在冰水浴中,其原因是 。
(3)反应后在装置C中可得NaClO2溶液。
已知(1)NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl;
(2)NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①减压,55℃蒸发结晶;
② ;
③ ;
④低于60℃干燥;得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL(已知2 Na2S2O3 + I2 =Na2S4O6 + 2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有: 。
②滴定过程中进行三次平行测定的原因是 。
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 。(填“偏高”、“偏低”或“不变” )
正确答案
(1)反应时搅拌,增大反应物的接触面积,加快反应速率
(2)温度计 使ClO2充分冷凝,减少挥发
(3)②趁热过滤 ③用38℃~60℃热水洗涤
(4)
① 100 mL 容量瓶、胶头滴管
②取平均值,减少计算误差
③偏高
解析
解析已在路上飞奔,马上就到!
知识点
25. 某化学研究小组为测定Na2O2样品(仅含Na2O杂质)的纯度,设计了两种实验方案进行探究。
[实验一] 取样品0. 100 g,用右图所示实验装置进行测定。(夹持装置省略)
(1)检查装置A气密性的方法是( ) 。
(2)若在实验过程中共产生气体11.20 mL(已折算成标准状况),则样品中Na2O2的纯度为( )。
[实验二] 样品溶于水后用盐酸滴定
(3)取一定量样品溶于水并配制成250 mL溶液,配制时,所用到的玻璃仪器除了烧杯和玻璃棒外,还需用到( )。
(4)取上述所配溶液各25.00 mL,用一定浓度的标准盐酸滴定,平行实验记录如下表:
由表中数据可知,标准盐酸体积的平均值为( )mL。若滴定前用上述所配溶液润洗锥形瓶,对实验测定结果产生的影响是( )(填“偏高”、“偏低”或“无影响”)。
[实验分析] 实验结果对比分析
(5)小组同学对比两个实验发现,实验一测得的Na2O2样品的纯度比理论值明显偏小。经过分析,小组同学认为,明显偏差不是由操作失误和装置缺陷引起的,可能是反应原理上的原因。查阅资料发现:Na2O2与水反应产生的H2O2未完全分解。
①写出Na2O2与水生成H2O2的化学方程式( )。
②若将实验一稍加改进,就能使测定结果接近理论值,写出改进方案:( )。
正确答案
(1)夹紧止水夹,向分液漏斗中加水,旋开活塞,一段时间后,若水不能顺利流下,证明气密性良好(其他合理答案均给分)。 (2分)
(2)78.0% (2分)
(3)250 mL容量瓶、胶头滴管 (2分)
(4)25.00 (2分);偏低 (2分)
(5)①
②反应前向

解析
解析已在路上飞奔,马上就到!
知识点
13.下列有关实验说法中,错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
17. (12分)中和滴定实验:
⑴ 取体积相同(25mL)的两份






⑵ 某烧碱样品含少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作
A. 在250mL的容量瓶中定容配成250mL烧碱溶液
B. 用移液管移取25mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙Ks5u
C. 在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D. 将物质的量浓度为C的标准硫酸溶液装入酸式滴定管,调节液面,
记下开始读数为V1
E. 在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
①正确操作步骤的顺序是(用字母填写)( ) →( ) →( )→ D → ( ) 。
②滴定前或滴定后读数时应注意( ) 。
③E中在锥形瓶下垫一张白纸的作用是( )。
④D步骤中液面应调节到( ),尖嘴部分应( ) 。
⑤滴定终点时颜色变化是 ( ) 。
⑥若酸式滴定管不用标准硫酸润洗,在其它操作均正确的前提下,会使测定结果
(指烧碱的纯度)( )(指偏高、低或不变)
⑦该烧碱样品纯度的计算式为 ( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
29.茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案测定某品牌茶叶中钙元素的质量分数,并检验铁元素的存在(已知CaC2O4为白色沉淀物质)。首先取200 g茶叶样品焙烧得灰粉后进行如下操作:
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的( ) 。
(2)写出从滤液A→沉淀D的离子反应方程式________________________________。
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试判断沉淀D已经洗涤干净的方法是( ) 。
(4)用

现将滤液C稀释至500 mL,再取其中的25.00 mL溶液,用硫酸酸化后,用0.100 0 mol·L-1的

①此步操作过程中需要用到下列哪些仪器(填写序号)______;
②达到滴定终点时,溶液的颜色变化是______;
③滴定到终点,静置后,如下图方法读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将______(填“偏高”“偏低”或“无影响”)。
(5)原茶叶中钙元素的质量分数为______。
(6)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及实验现象是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
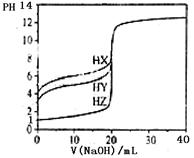
10.25℃时,用浓度为0.1000 mol/L的NaOH溶液滴定20.00 mL浓度均为0.1000 mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是________________________。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是________;
A.Mg2+
B.Fe2+
C.Al3+
D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
回答下列问题:
①操作I的名称是________,操作II的名称是________。
②写出在空气中煅烧FeCO3的化学方程式________;
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定
(5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O)。
a. 称取2.850g绿矾(FeSO4·7H2O)产品,溶解,在250mL容量瓶中定容;
b. 量取25.00mL待测溶液于锥形瓶中;
c. 用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
① 实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需_____________________________________。
② 某同学设计的下列滴定方式,最合理的是________。(夹持部分略去)(填字母序号)
③计算上述样品中FeSO4·7H2O的质量分数为________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.用某浓度的NaOH标准溶液滴定未知浓度的HA溶液,下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析