- 化学综合计算
- 共266题
19.将一定量镁铝合金完全溶于100mL某浓度盐酸中,测得混合液里c(Mg2+)= 2 mol·L-1、c(Al3+)=1mol·L-1、c(Cl-)= 8 mol·L-1,往此混合液加入浓度为5 mol·L-1的NaOH溶液至过量,估算后请在右图画出加入NaOH溶液体积与产生沉淀质量的关系图示。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.Cu、Cu2O和CuO组成的混合物,加入100 mL 0.6mol/LHNO3溶液恰好使混合物溶解,同时收集到224 mLNO气体(标准状况)。下列说法不正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.在一定条件下,使CO和O2的混合气体26g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14g,则原混合气体中CO和O2的质量比可能是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点







正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.某固体混合物可能含有下列物质Na2O2、Na2CO3、NaHCO3、NaCl,向混合物中加入足量的盐酸,有气体放出,将放出的气体通入足量的NaOH溶液后,气体体积减少了一部分,若将上述混合物在空气中充分加热,也有气体放出,下列判断正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.将一定质量的Mg和Al的混合物投入2.0mol·L—1,250 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示。则下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.为探究如何尽可能多的使NO2被水吸收,某活动小组设计并完成了以下实验。
(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
①根据反应原理他们选用了相同的装置 ________(填“图l”或“图2”)分别制取N2和O2。
②写出铜与浓硝酸反应的离子方程式______________________________________。
③简述浓硝酸的保存,并说明理由:
浓硝酸要保存在________瓶中,原因 __________;保存在细口瓶中,原因____________________;
使用____________塞,原因___________________________。
(2)活动小组的同学做了如下准备工作:用气囊收集好纯净的O2,收集了一试管NO2,
用干燥的烧瓶收集了一定比例的NO2和O2的混合气体。
①为了尽可能多的使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是 ____________________________。
②利用图4吸收气体时,其操作和现象为_______________________________________ 。
③若图4中混合气体NO2和O2比例为a:b,当混合气体全部被吸收时所得溶液物质的量浓度为___________________mol/L(保留两位有效数字,不考虑烧瓶中溶液向烧杯的扩散)。
正确答案
(1)①图2 ②Cu+4H++2NO-3=Cu2++2NO2↑+2H2O ③ 棕色,防止见光分解;便于倾倒;玻璃,硝酸具强氧化性,腐蚀橡皮塞;
(2)①有利于控制氧气气流的速度(控制氧气的量) ②将胶头滴管中的水挤压进烧瓶,然后打开止水夹,可以看到烧杯中的水进入烧瓶形成喷泉 ③0.036
解析
解析已在路上飞奔,马上就到!
知识点
13.将Fe和Cu的混合物17.6g完全溶解于足量的硝酸溶液中,收集反应产生的X气体。再向所得溶液中加入足量的NaOH溶液,产生31.2g沉淀。根据题意推断气体X的成分可能是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如下图所示,则下列对混合烃的判断正确的是( )
①可能有C2H4
②一定有CH4
③一定有C3H8
④一定没有C2H6
⑤可能有C2H6
⑥可能有C2H2
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
25.某同学设计如图所示装置分别进行探究实验(夹持装置已略去)
请回答下列问题:
(1)简述如何检查该装置的气密性:( )。
(2)该同学认为实验①可通过收集测量NO气体的体积,来探究Cu样品的纯度。你认为是否可行?请简述原因。( ) 。
(3) 实验②、③中,量气管中的液体最好分别是( )、( )。(只选一种)
A.H2O B.CCl4 C.饱和Na2CO3溶液 D.饱和NaHCO3溶液
(4) 本实验应对量气管多次读数,读数时应注意:
①恢复至室温,② ( ),
③视线与凹液面最低处相平。
(5) 实验④获得以下数据(所有气体体积均已换算成标准状况)
根据上述合理数据计算镁铝合金中铝的质量分数 ( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10、在硫酸铁溶液中,加入a g 铜,完全溶解后,又加入b g铁,充分反应后得到c g残余固体,且b<c,则下列判断正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
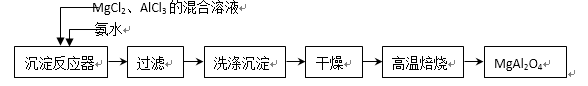
25.实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4 主要流程如下:
⑴制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式( )。
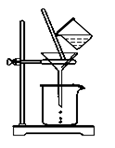
⑵如图所示,过滤操作中的一处错误是 ( )。
判断流程中沉淀是否洗净所用的试剂是( )。高温焙烧时,用于盛放固体的仪器名称是( ) 。
⑶在25℃下,向浓度均为0.01 mol・L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式( )
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10 -34。)
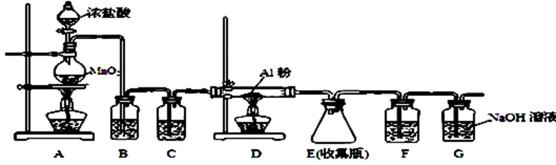
⑷无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
装置B中盛放饱和NaCl溶液,该装置的主要作用是( );
F中试剂的作用是 ( );用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为( )。
⑸将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为 ( ) g。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.某混合气体X,可能由H2、C0、C02和水蒸气中一种或几种组成,现将混合气体通入灼热 CuO,完全反应后,固体CuO质量减少1.6g;再将反应后的混合气体全部导入足量的澄淸 石灰水中,生成白色沉淀10g。根据以上信息,分析下列有关X的组成推断正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.将Mg、Cu组成的2.64g混合物投入适量稀稍酸中恰好完全反应,并收集还原产物气体NO(还原产物只有一种)。然后向反应后的溶液中加入一定浓度的氢氧化钠溶液,使金属恰好沉淀完全,此时生成沉淀的质量为4.68g,则反应过程中收集到NO气体(标况下)体积为( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点







正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析