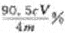- 真题试卷
- 模拟试卷
- 预测试卷
7.下列有关说法错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.常温下,用0. 01 mol 

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
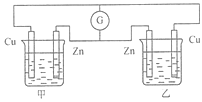
8.在如图的装置中,甲、乙两烧杯中都盛有相同体积的0. 1 mol/L的硫酸溶液,下列有关实验的叙述中错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.对于实验I-IV的描述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
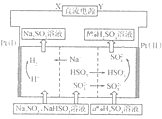
12.用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示。则下列有关说法中不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
2.对如图四幅曲线图中a、b两点的有关叙述中,正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
1.下列有关细胞结构和功能的叙述中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
3.羟可使胞嘧啶分子转变为轻化胞嘧啶,导致DNA复制时发生错配(如图),若一个DNA片段的两个胞嘧啶分子转变为经化胞嘧啶,下列相关叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
5.在西非肆虐的埃博拉病毒传播速度快,已严重威胁了人类的健康,世界各国正在研制疫苗以应对该病毒的传播。下列关于埃博拉病毒进人人体后会发生的情况的叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.下列关于生物育种技术操作合理的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.根据下列框图,有关说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.已知: 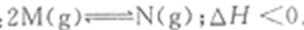
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
14.2012年度诺贝尔物理学奖授予了法国科学家塞尔日·阿罗什与美国科学家大卫·维因兰 德,以表彰他们独立发明并发展测量和控制粒子个体、同时保持它们量子力学特性的方法。在物理学的发展过程中,许多物理学家的科学发现推动了人类历史的进步。下列表述符合 物理学史实的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
16.如图,一质量为m的滑块静止置于倾角为30的粗糙斜面上,一根轻弹簧一端固定在竖直墙上的P点,另一端系在滑块上,弹簧与斜面垂直,则( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
18.如图所示,虚线所示的圆是某电场中某等势面。a,b两个带电粒子以相同的速度,从电场中P点沿等势面的切线方向飞出,粒子仅在电场力作用下的运动轨迹如图中实线所示。则在开始运动的一小段时间内(粒子在图示区域内)。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
17.我国连续发射了多颗“北斗一号”导航定位卫星.预示着我国通讯技术的不断提高。该卫星处于地球的同步轨道,假设卫星质量为m,离地高度为h.地球半径为R,地面附近重力加速度为g,则下列不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
15.如图所示,水平面上停放着A,B两辆小车,质量分别为M和m, M>m,两小车相距为L,人的质量也为m,另有质量不计的硬杆和细绳。第一次人站在A车上,杆插在B车上;第二次人站在B车上,杆插在A车上;若两种情况下人用相同大小的水平作用力拉绳子,使两车相遇,不计阻力,两次小车从开始运动到相遇的时间分别为t1和t2,则( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
31. 如图表示果蝇的几种性染色体异常性别、育性等。请回答下列问题:
(1)白眼雌果蝇(

(2)用黑身白眼雌果蝇(

(3)若控制果蝇眼色的基因仅位于X染色体上,且红眼(B)对白眼(b)为显性。研究发现眼色基因可能会因染色体片段缺失而丢失(记为


①欲用一次杂交实验判断这只白眼雌果蝇出现的原因(不考虑染色体数目变异),请简要写出实验方案的主要思路:让这只白眼雌果蝇与__________________杂交,观察后代果蝇的表现型情况。
②若子代果蝇出现红眼雄果蝇,则是环境条件改变导致的___________________________。
若子代果蝇雌雄个体数量之比为1:1.则是___________________________导致的。若子代果
蝇雌雄个体数量之比为2:1,则是__________________导致的。
③按照假说一演绎法的研究思想,接下来研究人员应___________________________。
正确答案
(1)XBXb 、XBXbY
(2)1/3 1/18
(3)
①红眼雄果蝇
②不可遗传的变异 基因突变 染色体片段缺失
③实施实验,验证假设
解析
解析已在路上飞奔,马上就到!
知识点
32. 如图为某湖泊生态系统部分组成示意图。据图回答下列问题:
(1)从苔草带到沉水植物带,地表分布不同类型生物,这属于群落________________的结构。对3,4带植物影响差异较大的生态因素主要是CO2 浓度和________________。
(2)图中从5-2植物带类型的演变过程,属于________________演替。如果气候条件适宜,从苔草带阶段最终将演变为________________阶段。
(3)小瓜虫寄生在鱼皮肤中,在生态系统的组成成分中,其属于________________。若图中的生物组成食物网,则不应包括的图中生物是________________。
(4)图中II表示的生物摄入的能量一部分储存在粪便中其余成为________________的能量;用干生长、发育和繁殖中的能量一部分成为遗体残骸被分解者分解,其余被________摄入。
正确答案
(1)水平 光照(强度或波长)
(2)初生 森林
(3)消费者 腐生菌
(4)同化 下一营养级
解析
解析已在路上飞奔,马上就到!
知识点
选做题:从给出的2道生物题中任选一题作答。
39.[生物—选修1:生物技术实践]
请利用所学知识,回答下列有关月季的花药培养问题。
(1)诱导花粉植株能否成功及诱导成功率的高低的主要影响因素是______________和___________________。
(2)为了选择适宜发育期的花药,通常选择___________的花蕾。将该时期的花药放在载玻片上,加一滴质量分数为1%的醋酸洋红,用镊柄将花药捣碎,再放在显微镜下观察,若发现大多数花粉粒内只有一个深色的“点”,这种状态的花药是否适合培养?______
(3)进行组织培养需配制MS培养基,欲利于根的分化,植物激素的用量比例应为__________________________。
(4)如图为花药培养产生花粉植株的两种途径,请填出图中A,B及①的名称。(A,B指发育阶段,①、②、③指发育过程,其中②是再分化、③是分化)。
A____________、B____________ ①____________。
(5)在花药培养,特别是通过愈伤组织形成的花粉植株,_____________的数目常常会发生变化,因此还需要对培养出来的植株进行。
40.[生物—选修3:现代生物科技专题]
为增加油菜种子的含油量,研究人员尝试将酶D基因与位于叶绿体膜上的转运肽基因相连,导人油菜细胞并获得了转基因油菜品种。
(1)研究人员依据基因的已知序列设计引物,采用____________法从陆地棉基因文库中获取酶D基因,从拟南芥基因文库中获取转运肽基因。所含三种限制酶(Cla I、Sac I、Xba I)的切点如下图所示。则用______________和_____________酶处理两个基因后,可得到____________ (填图中字母)端相连的融合基因。
(2)将上述融合基因插入右上图所示质粒的T-DNA中,构建____________并导入农杆菌中。将获得的农杆菌接种在含____________的固体平板上培养得到含融合基因的单菌落,再利用培养基震荡培养,可以得到用于转化的浸染液。
(3)剪取油菜的叶片放入染液中一段时间,此过程的目的是________________________。进一步筛选后获得转获因油菜细胞,该细胞通过____________技术,可培育成转基因油菜植株。
(4)提取上述转基因油菜的mRNA,在逆转录酶的作用下获得cDNA。再依据______的DNA片段设计引物进行扩增,对扩增结果进行检测,可判断融合是否完成______。
(5)用_______________法可检测转基因油菜植株中的融合基因是否成功表达。
正确答案
39.
(1)材料的选择 培养基的组成
(2)完全未开放 是
(3)生长素与细胞分裂素比值大
(4)胚状体 愈伤组织 脱分化
(5)染色体组 鉴定和筛选
40.
(1)PCR Cla I DNA连接 A、D
(2)基因表达载体(或重组质粒) 四环素 液体
(3)利用农杆菌将融合基因导入油菜细胞 植物组织培养
(4)融合基因 转录
(5)抗原——抗体杂交
解析
解析已在路上飞奔,马上就到!
知识点
30. 下图是体育运动对学习记忆的促进作用与蛋白质类神经营养因子(BDNF)关系的部分图解。请据图回答间题:
(1)突触小泡中的b物质是__________,该物质通过__________方式进人突触间隙。
(2)运动应激能促进a过程,a过程是指BDNF墓因的____________________。
(3)据图可知,BDNF具有____________________和激活突触后膜上相应受体的作用,从而促进兴奋在突触处传递。若向大鼠脑室内注射抗BDNF的抗体,将导致突触间隙内b物质的含量__________(填“增加’“不变”或“减少”)。
(4)图中________是突触蛋白,它在海马区的密度和分布可间接反映突触的数量和分布情况。有实验表明,水迷宫训练后大鼠海马区突触蛋白表达明显增强,大鼠学习记忆受损后突触蛋白表达水平下降。由此推测,长期记忆可能与____________________的建立有关。
正确答案
(1)神经递质 胞吐(或外排)
(2)表达(或转录和翻译)
(3)促进神经递质的释放 减少
(4)(新)突触
解析
解析已在路上飞奔,马上就到!
知识点
28.(1)已知25℃时有关弱酸的电离平衡常数:
①同温度下,等pH值的
顺序为_________________(填序号)
②25℃时将20 mL 0. 1 mol/LCH3COOH溶液和20 mL0. 1 mol/L HSCN溶液分别与20 mL 0.1 mol/LNaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示。反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是_______________________。反应结束后所得两溶液中,c (SCN-)__________________(填“>”“<”或"=")c( CH3COO-)。
③若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是__________(填序号)。

(2)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx,可以消除撅级化物的污染。
写出CH4 催化还原N2O4(g) 生成N2(g),CO2(g)和H2O (I)的热化学方程式_______________________________。
(3)甲烷燃料电池可以提升能量利用率。如图是利用甲烷燃料电池电解50ml 2mol/L的氯化铜溶液的装置示意图,请回答下列问题:(已知相时原子质量:N14 O16 Cu 64 H 1)
①甲烷徽料电池的负极反应式是_______________。
②当A中消耗0.15 mol氧气时,B中_____________极增重__________________g。
正确答案
(1)
①abc
②相同温度下HSCN比CH3COOH的电离平衡常数大,同浓度时电离出的氢离子浓度大,与NaHCO3溶液反应快 >
③b
(2)
(3)①
解析
解析已在路上飞奔,马上就到!
知识点
选做题:从给出的3道化学题中任选一题作答。
36.[化学—化学与技术]
一种含铝、锂、钴的新型电子材料.生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以

(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为____________。
(2)过程II中加人稀

(3)过程III得到锂铝渣的主要成分是LiF和

(4)碳酸钠溶液在过程III和IV中所起作用有所不同,请写出在过程IV中起的作用是______
________________________________________________________________________。
(5)在 
(6)CoO溶于盐酸可得粉红色的溶液。


37.[化学—物质结构与性质]
我国化学家在“铁基(报掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,荣获2013年度“国家最高科技奖”。
(1)基态
(2)氟、氧、砷三种元素中电负性硫由大到小的顺序是____________。(用元素符号填空)
(3)


①
a.配位键
b.氢键
c.金属键
d.离子键
②已知中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________。
该原子团中

(4)


(5)氮、磷、砷为同主族元素,其化合物的结构又是多样化的。
①该族氢化物(
则Y轴可表示的氢化物(
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化合物的化学式为_________
38.[化学——有机化学基础]
己知A的分子结构摸型如图所示(图中球与球之间的连线代表化学键,如单健、双键等)。
A~H有如下转化关系。
其中A、C、D的相对分子质量有如下关系: 
(1)A的分子式为__________。
(2)J的结构简式为__________。
(3)K和J的关系满足__________(填序号)。
A.同类物质
B.同分异构体
C.同系物
(4)写出下列反应方程式
反应②________________________________________________________;
反应⑤______________________________________________________;
C与F在一定条下反应生成高聚物_________________________________。
(5)同时符合“①1 mol 该物质能和3 mol NaOH反应②1 mol该物质与等量的银氨溶液反应,生成4mol银单质”两项要求的C的同分异构体的数目为_________种。任写出其中的一种的结沟简式____________________。
36.选做题:从给出的3道化学题中任选一题作答。36.[化学—化学与技术]
一种含铝、锂、钴的新型电子材料.生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以

(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为____________。
(2)过程II中加人稀H2SO4酸化后.再加人Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为____________________________________(产物中只有一种酸根)。在实验室模拟工业生产时,也可用盐酸浸出钴。但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因____________________________________。
(3)过程III得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用。请写出该反应的离子方程式____________________________________。
(4)碳酸钠溶液在过程III和IV中所起作用有所不同,请写出在过程IV中起的作用是______
________________________________________________________________________。
(5)在 Na2CO3,溶液中存在多种粒子,下列各粒子浓度关系正确的是______(填序号)。
(6)CoO溶于盐酸可得粉红色的溶液。


37.[化学—物质结构与性质]
我国化学家在“铁基(报掺杂镨氧铁砷化合物)高温超导”材料研究上取得了重要成果,荣获2013年度“国家最高科技奖”。
(1)基态Fe2+的核外电子排布式为_______。
(2)氟、氧、砷三种元素中电负性硫由大到小的顺序是____________。(用元素符号填空)
(3)Fe(SCN)3溶液中加入NH4F,发生如下反应:
①
a.配位键b.氢键c.金属键d.离子键
②已知中各原子最外层均满足8电子稳定结构,则C原子的杂化方式为_____________。
该原子团中

(4)FeCl3晶体易溶于水、乙醇,用酒精灯加热即可气化,而FeF3晶体熔点高于1000
(5)氮、磷、砷为同主族元素,其化合物的结构又是多样化的。
①该族氢化物(
则Y轴可表示的氢化物(RH3)性质可能有____________(选填序号,下同)。
②碳氮化钛化合物在汽车制造和航空航天等领域有广泛的应用,其结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,据此分析,这种碳氮化钛化合物的化学式为_________
38.[化学——有机化学基础]
己知A的分子结构摸型如图所示(图中球与球之间的连线代表化学键,如单健、双键等)。
正确答案
正确答案
正确答案
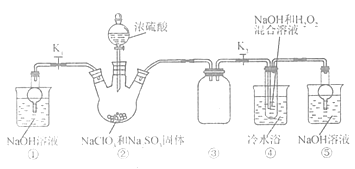
26. 某化学兴趣小组同学展开对漂白剂制亚氯酸钠(NaClO2)的研究。
实验I: 制取NaClO2 晶体
已知:NaClO2 饱和溶液在①温度低于38℃时析出晶体是NaClO2.H2O ②温度离于38℃时析出晶体是NaClO2 ③温度高于60℃时NaClO2分解成NaClO3和NaCl。
现利用如图所示装置进行实验。
(1)装置里③的作用是__________________________。
(2)装置中产生的ClO2化学方程式_______________________。装置④中制备NaClO2的化学方程式为_______________________。
(3)从装置反应后的溶液获得NaClO2晶体的操作步骤为①减压,55℃蒸发结晶,趁热过滤;③_______________________。④低手6℃干燥,得到成品。
实验II: 测定某亚氯酸钠样品的纯度
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品m g于烧杯中,加人适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应后,加蒸馏水至250 ml。(已知:
②移取25.00mL待测液于锥形瓶中,加几滴淀粉溶液,用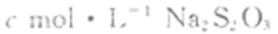
定,至滴定终点。重复2次,测得平均值为VmL(己知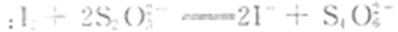
(4)达到滴定终点时的现象为_____________________________________。
(5)该样品中NaClO2(分子量=90.5)的质量分数为_______________________(用含m、c、V的代数式表示)。
(6)在滴定操作正确无误的情况下,此实验侧得结果偏高。原因用离子方程式表示为____
___________________。
正确答案
(1)安全瓶或防止倒吸
(2)
(3)用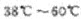
(4)滴入最后一滴,溶液刚好由蓝色变为无色,且在半分钟内不变色。
(5)
(6)
解析
解析已在路上飞奔,马上就到!
知识点
27. 铜是一种重要的战略物资,以黄铜矿(主要成分是CuFeS2)为主要原料生产铜、铁 红、单质硫时,原料的综合利用率较高,其主要流程如图所示(已知Na[CuCl2]〕的电离方程式为
(1)流程中粉碎的目的是______________________________________,操作①、②、
③、④的目的相同,在实验中这种操作的名称是___________________。
(2)铁红的重要用途:_________________________________,固体B将有两种产物,一种是单质C、另一种是原子个数比为1:1的一种金属的低价态盐,写出堆浸时反应的化学
方程式___________________。
(3)反应V的离子方程式为_________________。
(4)此方法中得到的铜纯度不能满足某些生产的需要,需要利用电解法进行提纯。若用如图所示的装置进行电解精炼,则乙中溶液的溶质是________。e电极上的电极反应式为__________________。若当电路中有2 mol电子通过时,乙中某个电极质量减轻了63.92g,则粗铜的纯度为_________(己知相对原子质量:Fe56 Cu 64)(假设杂质只有铁且精炼时铜与铁的放电比例与混合物比例相同。计算时用%表示保留一位小数)。
正确答案
(1)增大反应物间的接触面积,有利于充分、快速的反应 过滤
(2)生产油漆、铁盐
(3)
(4)CuSO4 
解析
解析已在路上飞奔,马上就到!
知识点
23. 如图(1)一a所示,用铁架台、弹簧和多个已知质量且质量相等的钩码,探究在弹性限内弹簧弹力与弹簧伸长长度的关系实验。
(1)为完成实验,还需要的实验器材有__________________。
(2)实验中需要测量的物理量有___________。
(3)图(1)-b是弹黄所受弹力F与弹簧伸长长度x的F-x图线,由此可求出弹赞的劲度系数为________N/m,图线不过原点的原因是___________________。
正确答案
(1)刻度尺
(2)弹簧的原长、弹簧伸长后的长度
(3)200 弹簧有自重
解析
解析已在路上飞奔,马上就到!
知识点
选做题:从给出的物理题中任选一题作答。
33.略
34.[物理—选修3一4]
(1)下列说法正确的是( )
A.拍摄玻璃橱窗内的物品时,往往在镜头前加一个偏振片以增加透射光的强度
B.麦克斯韦关于电磁场的两个基本观点是:变化的磁场产生电场和变化的电场产生磁场
C.部队过桥不能齐步走而要便步走,是为了避免桥梁发生共振现象
D.狭义相对论认为:一切物理规律在不同的惯性参考系中都相同
E.用标准平面来检查光学面的平整程度是利用光的偏振现象
(2)一列机械波某时刻的波形图如图所示。从此时开始,质点d到达波蜂的时间比质
点c早0. 5s。已知质点b的平衡位置为
①机械波的波速为多少;
②质点b再经过多少时间第一次到达波峰以及这段时间内通过的路程。
35.[物理—选修3一5]
(1)下列说法正确的是( )
A.采用物理或化学方法可以有效地改变放射性元索的半衰食期
B.夜德威克发现了中子
C.现在的很多手表指针上涂有一种并报型发光材料,白天吸收光子外层电子跃迁到高能轨道,晚上向低能级跃迁放出光子,其发光的波长一定跟吸收的光的波长完全一致
D.质子和中子结合成新原子核一定有质量亏损,释放出能量
E.分别用x射线和紫光照射同一金版表面都能发生光电效应。则用X射线照射时光电子的 最大初动能较大
(2)如图所示,长为L=2m的木板A质量为M=2 kg,A静止于足够长的光滑水平面上。小物块B(可视为质点)静止于A的左端,B的质量为m1=1 kg。曲面与水平面相切于M点。现让另一小物块C(可视为质点)从光滑曲面上离水平面高h=3.6 m处由静止滑下,C与A相碰后与A粘在一起,C的质量为m2=1 kg。A与C相碰后,经一段时间B可刚好离开A。g=

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
25. 如图(a)为一研究电磁感应的实验装置示意图。其中电流传感器(电阻不计)能将各时刻的电流数据实时通过数据采集器传输给计算机,经计算机处理后在屏幕上同步显示出I-t图像。平行且足够长的光滑金属轨道的电阻忽略不计。导轨平面与水平方向夹角




(1)匀强磁场的磁感应强度B的大小和在t=0.5时电阻R的热功率;
(2)已知0-1.2 s内通过电阻R的电荷量为1. 3 C,求0-1.2s内金属棒MN的位移及在R上产生的焦耳热。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
24. 有一条模拟索道长30米、倾斜角度设计为
(1)实验过程中,吊环从顶端静止释放,经过t=5s到达索道底端,则吊环到达底端时它所受重力的功率为多少?
(2)若在竖直平面内给吊环施加一个垂直于索道方向的恒力F。由静止释放吊环后保持它的加速度大小a=1



正确答案
解析
解析已在路上飞奔,马上就到!
知识点
22. 二极管是一种半导体元件,它的符号为
(1)某课外兴趣小组想要描绘某种晶体二极管的伏安特性曲线。因二极管外壳所印的标识模糊,为判断该二极管的正、负极,他们用多用电表电阻挡测二极管的正、反向电阻。其步骤是:将选择开关旋至合适倍率,进行欧姆调零,将黑表笔接触二极管的左端、红表笔接触右端时,指针偏角比较小。然后将红、黑表笔位处对调后再进行测量,指针偏角比较大,由此判断__________(填“左”或“右”)端为二极管的正极。
(2)厂家提供的伏安特性曲线如图,为了验证厂家提供的数据,该小组对加正向电压时的伏安特性曲线进行了描绘,可选用的器材有:
A.直流电源E:电动势3V,内阻忽略不计 B.滑动变阻器R:0-20
C.电压表V1:量程5V、内阻约50k
E.电流表A:量程0.6A、内阻约0.5 
G.待测二极管D H.单刀单掷开关S,导线若干
为了提高测量结果的准确度,电压表应选用________,电流表应选用________。
(填写各器材前的字母代号)
(3)为了达到测量目的,请在答题卡上虚线框内画出正确的实验电路原理图。
正确答案
(1)右 (2)D F (3)如图
解析
解析已在路上飞奔,马上就到!
知识点
20.如图所示的变压器,接如图甲所示的交流电时,灯泡正常发光,电容器能正常工作。现将电源换成如图乙所示的交流电,则( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
19.如图所示,边长为L、不可形变的正方形导线框内有半径为r的圆形磁场区域,其磁感应强度B随时间t的变化关系为B=kt(常量k>O)。回路中沿动变阻器R的最大阻值为滑动片P位于滑动变阻器中央。定值电阻R1=R0、R2=
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
21.如图所示,在I、II两个区域内存在磁感应强度均为B的匀强磁场,磁场方向分别垂直于纸面向外和向里,AD,AC边界的夹角


正确答案
解析
解析已在路上飞奔,马上就到!