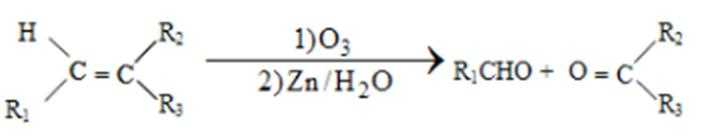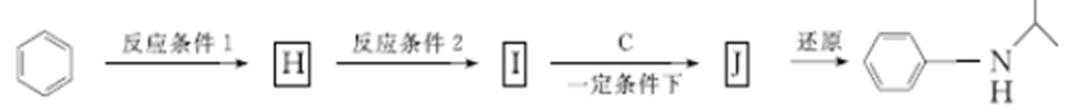- 真题试卷
- 模拟试卷
- 预测试卷
10.在不同温度下,水溶液中c(H+)与c(OH-)有如下图所示关系。下列关于离子共存说法中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
14.我国探月的“嫦娥工程”已启动,在不久的将来,我国宇航员将登上月球。假如宇航员在月球上测得摆长为l的单摆做小振幅振动的周期为T,将月球视为密度均匀、半径为r的球体,则月球的密度为( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.一定温度下,下列溶液的离子浓度关系式正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
1.用蛋白酶处理大肠杆菌核糖体,处理后的核糖体仍可催化氨基酸的脱水缩合反应,由此可以推测核糖体中能催化该反应的物质是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
2.将某植物花冠切成大小和形状相同的细条,分为a、b、c、d、e和f组(每组的细条数相等),取上述6组细条分别置于不同浓度的蔗糖溶液中,浸泡相同时间后测量各组花冠细条的长度,结果如图所示。假如蔗糖溶液与花冠细胞之间只有水分交换,则( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
3.正常生长的绿藻,照光培养一段时间后,用黑布迅速将培养瓶罩上,此后绿藻细胞的叶绿体内不可能发生的现象是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
4.下图是真核细胞中糖类合成与分解过程示意图。下列叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
5.某种植物果实重量由三对等位基因控制,这三对基因分别位于三对同源染色体上,对果实重量的增加效应相同且具叠加性。已知隐性纯合子和显性纯合子果实重量分别为150g和270g。现将三对基因均杂合的两植株杂交,F1 中重量为190g的果实所占比例为( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6. 鸟类的性别决定为ZW型。某种鸟类的眼色受两对独立遗传的基因(A、a和B、b)控制。甲乙是两个纯合品种,均为红色眼。根据下列杂交结果,推测杂交I的亲本基因型是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.用NA表示阿伏加德罗常数的值。下列叙述不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.已知:可逆反应N2(g)+3H2(g
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
17.在稳定轨道上的空间站中,物体处于完全失重状态。有如下图所示的装置,半径分别为r和R(R>r)的甲、乙两个光滑的圆形轨道安置在同一竖直平面上,轨道之间有一条水平轨道CD相通,宇航员让一小球以一定的速度先滑上甲轨道,通过粗糙的CD段,又滑上乙轨道,最后离开两圆轨道,那么下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
16. 利用如图所示的理想变压器给用电器供电。在原线圈ab端接交流电压(V),原线圈匝数n1=1000匝,副线圈匝数n2=50匝。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
15.图为某一质点作直线运动的位移x随时间变化的规律,图为一条抛物线,则下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
18.一个在y方向上做简谐运动的物体,其振动图象如图所示.下列关于图(1)~(4)的判断正确的是(选项中v、F、a分别表示物体的速度、受到的回复力和加速度)( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
19.如图所示,一个质量为m的人站在台秤上,跨过光滑定滑轮将质量为



正确答案
解析
解析已在路上飞奔,马上就到!
知识点
20.如下图所示,传送带的水平部分长为L,传动速率为v,在其左端无初速度释放一小木块,若木块与传送带间的动摩擦因数为μ,则木块从左端运动到右端的时间不可能是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
30.肥胖与遗传密切相关,是影响人类健康的重要因素之一。
(1)某肥胖基因发现于一突变系肥胖小鼠,人们对该基因进行了相关研究。为确定其遗传方式,进行了杂交实验,根据实验结果与结论完成以下内容。
实验材料:______________小鼠;杂交方法:______________。
实验结果:子一代表现型均正常;结论:遗传方式为常染色体隐性遗传。
(2)正常人体能合成一种抑制肥胖的蛋白类激素,检测蛋白质的试剂是 ______________。在人类肥胖症研究中发现,许多人能正常分泌能抑制肥胖的激素却仍患肥胖症,其原因是靶细胞缺乏相应的______________ 。
(3)目前认为,人的体重主要受多基因遗传的控制。假如一对夫妇的基因型均为AaBb(A、B基因使体重增加的作用相同且具累加效应,两对基因独立遗传),从遗传角度分析,其子女体重超过父母的概率是 ______________,体重低于父母的基因型为______________;从环境角度分析,AABB不一定表现为体重超重,说明肥胖是 ______________ 共同作用的结果。
正确答案
(1)纯合肥胖小鼠和纯合正常;正反交
(2)双缩脲试剂;受体
(3)5/16 aaBb、Aabb、aabb;基因型和环境
解析
解析已在路上飞奔,马上就到!
知识点
26.席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:
已知以下信息:
①
②1molB经上述反应可生成2molC,且C不能发生银镜反应。
③D属于单取代芳香烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤
回答下列问题:
(1)由A生成B的化学方程式为___________________,反应类型为___________________。
(2)D的化学名称是 ___________________,由D生成E的化学方程式为: ___________________ 。
(3)G的结构简式为___________________。
(4)F的同分异构体中含有苯环的还有________种(不考虑立体异构)。其中核磁共振氢谱中有
4组峰,且面积比为6:2:2:1的是__________________。(写出其中的一种的结构简式)。
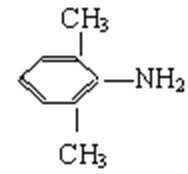
(5)由苯和化合物C经如下步骤可合成N-异丙基苯胺。
反应条件1所选择的试剂为_________________;反应条件2所选择的试剂为___________;I的结构简式为________________________。
正确答案
(1)C(CH3)2Cl—CH(CH3)2+NaOH乙醇△ C(CH3)2=C(CH3)2+NaCl+H2O,消去反应
(2)乙苯,C2H5—+HNO3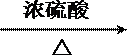
(3)C2H5——NCH3
(4)19种,
(5)浓硝酸、浓硫酸;Fe/稀盐酸;—NH2。
解析
解析已在路上飞奔,马上就到!
知识点
31.植物秸秆中的纤维素可被某些微生物分解。回答下列问题:
(1)分解秸秆中纤维素的微生物能分泌纤维素酶,该酶是由3种组分组成的复合酶,其中的葡萄糖苷酶可将__________分解成_________ 。
(2)在含纤维素的培养基中加入刚果红(CR)时,CR可与纤维素形成_________色复合物。用含有CR的该种培养基培养纤维素分解菌时,培养基上会出现以该菌的菌落为中心的 _________。
(3)为从富含纤维素的土壤中分离获得纤维素分解菌的单菌落,某同学设计了甲、乙两种培养(成分见下表):
(注:“+”表示有,“-”表示无)
据表判断,培养基甲_________(填“能”或“不能”)用于分离和鉴别纤维素分解菌;培养基乙 (填“能”或“不能”)用于分离和鉴别纤维素分解菌,原因是_________。
正确答案
(1)纤维二糖;葡萄糖
(2)红;透明圈
(3)能;不能培养基中有淀粉,纤维素不是唯一碳源,没有加CR。
解析
解析已在路上飞奔,马上就到!
知识点
25.四种短周期元素A、B、C、D的性质或结构信息如下:
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题。
(1)B元素在周期表中的位置______,请写出BC2分子的电子式_____ 。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式。
①A元素的单质与物质甲发生的反应________________________ 。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的反应_______________________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中的现象是:
①浅绿色溶液变成深棕黄色,
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间,
③试管底部出现红褐色沉淀。向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色。
请用化学方程式或离子方程式及必要的文字解释①、②、③中加点的字。① _____;② _____;③ _____ 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27. 次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式_______________________。
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为__________;
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为___________(填化学式);
③NaH2PO2为___________(填“正盐”或“酸式盐”),其溶液显___ ____(填“弱酸性”、“中性”或“弱碱性”)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________。
(4)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式_________________ ___________________;
②分析产品室可得到H3PO2的原因__________________ _________________;
③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有________杂质,该杂质产生的原因是 ________________ 。
正确答案
(1)H3PO2
(3)2P4+3Ba(OH)2+6H2O=2PH3↑+3Ba(H2PO2)2
(4)①2H2O-4e-=4H++O2↑或4OH--4e-=2H2O+O2.
②由于阳极室OH-放电,造成H+浓度增大,通过阳膜扩散进入产品室,而原料室中的H2PO2-可以通过阴膜进入产品室,二者反应生成H3PO2.
③H3PO4或PO43-。由于H3PO2具有还原性,电解时就会有H3PO2在阳极放电而被氧化生成H3PO4。
解析
解析已在路上飞奔,马上就到!
知识点
29.Ⅰ.氢是一种清洁能源。莱茵衣藻能利用光能将H2O分解成[H]和O2,[H]可参与暗反应,低氧时叶绿体中的产氢酶活性提高,使[H]转变为氢气。
(1)莱茵衣藻捕获光能的场所在叶绿体的_________。
(2)CCCP(一种化学物质)能抑制莱茵衣藻的光合作用,诱导其产氢。已知缺硫也能抑制莱茵衣藻的光合作用。为探究缺硫对莱茵衣藻产氢的影响,设完全培养液(A组)和缺硫培养液(B组),在特定条件下培养莱茵衣藻,一定时间后检测产氢总量。
实验结果:B组>A组,说明缺硫对莱茵衣藻产氢有_________ 作用。
为探究CCCP、缺硫两种因素对莱茵衣藻产氢的影响及其相互关系,则需增设两实验组,其培养液为_________和_________。
(3)产氢会导致莱茵衣藻生长不良,请从光合作用物质转化的角度分析其原因是莱茵衣藻光反应产生的[H]转变为氢气,参与暗反应的[H]减少,_________ 。
(4)在自然条件下,莱茵衣藻几乎不产氢的原因是_________抑制的产氢酶活性,因此可通过筛选高耐氧产氢藻株以提高莱茵衣藻产氢量。
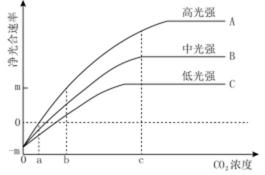
Ⅱ.某植物净光合速率的变化趋势如图所示。据图回答下列问题:
(1)当CO2浓度为a时,高光强下该植物的有机物积累量为_________;此时该植物的叶肉细胞中,光合作用强度_________ (填“大于”、“等于”或“小于”)呼吸作用强度。
(2)CO2浓度在a~b之间时,曲线_________表示了净光合速率随CO2浓度的增高而增高。
(3)CO2浓度大于c时,曲线B和C所表示的净光合速率不再增加,限制其增加的环境因素是_________;若此时升高温度,曲线B和C的饱和点都向_________方向移动。
(4)当环境中CO2浓度小于a时,在图示的3种光强下,该植物呼吸作用产生的CO2量_________(填“大于”、“等于”或“小于”)光合作用吸收的CO2量。
(5)据图可推测,在温室中,若要采取提高CO2浓度的措施来提高该种植物的产量,还应该同时考虑_________这一因素的影响,并采取相应措施。
正确答案
Ⅰ.(1)类囊体薄膜
(2)促进 添加CCCP的完全培养基 添加CCCP的缺硫培养基
(3)有机物合成量减少或暗反应速率减慢
(4)氧气
Ⅱ(1)0 大于
(2)A、B和C
(3)光强 左下
(4)大于
(5)光强
解析
解析已在路上飞奔,马上就到!
知识点
28. 下图为细菌冶铜和火法冶锎的主要流程。
(1)硫酸铜溶液一般不呈中性,原因是____________(用离子方程式表示)。写出电解硫酸铜溶液的化学方程式:______________(电解过程中,始终无氢气产生)。
(2)细菌冶金又称微生物浸矿,是近代湿法冶金工业上的一种新工艺。细菌冶铜与火法冶铜相比,优点为_______________________(写出一点即可)。
(3)用惰性电极分别电解浓的氯化铜溶液和硫酸铜溶液。电解浓的氯化铜溶液时发现阴极有金属铜生成,同时阴极附近会出现棕褐色溶液。而电解硫酸铜溶液时,没有棕褐色溶液生成。下面是关于棕褐色溶液成分的探究
①有同学认为,阴极附近出现的棕褐色溶液是氯气反应的结果,你认为他的猜测是否正确?______(填“正确”或“不正确"),原因是_____________________。
资料1:一般具有混合价态(指化合物中同一元素存在两种不同的化合价,如Fe3O4中的 Fe元索)的物质的颜色比单一价态的物质的颜色要深。
资料2:CuCl微溶于水,能溶于浓盐酸。
②猜想:棕褐色溶液中可能含有的离子是________________(填3种主要离子符号)。
③验证猜想:完成实验方案(配制棕褐色溶液)。
取少量___________固体于试管中,加入_____________使其溶解,再加入______________溶液,观察现象。
④已知电解前,U形管中加入了1OOmLO.5 mol.L-1 CuCl2溶液,电解结束时电路中一共转移了0.03 mol电子,且阴极生成0.64 g铜,则形成的低价阳离子的物质的量为_____mol。
正确答案
(1)酸:
(2)节约能源,环保,设备简单,操作方便,工艺条件易控制、投资少,成本低(或适宜处理贫矿、废矿、尾矿、炉渣等)
(3)①不正确,阴极不会产生氯气
②
③氯化亚铜;浓盐酸;氯化铜
④0.01
解析
解析已在路上飞奔,马上就到!
知识点
23.如下图,竖直平面坐标系xOy的第一象限,有垂直xOy面向外的水平匀强磁场和竖直向上的匀强电场,大小分别为B和E;第四象限有垂直xOy面向里的水平匀强电场,大小也为E;第三象限内有一绝缘光滑竖直放置的半径为R的半圆轨道,轨道最高点与坐标原点O相切,最低点与绝缘光滑水平面相切于N.一质量为m的带电小球从y轴上(y>0)的P点沿x轴正方向进入第一象限后做圆周运动,恰好通过坐标原点O,且水平切入半圆轨道并沿轨道内侧运动,过N点水平进入第四象限,并在电场中运动(已知重力加速度为g).
(1)判断小球的带电性质并求出其所带电荷量;
(2)P点距坐标原点O至少多高;
(3)若该小球以满足(2)中OP最小值的位置和对应速度进入第一象限,通过N点开始计时,经时间t=2小球距坐标原点O的距离s为多远?
正确答案
解析:(1)小球进入第一象限正交的电场和磁场后,在垂直磁场的平面内做圆周运动,说明重力与电场力平衡,
设小球所带电荷量为q,则有qE=mg
解得:
又电场方向竖直向上,
故小球带正电.
(2)设小球做匀速圆周运动的速度为v、轨道半径为r,
由洛伦兹力提供向心力得:qBv=mv2/r
小球恰能通过半圆轨道的最高点并沿轨道运动,
则应满足:mg=mv2/R
由②③④得:
即PO的最小距离为:
(3)小球由O运动到N的过程中设到达N点的速度为vN,
由机械能守恒定律得:

由④⑦解得:
小球从N点进入电场区域后,在绝缘光滑水平面上做类平抛运动,
设加速度为a,
则有:沿x轴方向有:x=vNt
沿电场方向有:
由牛顿定律得:
t时刻小球距O点为:
解析
解析已在路上飞奔,马上就到!
知识点
21.实验题
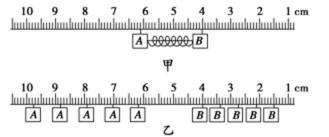
Ⅰ.气垫导轨上有A、B两个滑块,开始时两个滑块静止,它们之间有一根被压缩的轻质弹簧,滑块间用绳子连接(如图甲所示),绳子烧断后,两个滑块向相反方向运动,图乙为它们运动过程的频闪照片,频闪的频率为10 Hz,由图可知:
(1)A、B离开弹簧后,应该做________运动,已知滑块A、B的质量分别为200 g、300 g,根据照片记录的信息,从图中可以看出闪光照片有明显与事实不相符合的地方是______________________________________________。
(2)若不计此失误,分开后,A的动量大小为________ kg·m/s,B的动量的大小为________ kg·m/s,本实验中得出“在实验误差允许范围内,两滑块组成的系统动量守恒”这一结论的依据是:______________________________________。
Ⅱ.某学习小组通过实验来研究电器元件Z的伏安特性曲线。他们在实验中测得电器元件Z两端的电压与通过它的电流的数据如下表:
现备有下列器材:
A.内阻不计的6V电源;
B.量程为0~3A的内阻可忽略的电流表;
C.量程为0~0.3 A的内阻可忽略的电流表;
D.量程为0~3V的内阻很大的电压表;
E.阻值为0~10Ω,额定电流为3A的滑动变阻器;
F.电键和导线若干。
(1)这个学习小组在实验中电流表应选 (填器材前面的字母);
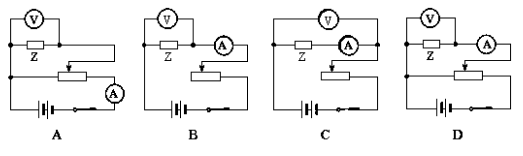
(2)请你从下面的实验电路图中选出最合理的一个( );
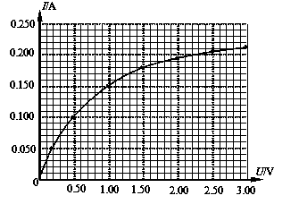
(3)利用表格中数据绘出的电器元件Z的伏安特性曲线,如图所示,分析曲线可知该电器元件Z的电阻随U变大而_________(填 “变大”、“变小”或“不变” );
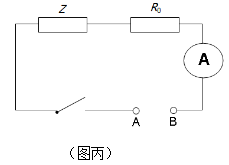
(4)若把用电器Z接入如图丙所示的电路中时,电流表的读数为0.150A,已知A、B两端电压恒为2V,则定值电阻R0 阻值为_______Ω。(结果保留两位有效数字)。
正确答案
Ⅰ.
(1) 匀速直线运动 、 在离开弹簧前A、B均做加速运动,A、B两滑块的第一个间隔应该比后面匀速时相邻间隔的长度小
(2) 0.018 kg·m/s 、0.018 kg·m/s 分开后A、B的动量大小均为p=0.018 kg·m/s,方向相反,满足动量守恒,系统的总动量为0
Ⅱ.
(1)C
(2)D
(3) 变大
(4) 6.7 (6.7----6.9之间均可)
解析
解析已在路上飞奔,马上就到!
知识点
24.如下图所示,光滑的水平面AB与半径为R=0.32 m的光滑竖直半圆轨道BCD在B点相切,D为轨道最高点.用轻质细线连接甲、乙两小球,中间夹一轻质弹簧,弹簧与甲、乙两球不拴接.甲球的质量为m1=0.1 kg,乙球的质量为m2=0.3 kg,甲、乙两球静止在光滑的水平面上.现固定甲球,烧断细线,乙球离开弹簧后进入半圆轨道恰好能通过D点.重力加速度g取10 m/s2,甲、乙两球可看作质点。
(1)试求细线烧断前弹簧的弹性势能;
(2)若甲球不固定,烧断细线,求乙球离开弹簧后进入半圆轨道能达到的最大高度;
(3)若给甲、乙两球一向右的初速度v0的同时烧断细线,乙球离开弹簧后进入半圆轨道仍恰好能通过D点,求v0的大小。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
22.如图丁所示为一电流表的原理示意图.质量为m的均质细金属棒MN的中点处通过一挂钩与一竖直悬挂的弹簧相连,绝缘弹簧劲度系数为k.在矩形区域abcd内有匀强磁场,磁感应强度大小为B,方向垂直纸面向外.与MN的右端N连接的一绝缘轻指针可指示标尺上的读数,MN的长度大于.当MN中没有电流通过且处于平衡状态时,MN与矩形区域的cd边重合;当MN中有电流通过时,指针示数可表示电流强度。(不计通电时电流产生的磁场的作用)
(图丁)
(1)当电流表示数为零时,弹簧伸长多少?(重力加速度为g)
(2)若要电流表正常工作,MN的哪一端应与电源正极相接?
(3)若k=2.0 N/m,=0.20 m,=0.050 m,B=0.20 T,此电流表的量程是多少?
正确答案
(1)设当电流表示数为零时,弹簧的伸长量为Δx,
则有mg=kΔx ①
由①式得:Δx=. ②
(2)为使电流表正常工作,作用于通有电流的金属棒MN的安培力必须向下,
因此M端应接正极.
(3)设电流表满偏时通过MN间电流强度为Im,
则有BIm+mg=k(+Δx) ③
联立②③并代入数据得Im=2.5 A. ④
解析
解析已在路上飞奔,马上就到!