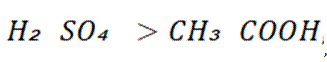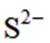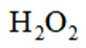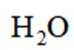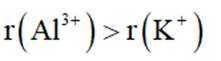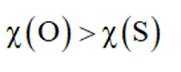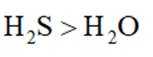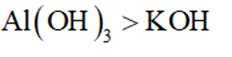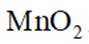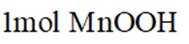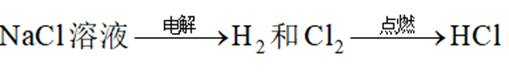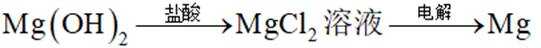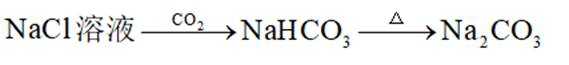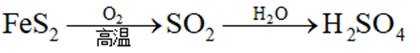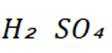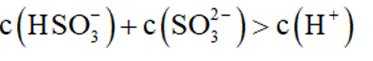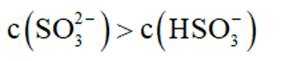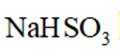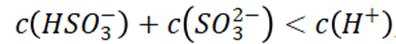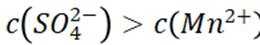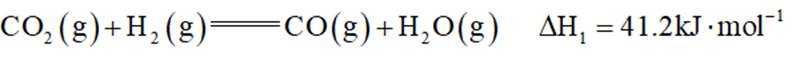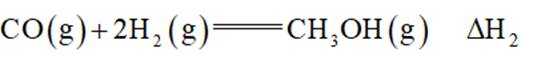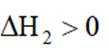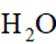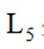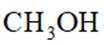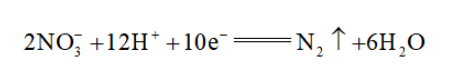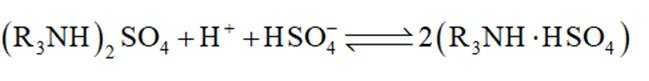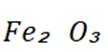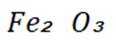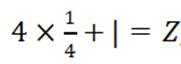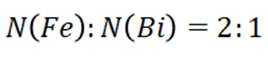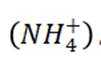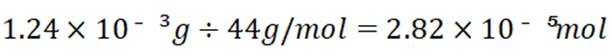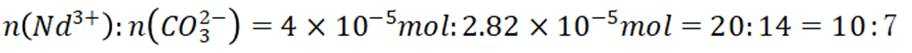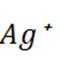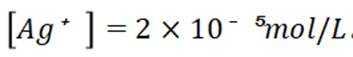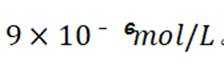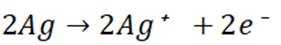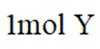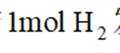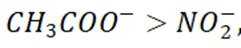- 真题试卷
- 模拟试卷
- 预测试卷
我国探月工程取得重大进展.月壤中含有Ca、Fe等元素的磷酸盐,下列元素位于元素周期表第二周期的是( )
正确答案
解析
这道题主要考察了元素周期表的相关知识
逐一分析各选项:
选项A:O是8号元素,核外有2个电子层,位于元素周期表第二周期,
故选项A正确。
选项B:P是15号元素,核外有3个电子层,位于元素周期表第三周期,故选项B错误
选项C:Ca是20号元素,核外有4个电子层,位于元素周期表第四周期,故选项C错误
选项D:Fe是26号元素,核外有4个电子层,位于元素周期表第四周期,故选项D错误。
反应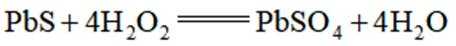
正确答案
解析
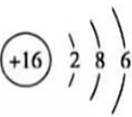
这道题主要考察了原子结构示意图、化学键、化合价以及分子空间构型等知识点
逐一分析各选项:
选项A: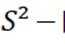
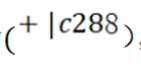
选项B: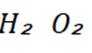
选项C: 在 
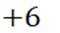
选项D: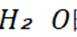
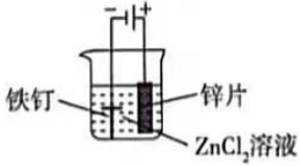
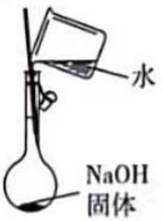
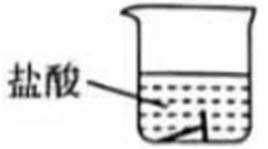
实验室进行铁钉镀锌实验.下列相关原理、装置及操作不正确的是( )

正确答案
解析
这道题主要考察了溶液的配制、金属的除锈、电镀等知识点
A 项:配制一定物质的量浓度的溶液时,在烧杯中溶解固体,用玻璃棒搅拌加速溶解,操作正确。
B 项:用盐酸可以除去铁钉表面的铁锈,操作正确。
C 项:除油污一般用碱性溶液,而盐酸不能除油污,该项操作错误。
D 项:可以通过该装置进行铁钉镀锌的实验,操作正确。
明矾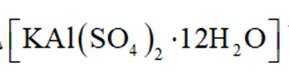
正确答案
解析
这道题主要考察了微粒半径比较、电负性比较、物质沸点比较以及碱性强弱比较等知识点。
A 项: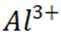
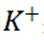

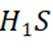

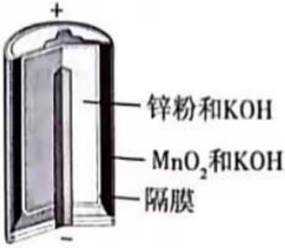
碱性锌锰电池的总反应为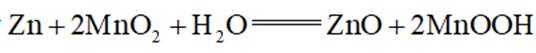
正确答案
解析
这道题主要考察了原电池的工作原理、氧化还原反应、离子的移动等知识点
A项: 在该反应中,
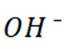
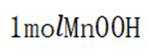
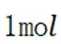

在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
正确答案
解析
这道题主要考察了物质的制备转化、化学反应的条件及可行性等知识点
A项, 


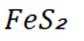
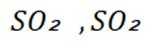
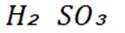

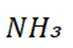

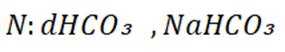


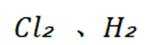
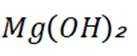
室温下,通过下列实验探究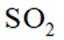

实验1:将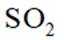
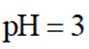
实验2:将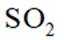
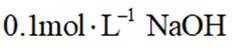
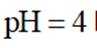
实验3:将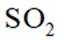
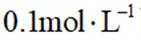

下列说法正确的是( )
正确答案
解析
这道题主要考察了二氧化硫的性质、电离平衡常数、溶液中离子浓度的比较等知识点
题干:给出了关于亚硫酸的电离常数以及三个涉及三氧化硫的实验。
A项:实验Ⅰ中三氧化硫与水反应生成亚硫酸,亚硫酸存在两步电离:

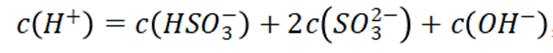




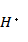
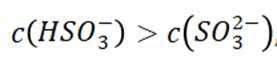

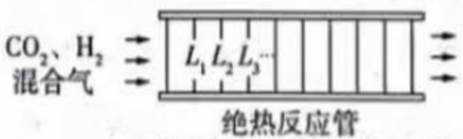
二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①
②
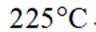


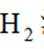
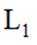

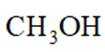
(容器内与外界没有热量交换)
正确答案
解析
这道题主要考察了化学反应原理的相关知识,包括化学平衡常数、焓变、化学反应速率,以及对反应过程中温度变化和物质体积分数变化的分析理解等知识点
题干:给出了二氧化碳加氢制甲醇过程中的主要反应以及在特定条件下反应管中不同位点处的温度、CO和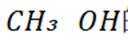
A项:平衡常数只与温度有关,从图中可知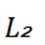

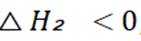

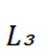
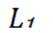
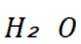
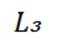
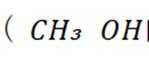
阅读下列材料,完成5~7题:
催化剂能改变化学反应速率而不改变反应的焓变,常见催化剂有金属及其氧化物、酸和碱等.催化反应广泛存在,如豆科植物固氮、石墨制金刚石、
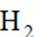
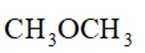
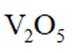
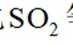



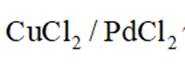
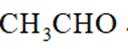
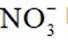

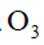
第一小题:下列说法正确的是( )
A.豆科植物固氮过程中,固氮酶能提高该反应的活化能
B.C2H4与O2反应中,Ag催化能提高生成CH3CHO选择性
C.H2O2制O2反应中,MNO2能加快化学反应速率
D.SO2与O2反应中,V2O5能减小该反应的焓变
第二小题:下列化学反应表示正确的是( )
A.汽车尾气处理:
B.电催化为的阳极反应:
C.硝酸工业中的氧化反应:
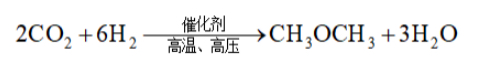
D.和催化制二甲醚:
第三小题:下列有关反应描述正确的是( )
A.CH3CH2OH催化氧化为CH3CHO,CH3CH2OH断裂C-O键
B.氟氯烃破坏臭氧层,氟氯烃产生的氯自由基改变O3分解的历程
C.丁烷催化裂化为乙烷和乙烯,丁烷断裂
D.石墨转化为金刚石,碳原子轨道的杂化类型由SP3转变为SP2
正确答案
第一小题正确答案
BC
第二小题正确答案
B
第三小题正确答案
B
解析
第一小题:这道题主要考察了催化剂对化学反应的影响,包括催化剂对反应活化能、反应速率、反应选择性以及焓变等方面的作用。同时也涉及到对一些常见化学反应和物质的理解A项:固氮酶的作用是降低反应的活化能, 而不是提高,A错误。B项:催化剂能提高目标产物的选择性, Ag催化(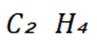
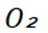


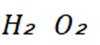
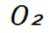
第二小题:这道题主要考察了化学反应方程式的书写是否正确,涉及到一些常见化学反应的原理和配平,同时也考查对一些特定反应中反应物、生成物及反应条件等方面知识的掌握
A选项:汽车尾气处理中, 一氧化碳和一氧化氮反应生成氮气和二氧化碳,化学方程式为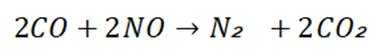
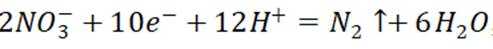
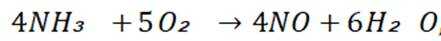

第三小题:这道题主要考察了有机反应中化学键的变化、一些物质对臭氧层的影响、化学反应历程、化学键的类型以及碳原子轨道杂化类型等知识点
A项: 乙醇 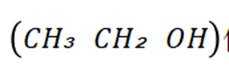

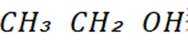
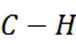
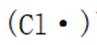
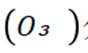

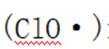

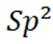
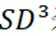


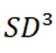
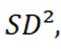
回收磁性合金钕铁硼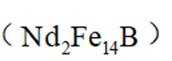
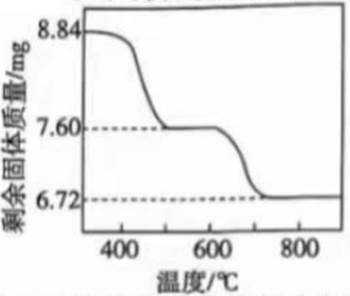
(1)钕铁硼在空气中焙烧转化为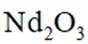

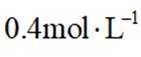
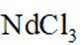

①含铁滤渣的主要成分为________(填化学式).
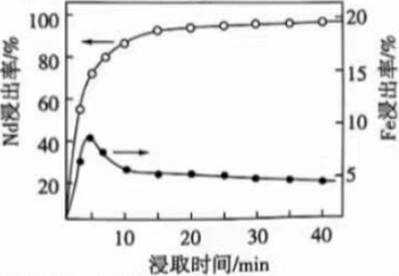
②浸出初期Fe浸出率先上升后下降的原因是________________.
(2)含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋.
①用含有机胺(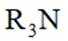
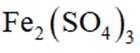

已知:
其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,有机层中Fe元素含量迅速增多的原因是________________.
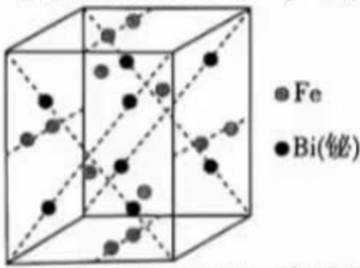
②反萃取后,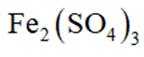
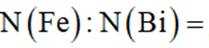
(3)净化后的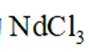
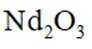
①向
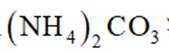
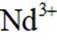
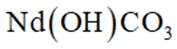
②将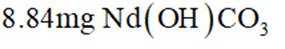
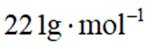
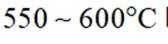


正确答案
(1)①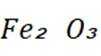

(2)①迅速增多,氢离子浓度减小, 平衡正向移动; ②2:1
(3)① 
解析
这道题主要考察了以下知识点:
金属化合物与酸的反应以及物质的溶解性。
化学反应速率的影响因素,包括反应物浓度、反应产物对反应的影响等
离子方程式的书写:包括正确判断反应物和生成物,并根据电荷守恒和原子守恒配平离子方程式。
物质的量的计算:通过给定物质的质量和摩尔质量,计算物质的量。
化学反应中的质量守恒:根据化学反应的化学计量关系,计算反应产物的质量。
对物质受热分解反应的理解和应用
(1)①含铁滤渣的主要成分为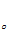
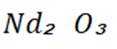

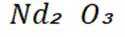
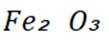
②浸出初期,随着反应进行,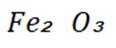
(2)①随水层pH增大,氢离子浓度减小,平衡
(有机层)正向移动,所以有机层中Fe元素含量迅速增多。②晶胞中Bi原子个数为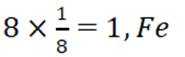



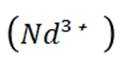

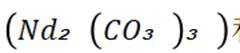
②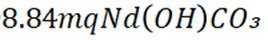
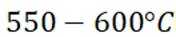

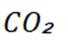
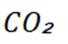
所以
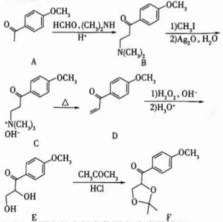
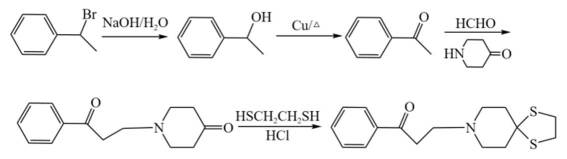
F是合成含松柏基化合物的中间体,其合成路线如下:
(1)A分子中的含氧官能团名称为醚键和________.
(2)
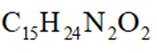
(3)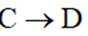
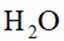
(4)写出同时满足下列条件的F的一种芳香族同分异构体的结构简式:________________.碱性条件下水解后酸化,生成X、Y和Z三种有机产物.X分子中含有一个手性碳原子;Y和Z分子中均有2种不同化学环境的氢原子,Y能与
(5)已知: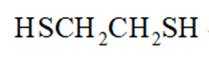
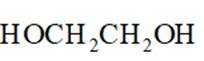
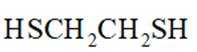


正确答案
(1)羟基
(2)
(3) 氧化反应,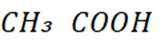
(4)
(5)
解析
这道题主要考察了以下知识点:
有机化合物中官能团的识别,如醚键、羟基等。
有机化学反应类型的判断,如取代反应、氧化反应。
同分异构体的书写和判断。
根据给定条件推导有机化合物的结构。
有机合成路线的设计和书写。
(1)A分子中的含氧官能团名称为醚键和羟基。
(2)根据A、B的结构简式及副产物的分子式可知,副产物是A中两个氨基与一分子甲醛反应的产物,结构简式为
(3)C → D是醇羟基被氧化为羰基,反应类型为氧化反应;C转化为D时还生成
(4)满足条件的F的一种芳香族同分异构体为
(5)
贵金属银应用广泛.Ag与稀
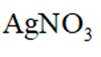
(1)沉淀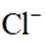
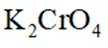
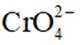
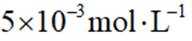
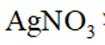
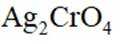
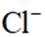
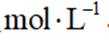
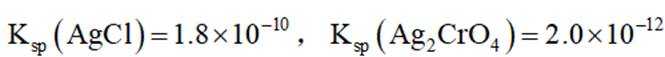
(2)还原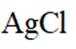
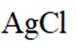
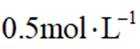
①铁将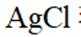
②不与铁圈直接接触的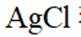
③为判断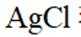
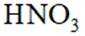

(3)Ag的抗菌性能.纳米Ag表面能产生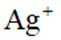
①纳米Ag溶解产生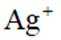
②实验表明溶解氧浓度过高,纳米Ag的抗菌性能下降,主要原因是________________.
正确答案
(1)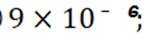
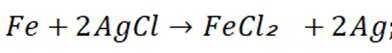
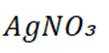
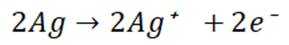

解析
这道题主要考察了以下知识点:
溶度积常数的计算和应用,通过溶度积常数计算溶液中离子的浓度。
氧化还原反应的化学方程式书写。
原电池原理在化学反应中的应用。
离子的检验方法。
电极反应式的书写。
物质性质与化学反应原理对物质抗菌性能的影响分析。
(1)当开始产生.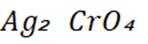
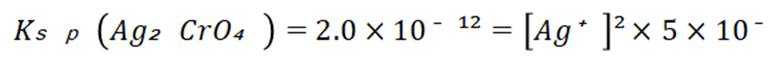

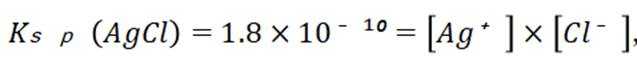
故此时溶液中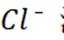
(2)①铁将AgCl转化为单质Ag的化学方程式为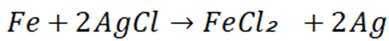
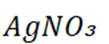
(3)①纳米Ag溶解产生
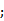

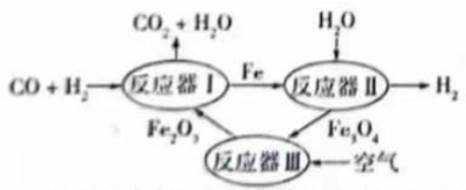
氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成.
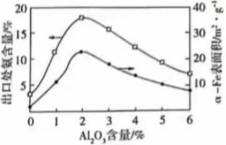
(1)利用铁及其氧化物循环制氢,原理如图所示.反应器Ⅰ中化合价发生改变的元素有________;含CO和
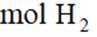
(2)一定条件下,将氮气和氢气按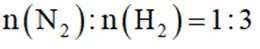
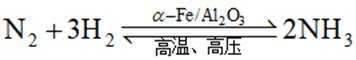
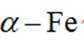
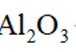

①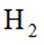
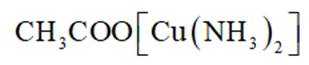
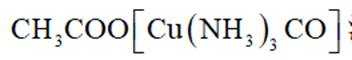
②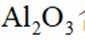

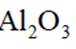
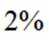
(3)反应
①密闭容器中,其他条件不变,向含有催化剂的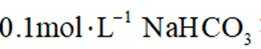
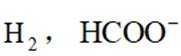

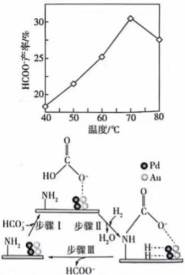
②使用含氨基物质(化学式为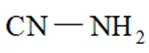
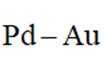
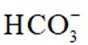

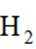
正确答案
(1)C、 H; l。
(2)①
②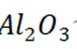

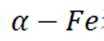
(3) ①温度升高,催化剂活性可能降低或反应可能为放热反应,温度升高平衡逆向移动;②氨基与
解析
这道题主要考察了
化合价、化学方程式的书写与理解
混合物中各物质的量的计算
化学反应速率和化学平衡的影响因素,包括温度对反应速率和平衡移动的影响。
催化剂的活性与温度的关系。
物质之间的静电作用。
利用同位素示踪法探究反应机理。
(1)在反应器Ⅰ中,碳元素由二氧化碳中的+4价变为一氧化碳中的+2价,氢元素由水中的+1价变为氢气中的0价,所以化合价发生改变的元素有C、H;根据反应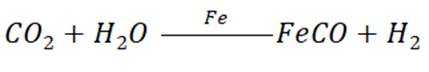

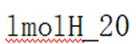

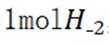
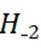
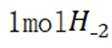
(2)①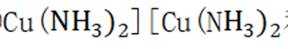
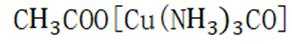
②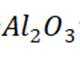
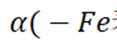
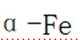
(3) ①温度高于

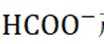
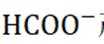
②氨基能将 
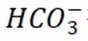
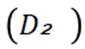

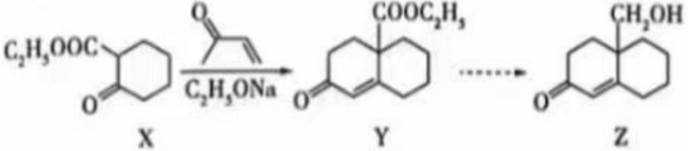
化合物Z是一种药物的重要中间体,部分合成路线如下:
下列说法正确的是( )
正确答案
解析
这道题主要考察了有机物的结构与性质方面的知识点
A项:x分子中存在饱和碳原子,饱和碳原子与其相连的原子构成四面体结构,所以X分子中所有碳原子不可能共平面,A错误。B项:Y分子中含有碳碳双键和酯基,酯基不能与氢气发生加成反应, 所以
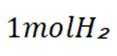


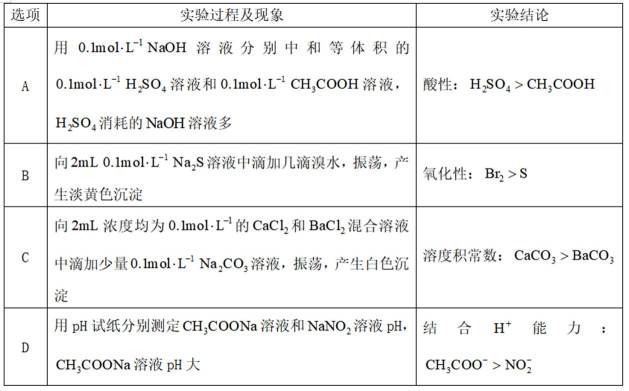
室温下,根据下列实验过程及现象,能验证相应实验结论的是( )
正确答案
解析
这道题主要考察了酸碱中和反应、氧化性强弱比较、沉淀溶解平衡以及盐类水解等知识点
A项: 等体积等浓度的硫酸和醋酸,硫酸是强酸完全电离,醋酸是弱酸部分电离,所以硫酸中氢离子浓度大于醋酸中氢离子浓度,与等浓度的氢氧化钠反应时,硫酸消耗的氢氧化钠多,可得出酸性: