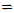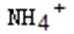- 真题试卷
- 模拟试卷
- 预测试卷
2.下列化学用语或图示表达正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
5.下列关于合成材料的说法中,不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.利用如图装置探究铁在海水中的电化学防护,下列说法不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
3.下列有机物系统命名正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
4.在通常条件下,下列各组物质的性质排列正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.一定条件下,可逆反应C(s)+CO2(g)
①升高反应体系的温度;
②增加反应物C的用量;
③缩小反应体系的体积:
④减少体系中CO的量。
上述措施中一定能使反应的正反应速率显著加快的( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温,下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列分离或提纯物质的方法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.常温下,浓度均为0.1mol/L的三种溶液:
①CH3COOH溶液
②NaOH溶液
③CH3COONa溶液
下列说法中不正确的是(忽略混合前后溶液体积变化)( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.下列离子方程式书写正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
14.下列各组中两种气体所含的原子数一定相等的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.据美国《科学》杂志报道,外太空的某个星球的大气层中含有大量的CH2=CHOH,此物质常温下为液体,不稳定,易转化为CH3CHO,方程式为CH2=CHOH→CH3CHO +Q(Q﹥0)。据此,以下叙述中不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
15.木质素是制浆造纸工业的副产物,具有优良的物理化学特点,若得不到充分利用,变成了制浆造纸工业中的主要污染源之一,不仅造成严重的环境污染,而且也造成资源的重大浪费。木质素的一种单体结构简式如图所示,下列说法错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
16.向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
17.将Fe和Fe2O3的混合物加入25mL 2mol/L的HNO3溶液中,反应完全后,无固体剩余,生成224mL NO气体(标准状况),再向反应后的溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积至少是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
1.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也叫可入肺颗粒物,与肺癌、哮喘等疾病的发生密切相关,是灰霾天气的主要原因,它主要来自化石燃料的燃烧(如机动车尾气、燃煤)等,下列与PM2.5相关的说法不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
19.两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是( )
正确答案
解析
每小题有一个或两个正确选项,只有一个正确选项的,多选不给分,有两个正确选项的,选对一个给2分,选错一个该小题不给分。
知识点
20.某二元酸(化学式H2A)在水中的电离方程式是H2A→ H+ + HA-、HA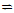
正确答案
解析
每小题有一个或两个正确选项,只有一个正确选项的,多选不给分,有两个正确选项的,选对一个给2分,选错一个该小题不给分。
知识点
21.下图所示的实验,能达到实验目的的是( )
正确答案
解析
每小题有一个或两个正确选项,只有一个正确选项的,多选不给分,有两个正确选项的,选对一个给2分,选错一个该小题不给分。
知识点
18.从下列事实所得出的相应结论正确的是( )
正确答案
解析
每小题有一个或两个正确选项,只有一个正确选项的,多选不给分,有两个正确选项的,选对一个给2分,选错一个该小题不给分。
知识点
22.把一定量的Na2O2和NaHCO3混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成干燥的气体2.24L(标准状况),再将此气体通入到另一份混合物中,充分反应后,气体减少为2.016L(标准状况),则原混合粉末中Na2O2和NaHCO3的物质的量之比及原稀盐酸的物质的量浓度可能是( )
正确答案
解析
每小题有一个或两个正确选项,只有一个正确选项的,多选不给分,有两个正确选项的,选对一个给2分,选错一个该小题不给分。
知识点
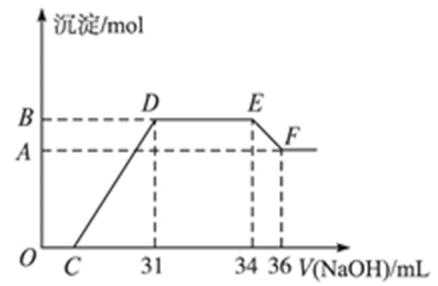
23.某反应池中,发生“生物硝化过程”,利用O2将NH4+氧化成NO3-,如果不考虑过程中硝化细菌的增殖,其净反应如下式所示:
(1)完成上述反应的离子方程式并配平,将系数填入方框中,并标出电子的转移方向和数目。
(2)反应中,还原剂是_____________,被还原的元素是_____________。
(3)将铵态氮中的lmg氮转化成硝酸根中的氮,需氧气_____________mg。(精确到0.01)
(4)取100mL完全反应以后的溶液,加入19.2g铜粉及一定量的稀硫酸,恰好完全反应(假设还原产物全部是NO气体),则原溶液中NH4+的浓度为_____________mol/L。(假设反应前后溶液的体积不变)
正确答案
(1)
(2)NH4+ 、 O2中的O
(3)4.57
(4) 2
解析
解析已在路上飞奔,马上就到!
知识点
26.黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:
现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的
请回答下列问题:
(1)称量样品所用的仪器为____________,将样品研细后再反应,其目的是___________________________。
(2)装置a的作用是________。
A.有利于空气中氧气充分反应
B.除去空气中的水蒸气
C.有利于气体混合
D.有利于观察空气流速
(3)上述反应结束后,仍需通一段时间的空气,其目的是__________________________。
(4)滴定时,标准碘溶液所耗体积为_______mL。
判断滴定已达终点的现象是__________________________。
(5)通过计算可知,该黄铜矿的纯度为_______________。
(6)若用如图装置替代上述实验装置d,同样可以达到实验目的的是____。(填编号)
正确答案
(1)电子天平 ; 提高反应速率,并使黄铜矿充分反应
(2)BD
(3)把装置中的二氧化硫气体全部吸收
(4)20.00 ;溶液由无色变成蓝色,并半分钟内不褪色
(5)80%
(6)②
解析
解析已在路上飞奔,马上就到!
知识点
27.三聚氰胺(化学式:C3N6H6)是一种非食品类的重要有机化工原料,广泛用于塑料、造纸、建材等行业。下图是我国科技工作者研制的以尿素为原料生产三聚氰胺的工艺——“常压气相一步法联产纯碱新技术”:
已知:
①尿素的熔点是132.7℃,常 压下超过160℃即可分解;
②三聚氰胺的熔点是354℃,加热易升华,微溶于水;
③以尿素为原料生产三聚氰胺的原理是:6 CO(NH2)2
请回答:
(1)尿素是一种常用含氮量最高的化肥,其氮元素的质量百分数为______,在实验室使其熔化的容器名称叫__________。
(2)工业上合成尿素的化学反应方程式为___________________________(反应条件可以不写)
(3)写出各主要成份的化学式:产品1____________、产品2____________、X____________;(4)联氨系统沉淀池中发生的化学反应方程式为:___________________________;
(5)为了使母液中析出更多的产品2 ,常用的方法是_______.
A.加入固体NaCl
B.加入固体NaHCO3
C.通入CO2气体
D.通入NH3
(6)若生产过程中有4%的尿素损耗,每吨尿素可生产三聚氰胺__________吨,副产品纯碱_______吨。(精确到0.001)
正确答案
(1) 46.67%;坩埚
(2)CO2+2NH3 → CO(NH2)2 + H2O
(3)三聚氰胺 ;NH4Cl ;CO2
(4)CO2+ NH3 + NaCl + H2O → NH4Cl + NaHCO3
(5)AD
(6)0.336; 0.848
解析
解析已在路上飞奔,马上就到!
知识点
24.X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示。
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)X单质分子的结构式是______________,Z元素原子最外层共有_____种不同运动状态的电子。
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是________________。
(3)常温时,W的硫酸盐溶液的pH___ 7(填“=”、“>”或“<”),理由是(用离子方程式表示):___________________________。
(4)25℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6 kJ的热量,写出该反应的热化学方程式___________________________ 。
正确答案
(1)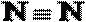
(2) HClO4>HNO3>H2CO3
(3)< 7 ;Al3+ + 3H2O
(4)CH4(g)+ 2O2(g)→ CO2(g)+ 2H2O(l)+ 890.3 KJ
解析
解析已在路上飞奔,马上就到!
知识点
25.在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为____________mol/L·min。
(2)根据上图写出该反应的化学方程式________________________,该反应的平衡常数表达式为K =____________________。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如右图,则该反应的正反应是_________(填“放热”或“吸热”)反应,反应的平衡常数_________(填“增大”、“减小”或“不变”。下同),B的反应速率_________。
(4)若在第7分钟时增加D的物质的量,A的物质的量变化正确的是______(用图中a、b、 c的编号回答)
正确答案
(1)0.067
(2)2D(s) 
(3)吸热 ;增大;增大
(4)b
解析
解析已在路上飞奔,马上就到!
知识点
28.由中国科研人员从中药材中提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有100%的治愈率。根据下面金丝桃素的结构简式回答下列问题:
(1)金丝桃素能在NaOH水溶液中加热反应得A和B,B为芳香族化合物,写出:
B的结构简式:_____________,A的分子式是_____________.
(2)室温下,B用稀盐酸酸化得C,下列物质中不能和C发生反应的是____________(填序号)
①浓H2SO4和HNO3的混合
②H2(催化剂加热)
③CH3CH2CH2CH3
④Na
⑤ O2(催化剂)
⑥NaHCO3溶液
(3)写出两分子C与浓H2SO4共热,生成八元环状物的化学方程式:________________________。
(4)写出符合下列条件的与C互为同分异构体是____________________。(任写一种)
①能发生银镜反应
②苯环上的一卤代物有3种
③1mol该有机物与足量金属钠反应产生1mol气体
正确答案
(1)
(2)③
(3)
(4)
解析
解析已在路上飞奔,马上就到!
知识点
29.由苯合成香料K和解热镇痛药物G的路线如下:
已知:
Ⅰ.
Ⅱ.
请回答:
(1)芳香烃A中C、H原子数之比是4∶5,1 mol A在氧气中完全燃烧生成8 mol CO2,A的分子式是__________; A的结构简式是______________。
(2)B→K的反应类型是__________。
(3)B的结构简式是__________________。
(4)D→E反应的化学方程式是__________________________。
(5)K与新制Cu(OH)2悬浊液反应的化学方程式是____________________________。
(6)G与第55小题中反应的有机产物互为同分异构体,含有相同的官能团,且位置与F中官能团的位置相同,G的结构简式是_________________。
正确答案
(1)C8H10;
(2)取代反应
(3)
(4)
(5)
(6)
解析
解析已在路上飞奔,马上就到!
知识点
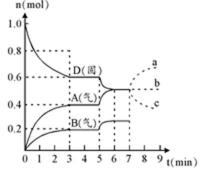
30.某同学取一定量的Al和Fe固体混合物,与2.0 L极稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为_________________________。
在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为______________________;上述现象说明溶液中____________结合OH-的能力比___________强(填写离子符号)。
(2)B与A的差值为______________mol。
(3)B点对应的沉淀的物质的量为____________mol,C点对应的氢氧化钠溶液的体积为______________mL。
(4)求原硝酸溶液的物质的量浓度?
正确答案
(1)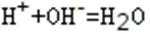
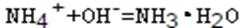
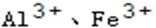
(2)0.008
(3)0.032 ;7
(4)0.074
解析
解析已在路上飞奔,马上就到!