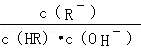- 真题试卷
- 模拟试卷
- 预测试卷
8.CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE路线如下:
下列分析正确的是
正确答案
解析
A.CPAE中含有1个酯基与2个酚羟基,可与NaOH反应,含有2个酚羟基与1个碳碳双键,可与溴水发生反应,含有苯环与碳碳双键,可与氢气发生加成反应,则1molCPAE与NaOH溶液,浓溴水和氢气反应时最多消耗的NaOH、Br2和H2的物质的量分别是3mol、4mol和7mol,正确;
B.咖啡酸分子中,苯环上6个碳原子与6个H原子共面,碳碳双键中的碳取代苯环上的氢原子,则分子中至少有7个碳原子共平面,错误;
C.咖啡酸中含有酚羟基,可与溴水发生取代,与氢气发生加成反应,但不能发生消去反应,错误;
D.CAPE与咖啡酸均含有酚羟基,遇FeCl3溶液均可显紫色,所以不能检测上述反应中是否有CPAE生成,错误;所以答案为A。
考查方向
解题思路
本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重羧酸、酚、醇等物质性质的考查,选项B为解答的难点,注意酚-OH不能发生消去反应。
咖啡酸不能发生消去反应,CPAE不能发生消去反应,均含苯环可发生加成反应,-OH可发生取代反应;
咖啡酸、CPAE均含酚-OH,均与FeCl3溶液发生显色反应,则不能检验是否有CPAE生成;
含有酚羟基,在邻位和对位发生取代反应,含有碳碳双键,可发生加成反应,则1 mol的咖啡酸最多可与4 mol Br2发生反应;
苯环上所有碳原子处于同一平面上,乙烯中两个碳原子处于同一平面上,咖啡酸中含有苯环碳碳双键,所以所有碳原子可能处于同一平面上。
易错点
1、咖啡酸分子中碳原子共平面的结构分析。
2、含有酚羟基,在邻位和对位发生取代反应,含有碳碳双键,可发生加成反应。
知识点
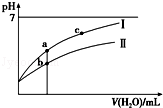
11.已知:25℃时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、 HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是
正确答案
解析
根据表中电离常数可知:酸性由强至弱的顺序为CH 3 COOH>H 2 CO 3 >HClO>HCO,结合质子的能力由大到小的顺序为>ClO- >>CH 3 COO- 。
A项, ClO- 的水解程度大于CH 3 COO- 的水解程度,同浓度CH 3 COONa和NaClO的混合液中,各离子浓度的大小关系应是 c (Na+ )> c (CH 3 COO- )> c (ClO- )> c (OH- )> c (H+ ),错误;
B项, 结合质子的能力大于ClO- 结合质子的能力,离子方程式应为ClO- +CO 2 +H 2 O=HClO+,错误;
C项, 分子、分母同乘以溶液中 c (H+ ),得,该式即为 K 电离 / K w ,温度相同则该式的值相等,正确;
D项, CH 3 COOH的酸性强于HClO,pH相同时,HClO的浓度大于CH 3 COOH的浓度,错误。
考查方向
解题思路
由表格可知,酸性的强弱顺序为CH3COOH >H2CO3> HClO>HCO3-,大于A中相同浓度CH3COONa和NaClO的混合液中,由于醋酸酸性强于次氯酸,则NaClO的水解程度CH3COONa,则溶液中c(CH3COO﹣) >c(ClO﹣),;B、由于酸性H2CO3> HClO>HCO3-,则向NaClO溶液中通入少量二氧化碳的离子方程式为:ClO﹣+CO2+H2O═HClO+HCO3﹣;C、由图象可知,稀释过程中,Ⅰ的变化程度更大,则Ⅰ为酸性更强的CH3COOH,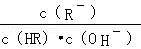
易错点
1、溶液导电能力大小与溶液中自由移动离子成正比,与电解质强弱无关,为易错点。
2、弱电解质的电离要根据酸的电离常数与酸根离子水解程度、酸的酸性强弱等知识点来分析解答。
知识点
6.2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行.能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是
正确答案
解析
A.地沟油、矿物油均能燃烧,不能区别,故A错误;
B.地沟油、矿物油均为混合物,没有固定沸点,不能区别,故B错误;
C.地沟油、矿物油均不溶于水,且密度均比水小,不能区别,故C错误;
D.加入足量氢氧化钠溶液共热,不分层的是地沟油,分层的为矿物油,现象不同,能区别,故D正确;
故选D.
考查方向
解题思路
A、地沟油属于油脂,含有C、H、O三种元素,矿物油中含有C、H元素,均可燃烧,错误;
B、矿物油为混合物,没有恒定的溶沸点,错误;
C、地沟油与矿物油的密度均小于水,都会浮在水面上,错误;
D、地沟油的主要成分为油脂,与NaOH可发生水解,矿物油不能与其反应,会浮在液面上方,正确;所以答案为D。
易错点
1、地沟油属于油脂,矿物油属于烃。
2、油脂与NaOH可发生水解,矿物油属于烃不能发生水解。
知识点
7.实验室制备下列气体时,所用方法正确的是
正确答案
考查方向
解题思路
二氧化氮与水反应生成NO,NO有毒,应选NaOH溶液吸收尾气;氯气与碳酸氢钠溶液反应,不能除杂,应选饱和食盐水和浓硫酸;乙烯不溶于水,密度比空气小,且与空气密度接近,则不能利用排空气法;
Na2O2或H2O2作反应物,均为固体与液体反应,且不需要加热,则制备氧气时可选择相同的气体发生装置。
易错点
1、氯气与碳酸氢钠溶液反应,不能除杂,应选饱和食盐水和浓硫酸。
2、乙烯不溶于水,密度比空气小,且与空气密度接近,则不能利用排空气法
知识点
9.如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O下列关于该电池工作时说法正确的是
正确答案
解析
A、甲池中为原电池反应,对应的电极反应式是:正极O2+4e-+2H2O=4OH-,负极N2H4-4e-+4OH-=N2+4H2O,故A错误;
B、甲池中因反应生成了水会使溶液的pH值减小,乙池中因反应生成了酸也会使溶液的pH值减小,故B错误;
C、选项中没说明气体的体积是否是标准状况下,所以气体的物质的量无法计算,则乙中生成的固体的质量也无法计算,故C错误;
D、乙池发生的是电解池反应,其电解总反应的离子方程式为:2Cu2++2H2O 通电2Cu+4H++O2↑,两极析出的分别是Cu和O2,因而加CuO后溶液能够复原,故D正确.
故选D.
考查方向
本题主要考查了原电池和电解池的工作原理
解题思路
本题考查了原电池、电解池工作的基本原理,以及原电池电极反应式的书写,注意把握原电池和电解池中电极方程式的书写方法。由图可知,甲为原电池,乙为电解池,甲池的总反应式为:N2H4+O2═N2+2H2O,则通过化合价的变化可知,N2H4的化合价升高,为负极,但电解质溶液为KOH,则电极反应为N2H4﹣4e﹣+4OH-═N2+4H2O,
甲池中生成了水,导致甲池中的PH变小;C中没有指明是否为标准状况下,不能进行计算;乙池中的总反应为2CuSO4+2H2O=2H2SO4+2Cu+O2,加入CuO,可与硫酸发生反应,生成硫酸铜,恢复到原浓度。
易错点
1、原电池和电解池中电极方程式的书写方法。
2、通过化合价的变化判断电极的正负极。
知识点
苯酚是一种重要的化工原料.以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N.(部分产物及反应条件已略去)
13.由苯酚生成A的化学方程式是 .
14.已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种.C的结构简式是________________
15.B与C反应的化学方程式是 .
16.由苯酚生成D的化学方程式是
由D生成N的反应类型是_________________
由D生成N的反应方程式是___________________
17.以苯酚为基础原料也可以合成防腐剂F.经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31%,F完全燃烧只生成

则F的分子式是___________________
已知:①芳香族化合物F能与
②F的核磁共振氢谱显示其分子中含有4种氢原子;
③分子结构中不存在“-O-O-”的连接方式.
F的结构简式是____________________
正确答案


解析
苯酚与氢氧化钠反应生成苯酚钠,故A为


故答案为:

考查方向
解题思路
考查有机物的推断,涉及酚、羧酸等性质与转化,注意根据苯酚、D的分子式、N的结构式推断D的结构,注意(5)中利用相对分子质量取代F的分子式,是对有机化合物知识的综合考查,能较好的考查学生思维能力,是高考热点题型。苯酚与氢氧化钠反应生成苯酚钠,故A为




易错点
1、有机合成与推断高分子化合物。
2、有机反应的书写。
正确答案
解析
由上述分析可知,C的结构简式是
考查方向
本题主要考查了酚、酸、醇;有机合成与推断高分子化合物;有机物的结构;有机反应类型
解题思路
考查有机物的推断,涉及酚、羧酸等性质与转化,注意根据苯酚、D的分子式、N的结构式推断D的结构,注意(5)中利用相对分子质量取代F的分子式,是对有机化合物知识的综合考查,能较好的考查学生思维能力,是高考热点题型。苯酚与氢氧化钠反应生成苯酚钠,故A为






易错点
1、有机合成与推断高分子化合物。
2、有机反应的书写。
正确答案
解析
B与C反应的化学方程式是
考查方向
本题主要考查了酚、酸、醇;有机合成与推断高分子化合物;有机物的结构;有机反应类型
解题思路
考查有机物的推断,涉及酚、羧酸等性质与转化,注意根据苯酚、D的分子式、N的结构式推断D的结构,注意(5)中利用相对分子质量取代F的分子式,是对有机化合物知识的综合考查,能较好的考查学生思维能力,是高考热点题型。苯酚与氢氧化钠反应生成苯酚钠,故A为




易错点
1、有机合成与推断高分子化合物。
2、有机反应的书写。
正确答案
2


解析
生成N的反应类型是缩聚反应,D的结构简式是

考查方向
解题思路
考查有机物的推断,涉及酚、羧酸等性质与转化,注意根据苯酚、D的分子式、N的结构式推断D的结构,注意(5)中利用相对分子质量取代F的分子式,是对有机化合物知识的综合考查,能较好的考查学生思维能力,是高考热点题型。苯酚与氢氧化钠反应生成苯酚钠,故A为




易错点
1、有机合成与推断高分子化合物。
2、有机反应的书写。
正确答案
解析
以苯酚为基础原料也可以合成防腐剂F.经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31%,则分子中氧原子数目为







故答案为:
考查方向
本题主要考查了酚、酸、醇;有机合成与推断高分子化合物;有机物的结构;有机反应类型
解题思路
考查有机物的推断,涉及酚、羧酸等性质与转化,注意根据苯酚、D的分子式、N的结构式推断D的结构,注意(5)中利用相对分子质量取代F的分子式,是对有机化合物知识的综合考查,能较好的考查学生思维能力,是高考热点题型。苯酚与氢氧化钠反应生成苯酚钠,故A为




易错点
1、有机合成与推断高分子化合物。
2、有机反应的书写。
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
18.已知:N2(g)+O2(g) = 2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g) 
2H2(g)+O2(g) = 2H2O(g) △H=-483.6kJ/mol
若有17 g 氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为 .
19.某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)
实验结果如图所示:
(图中T表示温度,n表示物质的量)
①图像中T2和T1的关系是:T2 T1(填“高于”、“低于”、“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2 的转化率最高的是 (填字母).
③在起始体系中加入N2的物质的量为 mol时,反应后氨的百分含量最大; 若容器容积为1L,n=3mol反应达到平衡时H2的转化率为60%,则此条件下(T2), 反应的平衡常数K= .
20.N2O5是一种新型硝化剂,其性质和制备受到人们的关注
①一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)
则500s内NO2的平均生成速率为 .
②现以H2、O2、熔融盐Na2CO3组成的燃料电池,
写出石墨I电极上发生反应的电极反应式 .
在电解池中生成N2O5的电极反应式为 .
正确答案
226.3 kJ
解析
N2(g)+O2(g)═2NO(g)△H=+180.5kJ/mol ①
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol ②
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol ③
由盖斯定律①×2-②×2+③×3得:4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=905.2kJ/mol;
则17g 即1mol氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为1/4×905.2kJ=226.3 kJ,
故答案为:226.3 kJ;
考查方向
解题思路
根据盖斯定律来求反应的焓变,然后根据反应放出的热量与物质的量成正比;
①根据温度升高化学平衡向着吸热方向进行;
②根据增加氢气的物质的量化学平衡向着正反应方向移动;
③根据a、b、c三点所表示的意义来回答;
④根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大;根据化学平衡状态是反应物的转化率最大、生成物的产率最大来回答;先求出各自的平衡浓度,然后根据平衡常数的概念来回答;
⑤根据该反应为放热反应,温度升高,平衡向吸热的方向移动,平衡逆向移动,平衡常数减少;
易错点
1、根据温度升高化学平衡向着吸热方向进行
2、根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大。
正确答案
① 低于 ② c ③ n/3 ; 2.08
解析
①反应为放热反应,温度升高化学平衡向着吸热方向进行,从T1到T2反应物氮气的量增加,故T1<T2,故答案为:低于;
②b点代表平衡状态,c点又加入了氢气,故平衡向右移动,氮气的转化率增大,故答案为:c;
③当氮气和氢气的物质的量之比为1:3时达平衡状态时氨的百分含量最大,平衡点时产物的产率最大,据图示,当平衡时氢气的物质的量为n,故加入N2的物质的量为n/3,当n=3mol反应达到平衡时H2的转化率为60%,故起始氮气浓度为1,mol/l,变化的氢气浓度为1.8mol/l,变化的氮气浓度为0.6mol/l,平衡时氮气、氢气、氨气的浓度分别是0.4mol/l、1.2mol/l、1.2mol/l,据K==
考查方向
本题主要考查了热化学方程式;化学平衡建立的过程;化学平衡的调控作用。
解题思路
根据盖斯定律来求反应的焓变,然后根据反应放出的热量与物质的量成正比;
①根据温度升高化学平衡向着吸热方向进行;
②根据增加氢气的物质的量化学平衡向着正反应方向移动;
③根据a、b、c三点所表示的意义来回答;
④根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大;根据化学平衡状态是反应物的转化率最大、生成物的产率最大来回答;先求出各自的平衡浓度,然后根据平衡常数的概念来回答;
⑤根据该反应为放热反应,温度升高,平衡向吸热的方向移动,平衡逆向移动,平衡常数减少;
易错点
1、根据温度升高化学平衡向着吸热方向进行
2、根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大。
正确答案
①0.00592 mol•L-1•s-1
② H2 + CO32--2e- = CO2 + H2O
阳极:N2O4 + 2HNO3 - 2e— = 2N2O5 + 2H+
解析
①500s,c(N2O5)变化量为5.00-3.52=1.48mol/L,则v(N2O5)=1.48mol/L /500s=0.00296mol·L-1·s-1,由速率之比等于化学计量数之比可知,v(NO2)=0.00296mol·L-1·s-1×2=0.00592 mol·L-1·s-1;
②氢氧燃料电池中,氢气做负极,发生失电子成为氢离子的反应,在熔融碳酸盐碳酸钠的作用下,电极反应为:H2 + CO32--2e- = CO2 + H2O;电 解 池 中阳极为与氧气连接的电极,则阳极的反应为N2O4失去电子生成N2O5,电解质为无水硝酸,则电极反应式为N2O4 + 2HNO3 - 2e— = 2N2O5 + 2H+,故答案为① 0.00592 mol•L-1•s-1 ;② H2 + CO32--2e- = CO2 + H2O ;阳极:N2O4 + 2HNO3 - 2e—= 2N2O5+2H+。
考查方向
解题思路
根据盖斯定律来求反应的焓变,然后根据反应放出的热量与物质的量成正比;
①根据温度升高化学平衡向着吸热方向进行;
②根据增加氢气的物质的量化学平衡向着正反应方向移动;
③根据a、b、c三点所表示的意义来回答;
④根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大;根据化学平衡状态是反应物的转化率最大、生成物的产率最大来回答;先求出各自的平衡浓度,然后根据平衡常数的概念来回答;
⑤根据该反应为放热反应,温度升高,平衡向吸热的方向移动,平衡逆向移动,平衡常数减少;
易错点
1、根据温度升高化学平衡向着吸热方向进行
2、根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大。
某化学课外活动小组通过实验研究NO2的性质.
已知:2NO2 + 2NaOH=== NaNO3 + NaNO2 + H2O
任务1:利用下图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去).
21.E装置中制取NO2反应的化学方程式是 .
22.若NO2能够被NH3还原,预期观察到C装置中的现象是 .
23.实验过程中,未能观察到C装置中的预期现象.该小组同学从反应原理的角度分析了原因,认为可能是:
①NH3还原性较弱,不能将NO2还原;
②在此条件下,NO2的转化率极低;
③ .
24.此实验装置存在一个明显的缺陷是 .
25.任务2:探究NO2能否与Na2O2发生氧化还原反应.
实验前,该小组同学提出三种假设.
假设1:二者不反应;
假设2:NO2能被Na2O2氧化;
假设3: .
26.为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如右图所示),重新组装,进行实验.
①装置的合理连接顺序是(某些装置可以重复使用) .
②实验过程中,B装置中淡黄色粉末逐渐变成白色.经检验,该白色物质为纯净物,且无其他物质生成.推测B装置中反应的化学方程式为 .
正确答案
Cu + 4HNO3 (浓) === Cu(NO3)2 + 2NO2↑+ 2H2O
解析
浓硝酸和铜反应生成硝酸铜、二氧化氮和水,反应方程式为:Cu+4HNO3 (浓)═Cu(NO3)2+2NO2↑+2H2O,故答案为:Cu+4HNO3 (浓)═Cu(NO3)2+2NO2↑+2H2O;
考查方向
解题思路
若NO2能够被NH3还原,则混合气体的颜色将变浅;
易错点
1、实验过程分析。
2、本题考查了氮及其化合物性质分析判断。
正确答案
C装置中混合气体颜色变浅(其他合理答案也可)
解析
二氧化氮是红棕色气体,如果能被氨气还原,生成无色气体氮气,则C装置中混合气体颜色变浅,故答案为:C装置中混合气体颜色变浅;
考查方向
解题思路
实验过程中,未能观察到C装置中的预期现象,说明二氧化氮反应的量很少,可能是反应速率降低,或者二氧化氮的转化率较低;
易错点
1、实验过程分析。
2、本题考查了氮及其化合物性质分析判断。
正确答案
在此条件下,该反应的化学反应速率极慢。
解析
造成未能观察到C装置中的预期现象可能原因是:在此条件下,该反应的化学反应速率极慢或NO2的转化率极低导致反应现象变化不明显,故答案为:在此条件下,该反应的化学反应速率极慢;
考查方向
解题思路
铜和浓硝酸反应生成硝酸铜,二氧化氮和水,依据反应写出离子方程式;
二氧化氮是红棕色气体,如果能被氨气还原,生成无色气体氮气,则C装置中混合气体颜色变浅;造成未能观察到C装置中的预期现象可能原因是:在此条件下,该反应的化学反应速率极慢或NO2的转化率极低导致反应现象变化不明显;铜和浓硝酸反应生成硝酸铜,二氧化氮和水,反应写出离子方程式为;Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
易错点
1、实验过程分析。
2、本题考查了氮及其化合物性质分析判断。
正确答案
缺少尾气吸收装置
解析
二氧化氮是有毒气体,氨气是有刺激性气味的气体,所以都不能直接排空,要进行尾气处理才能排空,故答案为:缺少尾气吸收装置;
考查方向
本题主要考查了氮的氧化物的性质及其对环境的影响;性质实验方案的设计.
易错点
1、实验过程分析。
2、本题考查了氮及其化合物性质分析判断。
正确答案
NO2能被Na2O2还原(其他合理答案也可)
解析
Na2O2中O为-1价,可以被NO2氧化,也可以被Na2O2还原,
故答案为:NO2能被Na2O2还原;
考查方向
易错点
1、实验过程分析。
2、本题考查了氮及其化合物性质分析判断。
正确答案
① EDBDF或EDBF ;
② 2NO2 + Na2O2 === 2NaNO3
解析
验证过氧化钠和二氧化氮反应,首先要用E装置制取二氧化氮,因为制取的二氧化氮气体中含有水蒸气,水能和过氧化钠反应而造成干扰,所以要用D装置除去水蒸气,然后较纯净的二氧化氮通过B装置,未反应的二氧化氮有毒不能直接排空,所以最后要进行尾气处理,选用图2装置处理尾气,所以装置的合理连接顺序是EDBDF或EDBF;B装置中淡黄色粉末逐渐变成白色.经检验,该白色物质为纯净物,且无其他物质生成,过氧化钠作氧化剂,则二氧化氮中氮元素失电子化合价升高而作还原剂,所以氮元素只能转化为+5价,且生成物是纯净物,所以是硝酸钠,反应方程式为2NO2+Na2O2═2NaNO3,故答案为:EDBDF或EDBF; 2NO2+Na2O2═2NaNO3.
考查方向
本题主要考查了氮的氧化物的性质及其对环境的影响;性质实验方案的设计.
易错点
1、实验过程分析。
2、本题考查了氮及其化合物性质分析判断。
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g)
一种工业合成氨的简易流程图如下:
28.步骤II中制氢气原理如下:
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是 .
a.升高温度
b.增大水蒸气浓度
c.加入催化剂
d.降低压强
利用反应②,将CO进一步转化,可提高H2产量.若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18mol CO、CO2和H2的混合气体,则CO转化率为 .
27.天然气中的H2S杂质常用氨水吸收,产物为NH4HS.一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式: .
29.图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系.根据图中a点数据计算N2的平衡体积分数: .
30.依据温度对合成氨反应的影响,在图2坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
31.上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是(填序号) ,简述本流程中提高合成氨原料总转化率的方法: .
正确答案
a 90%
解析
反应①CH4(g)+H2O(g)⇌CO2(g)+3H2(g)△H=+206.4 kJ•mol-1,是气体体积增大的吸热反应,一定可以提高平衡体系中H2百分含量,说明平衡正向进行,又能加快反应速率,说明影响反应速率的条件可以是升温、加压、增大浓度等,分析反应特征可知反应正向进行且反应速率增大的只有升温平衡向吸热反应进行,平衡正向进行反应速率增大;a.反应是吸热反应,升高温度,反应速率增大,平衡正向进行,平衡体系中H2百分含量增大,故a符合;b.增大水蒸气浓度,平衡正向进行,反应速率增大,但平衡体系中H2百分含量不一定增大,故b不符合;c.加入催化剂,改变反应速率不改变化学平衡,反应速率增大,氢气百分含量不变,故c不符合;d.降低压强,反应速率减小,平衡逆向进行,氢气百分含量减小,故d不符合;故选a;利用反应②,将CO进一步转化,可提高H2产量,若1mol CO和H2的混合气体(CO的体积分数为20%)中 CO为0.2mol,H2的物质的量为0.8mol,与H2O反应,得到1.18mol CO、CO2和H2的混合气体,依据反应前后气体体积不变,增加的部分应该是起始的水蒸气的物质的量为0.18mol,设转化的一氧化碳的物质的量为x,依据化学平衡三段式列式计算CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41.2 kJ•mol-1起始量(mol) 0.2 0.18+x 0 0.8
变化量(mol) x x x x
平衡量(mol)0.2-x 0.18 x x+0.8则0.2-x+x+x+0.8=1.18 x=0.18则CO转化率为0.18/0.2×100%=90%故答案为:a;90%;
考查方向
本题主要考查了化学反应进行的方向化学平衡硫及其化合物。
解题思路
反应①是气体体积增大的吸热反应,一定可以提高平衡体系中H2百分含量,说明平衡正向进行,又能加快反应速率,说明影响反应速率的条件可以是升温、加压、增大浓度等,分析反应特征可知反应正向进行且反应速率增大的只有升温平衡向吸热反应进行,平衡正向进行反应速率增大,依据平衡移动原理和影响反应速率因素分析判断;依据化学平衡三段式列式计算;
易错点
1、化学平衡影响因素分析,掌握基础是关键。
2、平衡计算应用
3、注意反应特征的计算应用,图像绘制。
正确答案
2NH4HS+O2 2NH3·H2O+2S↓
解析
H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,反应过程中生成一水合氨,依据原子守恒和电子守恒配平书写化学方程式为:2NH4HS+O2==2NH3•H2O+2S;
故答案为:2NH4HS+O2==2NH3•H2O+2S;
考查方向
解题思路
H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,反应过程中生成一水合氨,依据原子守恒和电子守恒配平书写化学方程式;
易错点
1、化学平衡影响因素分析,掌握基础是关键。
2、平衡计算应用
3、注意反应特征的计算应用,图像绘制。
正确答案
14.5%
解析
依据反应特征N2+3H2=2NH3 △V
1 3 2 2
平衡体积 V V
即反应前后气体体积减小为生成氨气的体积,相同条件下,气体体积比等于气体物质的量之比,图象分析可知平衡状态氨气体积含量42%,设平衡混合气体体积为100,氨气为体积42,则反应前气体体积100+42=142,氮气和氢气按照1:3混合,氮气体积=142×1/4=35.5,依据化学方程式计算反应的氮气体积为21,平衡状态氮气为35.5-21=14.5,则氮气体积分数为14.5%;
故答案为:14.5%;
考查方向
解题思路
依据反应特征N2+3H2=2NH3,反应前后气体体积减小为生成氨气的体积,相同条件下,气体体积比等于气体物质的量之比,图象分析可知平衡状态氨气体积含量42%,设平衡混合气体体积为 100,氨气为体积42,计算反应的氮气,依据气体体积比计算原混合气体中氮气体积,得到平衡状态下氮气体积分数;
易错点
1、化学平衡影响因素分析,掌握基础是关键。
2、平衡计算应用
3、注意反应特征的计算应用,图像绘制。
正确答案
解析
合成氨的反应是放热反应,开始反应,氨气物质的量增大,达到平衡状态,继续升温,平衡逆向进行,氨气物质的量减小,画出的图象为:

故答案为:

考查方向
解题思路
依据反应是气体体积减小的放热反应,结合平衡移动原理分析判断;
易错点
1、化学平衡影响因素分析,掌握基础是关键。
2、平衡计算应用
3、注意反应特征的计算应用,图像绘制。
正确答案
Ⅳ 对原料气加压;分离液氨后,未反应的N2、H2循环使用。
解析
分析流程合成氨放热通过Ⅳ热交换器加热反应混合气体,使反应达到所需温度,提高合成氨原料总转化率,依据平衡移动原理分析,对原料气加压、分离出氨气促进平衡正向进行,把平衡混合气体中氮气和氢气重新循环使用,提高原理利用率;故答案为:Ⅳ,对原料气加压,分离液氨,未反应的氮气和氢气循环使用。
考查方向
解题思路
依据反应是气体体积减小的放热反应,结合平衡移动原理分析判断;
易错点
1、化学平衡影响因素分析,掌握基础是关键。
2、平衡计算应用
3、注意反应特征的计算应用,图像绘制。
10.根据元素周期律,由下列事实进行归纳推测,推测不合理的是
正确答案
B
解析
A、Mg、Ca与Ba均属于第ⅡA族,金属性依次增强,与水反应的剧烈程度也变大,正确;
B、半导体是指金属与非金属的交界线处,而不是第ⅣA族的元素,错误;
C、Cl、Br、I均为第ⅦA族元素,非金属性依次减弱,气态氢化物的稳定性依次减弱,正确;
D、Si、P、S为同一周期元素,非金属性依次增大,与氢气反应应依次更加容易,则条件逐渐变得容易,正确;所以答案为B。
考查方向
解题思路
高中化学里 这里的元素性质主要体现在三个方面:
1、金属性与非金属性
越靠左下侧的元素金属性越强,非金属性越弱;越靠右上侧的元素非金属性越强,金属性越弱。
2、原子半径
同周期元素,越靠右的原子半径越小;同族元素,越靠下的原子半径越大。
3、化合价
主族元素化合价=元素所在主族族序数=最外层电子数=价电子数。物理性质(例如熔沸点)是不可以从元素周期表上直接得出结论的。
易错点
1、元素的金属性和非金属性随与原子序数呈现周期性变化。
知识点
12.下列实验的实验目的、图示操作和实验现象均正确的是
正确答案
D
解析
A、淀粉在唾液与硫酸条件下发生水解,会生成葡萄糖,不会遇碘变蓝,错误;
B、二氧化氮转化为四氧化二氮为放热反应,温度高时,平衡右移,二氧化氮浓度增大,颜色加深,所以现象应为右边烧瓶内气体颜色变深,左边烧瓶内气体颜色变浅,错误;
C、图中左试管内液面产生气泡,右试管无明显现象,说明醋酸的酸性强于碳酸,碳酸的酸性强于硼酸,正确;
D、外加电流的阴极保护法,应为电解池,图中为原电池,错误,所以答案为D。
考查方向
本题主要考查了化学实验方案的评价;非金属在元素周期表中的位置及其性质递变的规律;化学平衡;原电池;
解题思路
本题综合考查化学实验基本操作,为高考常见题型,侧重于学生的分析能力、实验能力和评价能力的考查,有利于培养学生的实验能力和学习的积极性,注意把握实验原理以及实验操作方法和注意事项。
易错点
1、温度对化学平衡移动的影响。
2、侧重于学生的分析能力、实验能力。