- 真题试卷
- 模拟试卷
- 预测试卷
2.X、Y、Z、W为四种短周期主族元素,且原子序数依次递增,其中X、Z同族,Y是短周期主族
元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,下列说法正确的是()
正确答案
解析
A、HCl为强酸,Cl﹣不水解,故A错误;
B、Cl元素的最高价氧化物对应水化物的酸性一定强于S,不是最高价氧化物的水化物的酸性不能判断酸性强弱,故B错误;
C、X、Y、Z分别为X为O、Na、S,三种元素形成的化合物由Na2SO3、Na2SO4、Na2S2O3等,故C正确;
D、氢化物的稳定性与共价键有关,与氢键无关,O﹣H键能大于H﹣S键能,所以H2O的稳定性大于H2S,故D错误。
故选C
考查方向
解题思路
X原子的最外层电子数是核外电子层数的3倍,则核外各电子层的电子分别为2、6,应为O元素,X、Z同主族,则Z为S元素,W为短周期元素,而且W的原子序数大于S,所以W为Cl元素,Y是短周期主族元素中原子半径最大的,则Y为Na元素
知识点
4. 一种免疫抑制剂麦考酚酸结构简式如图:
说法不正确的是()
正确答案
解析
A.由结构可知分子式为C17H20O6,故A正确;
B.含酚-OH,能与FeCl3溶液显色,双键与溴水发生加成反应,与浓溴水反应,最多消耗量1 mol Br2,故B正确;
C.酚-OH、-COOH、-COOC-与NaOH反应,则1mol麦考酚酸最多与3 mol NaOH反应,故C正确;
D.该有机物不能发生消去反应,故D错误。
故选D
考查方向
解题思路
由结构可知,分子中含酚-OH、-COOH、碳碳双键、-COOC-,结合酚、羧酸、烯烃及酯的性质来解答.
易错点
分子式写错
知识点
5.向硫酸酸化的Fe( NO3) 3溶液中逐渐通入H2S气体,可能发生反应的离子方程式正确的是()
①S2- +2N03- +4H+=2NO2+S+2H2O
②2Fe3+ +H2S =2Fe2+ +S+2H+
③Fe3+ +3NO3-+5H2S+2H+=3NO+5S +Fe2+ +6H2O
④Fe3+ +7NO3-+10H2S+8H+=7NO +10S+Fe2+ +14H2O
⑤Fe3+ +5NO3- +8H2S +4H+=5NO +8S +Fe2+ +10H2O
正确答案
解析
酸性溶液中,氧化性HNO3>Fe3+,硫化氢不足,硝酸根离子氧化硫化氢,由电子、电荷守恒可知,离子反应为3H2S+2NO3-+2H+=2NO↑+3S↓+4H2O,故①错误,
硫化氢足量,则Fe(NO3)3完全反应,由电子、电荷守恒可知,离子反应为Fe3++3NO3-+5H2S+2H+=3NO↑+5S↓+Fe2++6H2O,故③正确,
当硫化氢将硝酸根全部还原后,再通入硫化氢发生离子反应2Fe3++H2S═2Fe2++S+2H+,故②正确;
当硝酸根离子全部反应,而铁离子部分反应,如铁离子与硝酸根离子的物质的量之比为:1:5时,离子方程式为:Fe3++5NO3-+8H2S+4H+═5NO+8S+Fe2++10H2O,故⑤正确;
而Fe3++7NO3-+10H2S+8H+═7NO+10S+Fe2++14H2O中也是亚铁离子部分反应,但得失电子不守恒,故④错误;
综上所述②③⑤正确,
故选A.
考查方向
解题思路
酸性溶液中,氧化性HNO3>Fe3+,硫化氢不足,硝酸根离子氧化硫化氢;硫化氢足量,则Fe(NO3)3完全反应,以此来解答。
易错点
离子方程式的书写
知识点
1.化学与人类社会的生产、生活有着密切联系。下列叙述中正确的是()
正确答案
解析
A.纸张久置变黄因为纸张纤维间的空隙中会渗入很多霉菌之类的真菌孢子,苹果久置变黄是因为所含二价铁离子被氧化生成三价铁离子,二者原理不相同,故A错误;
B、根据蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性.物理因素有:加热、加压、搅拌、振荡、紫外线照射、超声波等;化学因素有:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等,故高温或日常用的消毒剂可使禽流感病毒蛋白质变性,故B正确;
C、铜活泼性比氢弱,不能将氢气还原出,故不能发生析氢腐蚀,故C错误;
D、重金属盐,能够使蛋白质变性,引起人体中毒,可以服用牛奶或者鸡蛋清等解毒,故D错误。
故选B
考查方向
解题思路
A.纸张久置变黄因为纸张纤维间的空隙中会渗入很多霉菌之类的真菌孢子,苹果久置变黄是因为所含二价铁离子被氧化生成三价铁离子;
B、根据蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性;
C、铜活泼性比氢弱;
D、重金属盐,能够使蛋白质变性。
易错点
基础知识的积累掌握不牢固
知识点
3.常温下,向饱和氯水中逐滴滴入0. 1mol.L-1的氢氧化钠溶液,pH变化如右图所示,下列有关叙述正确的是()
正确答案
解析
A.①为饱和氯水,饱和氯水中存在次氯酸的电离平衡、水的电离平衡和氯气的溶解平衡,故A错误;
B.①到②的过程中,氯水中氢离子浓度逐渐减小,水的电离程度逐渐增大,当氯气和氢氧化钠溶液恰好完全反应时,水的电离程度达到最大,此时溶质为氯化钠和次氯酸钠,溶液呈碱性,而②点为中性,说明②到③的过程中水的电离程度先增大,之后氢氧化钠过量后水的电离程度开始减小,故B错误;
C.当氯气与氢氧化钠溶液恰好反应时生成氯化钠、次氯酸钠和水,次氯酸根离子部分水解,溶液呈碱性,而②的pH=7,为中性溶液,说明氯水稍过量,二者没有恰好反应,故C错误;
D.②点溶液中溶质为NaCl、NaClO、HClO,溶液呈中性,则c(H+)=c(OH﹣),根据电荷守恒得:c(H+)+c(Na+)=c(Cl﹣)+c(ClO﹣)+c(OH﹣),所以c(Na+)=c(Cl﹣)+c(ClO﹣),由电物料守恒可得:c(Cl﹣)=c(ClO﹣)+c(HClO),所以c(Na+)=c(HClO)+2c(ClO﹣),故D正确。
故选D.
考查方向
解题思路
A.①点所示溶液中只存在HCl0的电离平衡、氯气的溶解平衡和水的电离平衡;
B.当氯气与氢氧化钠溶液恰好反应生成氯化钠、次氯酸钠和水时,水的电离程度达到最大,而②点pH=7,说明②到③的过程中水的电离程度先最大后减少;
C.当恰好反应时溶液显示碱性,而②点为中性;
D.②点溶液呈中性,则c(H+)=c(OH﹣),根据电荷守恒得c(H+)+c(Na+)=c(Cl﹣)+c(ClO﹣)+c(OH﹣),所以c(Na+)=c(Cl﹣)+c(ClO﹣),由电子转移守恒c(Cl﹣)=c(ClO﹣)+c(HClO),联立计算判断。
知识点
含氮化合物的研发与绿色反展、经济可持续发展有着密切关联。
13.氨是一种重要化工原料。合成氨原料气H2,可用天然气为原料制得,有关反应能量变
化如下图所示。
则用CH4(g)和H20(g)反应制得H2(g)和CO(g)的热化学方程式为: 。
14.氮的氧化物有着广泛用途,又是环境的污染物。
(i)在150C时,将0.4mol NO2气体充人体积为2L的真空密闭容器中,发生反应:
2NO2(g)-
每隔一定时间测定容器内各物质的物质的量,数据如下表:
①当反应在1500C达到平衡时,该反应平衡常数K=____。(填数值)
②若最初通人N2O4,在相同条件下达到平衡时,各物质浓度仍然相同,则N2O4的起始浓度
应为____。
(ii)氨氧化制HN03的尾气中含有NO和N02,且n(NO):n(N02) =1:1,可用尿素溶液除
去,其作用原理是:N02和NO与水反应生成亚硝酸,亚硝酸再与尿素反应生成对环境无污
染的物质。若用1mol尿素吸收该尾气,则能吸收氮氧化物 g。
15.氨气,CO2在一定条件下可合成尿素,其反应为:2NH3(g)+CO2(g)-CO( NH2)2(s)+H2O(g)右图表示合成塔中氨碳比a与CO2转化率ω的关系。a为[n(NH3)/n(CO2)],b为水碳比[n(H20)/n(CO2)]。则:
①b应控制在____; A.1.5. 1.6 B.1~1.1 C.0.6~0.7
②a应控制在4.0的理由是____ 。
正确答案
CH4(g)+H2O(g)
解析
分别根据图像1、2、3来写出热化学方程式,然后根据盖斯定律来分析。
考查方向
解题思路
根据相关反应计算
易错点
化学平衡的相关计算
正确答案
(i)①2.8 ②0.10mol/L
(ii)76g
解析
(i)①根据方程式可得n₁=0.3mol,n₂=0.07mol,n₃=0.24mol,n4=0.24mol,根据NO2的平衡浓度为0.12mol/L,N2O4为0.12mol/L来计算
②根据反应 2NO2
考查方向
解题思路
根据相关反应计算
易错点
化学平衡的相关计算
正确答案
①C
②a等于4.0, CO2转化率迅速提高到最大值;而a在4.0之后增大,c(NH3)转化率无明显增大。
解析
根据氨碳比相同时,水碳比为0.6~0.7时,二氧化碳转化率最大,根据氨碳比大于4时,增大氨气的物质的量,二氧化碳的转化率增加不大,增加了成本;氨碳比大于4时,二氧化碳转化率较小。
考查方向
解题思路
根据相关反应计算
易错点
化学平衡的相关计算
某实验研究小组欲检验草酸晶体分解的产物并测定其纯度(杂质不发生反应)。查阅资
料:草酸晶体( H2C204·2H20) l00℃开始失水,101. 5C熔化,150℃左右分解产生H2O、CO和
C02。下面是可供选择的实验仪器(图中某些加热装置已略去),实验所需药品不限。
8. 最适宜加热分解革酸晶体的装置是C。若选装置A可能会造成的后果是 ;
若选装置B可能会造成的后果是 。
9.三种气体检验的先后次序是____(填编号)。
A. CO2 、H2O、CO
B.CO、H2O、CO2
C.H2O、CO2、CO
D.H2O、CO、CO2
10.实验利用装置“G(碱石灰)-F-D(CuO固体)-F”检验CO,则F中盛装的试剂是
__ _,证明含有CO的现象是 ____。
11.把分解装置与装有NaOH溶液的E装置直接组合,测量完全分解后所得气体的体积,
测定ag草酸晶体的纯度。经实验得到气体的体积为V mL(已换算成标准状况),则草酸
纯度的表达式为____ 。
12.请设计实验方案测量草酸二级电离平衡常数Ka2的值: ____,并根据方案中测得的物理量,写出计算Ka2的表达式 。
正确答案
固体药品熔化后会流到试管口
冷凝水会倒流到试管底,造成试管破裂
解析
最适宜加热分解革酸晶体的装置是C.若选装置A可能会造成的后果是固体药品熔化后会流到试管口,若选装置B可能会造成的后果是冷凝水会倒流到试管底,造成试管破裂。
故答案为:固体药品熔化后会流到试管口;冷凝水会倒流到试管底,造成试管破裂
考查方向
解题思路
草酸晶体的熔点低,受热容易熔化,用C装置加热分解革酸晶体,熔融的固体不易流下,适用于加热草酸,若选择装置A加热会使固体熔融物溶化后流到试管口处,若选择装置B分解生成的水会倒流试管底部炸裂试管。
易错点
电离平衡常数掌握不熟
正确答案
C
解析
150℃左右分解产生H2O、CO和C02,三种气体的检验顺序应遵循现象明显且不相互干扰,应先检验水,再检验二氧化碳,最后检验一氧化碳。
故答案为:C
考查方向
解题思路
150℃左右分解产生H2O、CO和C02,三种气体的检验顺序应遵循现象明显且不相互干扰,应先检验水,再检验二氧化碳,最后检验一氧化碳。
易错点
电离平衡常数掌握不熟
正确答案
澄清的石灰水
前一个F中没有浑浊,后一个F中有沉淀;D中固体反应后从黑色变成红色。
解析
实验利用装置“G(碱石灰)﹣F﹣D(CuO固体)﹣F”检验CO,通过装置G吸收水和二氧化碳,通过装置F检验二氧化碳是否除净,通过装置D检验是否有一氧化碳含有氧化铜为铜,最后通过装置F检验是否生成二氧化碳气体。
故答案为:澄清的石灰水;前一个F中没有浑浊,后一个F中有沉淀,D中固体反应后从黑色变成红色
考查方向
解题思路
实验利用装置“G(碱石灰)﹣F﹣D(CuO固体)﹣F”检验CO,通过装置G吸收水和二氧化碳,通过装置F检验二氧化碳是否除净,通过装置D检验是否有一氧化碳含有氧化铜为铜,最后通过装置F检验是否生成二氧化碳气体。
易错点
电离平衡常数掌握不熟
正确答案
解析
反应的化学方程式为:H2C2042H203H2O+CO+C02,实验得到气体的体积为VmL(已换算成标准状况),为一氧化碳,物质的量和草酸晶体物质的量相同,n(H2C2042H20)=n(CO)=mol/L,
草酸纯度的表达式=
故答案为:
考查方向
解题思路
草酸晶体(H2C2042H20)l00℃开始失水,101.5C熔化,150℃左右分解产生H2O、CO和C02.反应的化学方程式为:H2C2042H203H2O+CO+C02,实验得到气体的体积为VmL(已换算成标准状况),为一氧化碳,物质的量和草酸晶体物质的量相同,据此计算。
易错点
电离平衡常数掌握不熟
正确答案
常温时,用pH计测量0.100 mol/L 草酸钠溶液的pH,则c(OH-)=Kw/c(H+)
依据 C2O42-+H2O
或

解析
常温时,用pH计测量0.100mol/L草酸钠溶液的pH,则c(OH-)=Kw/c(H+)
依据 C2O42-+H2O
或

考查方向
解题思路
常温时,用pH计测量0.100mol/L草酸钠溶液的pH,依据水解平衡C2O42﹣+H2O?HC2O4﹣+OH﹣,计算平衡常数。
易错点
电离平衡常数掌握不熟
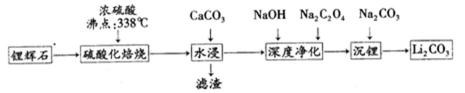
碳酸锂(相对分子质量74)广泛应用于化工、冶金、陶瓷、医药、制冷、焊接、锂合金等行业。制备流程如下:
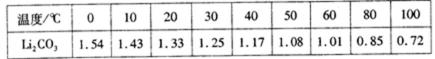
已知:碳酸锂的溶解度为( g/L)
16.锂辉石(Li2Al2Si4Ox)可以用氧化物的形式表示其组成,形式为____ 。
17.硫酸化焙烧工业反应温度控制在250 - 300℃,主要原因是_______ _;同时,硫
酸用量为理论耗酸量的115%左右,硫酸如果加入过多则 (填入选项代号)。
A.增加酸耗量
B.增加后续杂质的处理量
C.增加后续中和酸的负担
18.水浸时,需要在搅拌下加入石灰石粉末的主要作用是________。
19.“沉锂”的化学反应方程式为 。
20.“沉锂”需要在95℃以上进行,主要原因是 。过滤碳酸锂所得母液
中主要含有硫酸钠,还可能含有____和______。
正确答案
Li2O·Al2O3·4SiO2
解析
锂辉石(Li2Al2Si4Ox)可以用氧化物的形式表示,其组成形式为:Li2O·Al2O3·4SiO2,
故答案为:Li2O·Al2O3·4SiO2
考查方向
解题思路
锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出。
易错点
本题是对学生综合能力的考查,关键是对工艺流程的理解,难度较大
正确答案
温度低于250℃,反应速率较慢
解析
温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多,反应温度控制在250﹣300℃,反应速率较快,避免硫酸挥发;
硫酸如果加入过多,消耗的酸多,后续中还需要除去过量的硫酸,增加后续杂质的处理量、增加后续中和酸的负担。
故答案为:温度低于250℃,反应速率较慢,温度高于300℃,硫酸挥发较多;ABC
考查方向
解题思路
锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出。
易错点
本题是对学生综合能力的考查,关键是对工艺流程的理解,难度较大
正确答案
除去多余的硫酸,同时调整pH,除去大部分杂质。
解析
加入碳酸钙除去未反应的硫酸,同时调节溶液pH值,除去大部分杂质。
故答案为:除去多余的硫酸,同时调整pH,除去大部分杂质
考查方向
解题思路
锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出。
易错点
本题是对学生综合能力的考查,关键是对工艺流程的理解,难度较大
正确答案
Na2CO3+Li2SO4=Li2CO3↓+Na2SO4
解析
“沉锂”过程是碳酸钠与Li2SO4反应生成Li2CO3,反应方程式为:Na2CO3+Li2SO4=Li2CO3↓+Na2SO4故答案为:Na2CO3+Li2SO4=Li2CO3↓+Na2SO4
考查方向
解题思路
锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出。
易错点
本题是对学生综合能力的考查,关键是对工艺流程的理解,难度较大
正确答案
温度越高,碳酸锂溶解度降低,可以增加产率
碳酸钠、碳酸锂
解析
温度越高,碳酸锂溶解度降低,减少碳酸锂溶解,可以增加产率;溶液中硫酸钠不反应,使用的碳酸钠要过量,少量碳酸锂溶解在溶液中,过滤碳酸锂所得母液中主要含有硫酸钠,还可能含有碳酸钠、碳酸锂,故答案为:温度越高,碳酸锂溶解度降低,可以增加产率。
考查方向
解题思路
锂辉石加硫酸,浸取焙烧,氧化铝、氧化锂溶解,二氧化硅不反应,水浸时加入碳酸钙,除去为反应的硫酸,同时调节溶液pH值,可以将Al3+转化为Al(OH)3沉淀,过滤除去不溶物,滤液再进行深度净化后主要为Li2SO4、Na2SO4,最后加入Na2CO3,转化为溶解度更小Li2CO3析出。
易错点
本题是对学生综合能力的考查,关键是对工艺流程的理解,难度较大
【化学一选修2:化学与技术】
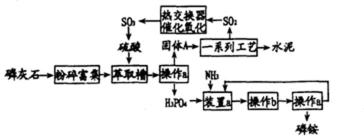
最近,我国利用生产磷铵排放的废渣磷灰石制取硫酸并联产水泥的技术研究获得成功。具
体生产流程如图:
回答下列问题:
21.实验室中进行操作a所需的玻璃仪器有____、 和____,在实验室中操作b的名称是____。
22.装置a中生成两种酸式盐,它们的化学式分别是________。
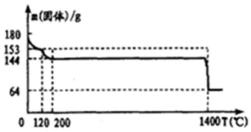
23.固体A为生石膏(CaSO4.2H2O)和不含结晶水且高温时也不分解的杂质。
①实验中每次对固体称量时须在冷却后进行。为保证实验结果的精确性,固体冷却时必须防止____
②将加热到1400℃时生成的气体通人品红溶液中,品红褪色。写出1400℃时的化学反应方程式:
。
③固体A中生石膏的质量百分含量=____。
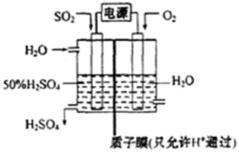
24.科学家研究出如图所示装置,用电化学原理生产硫酸的新工艺,其阳极的电极反应式为: 。
正确答案
烧杯 漏斗 玻璃棒 蒸发浓缩、冷却结晶
解析
分离固体和液体的方法是过滤;过滤需要盛放药品的烧杯、过滤的漏斗、引流作用的玻璃棒、固定漏斗的铁架台(含铁圈)、滤纸等,此操作需要玻璃仪器:烧杯、漏斗、玻璃棒;
从溶液中析出晶体的方法是:将溶液蒸发浓缩、冷却结晶可得相应晶体。
故答案为:烧杯、漏斗、玻璃棒;蒸发浓缩、冷却结晶
考查方向
解题思路
操作a是把固体与液体分开,应为过滤;过滤需要烧杯、漏斗、玻璃棒、铁架台(含铁圈)、滤纸等;操作b是由溶液中析出晶体,应萃取蒸发浓缩、冷却结晶等操作.磷酸受热容易分解,在结晶时应采用低温蒸发结晶。
易错点
化学计算、电解原理应用
正确答案
(NH4)2HPO4 NH4H2PO4
解析
装置a中磷酸与氨气发生反应,磷酸是三元酸,可以生成(NH4)3PO4、(NH4)2HPO4、NH4H2PO4三种盐,其中(NH4)2HPO4、NH4H2PO4两种酸式盐,
故答案为:(NH4)2HPO4、NH4H2PO4
考查方向
解题思路
装置a中磷酸与氨气发生反应,可以生成(NH4)3PO4、(NH4)2HPO4、NH4H2PO4
易错点
化学计算、电解原理应用
正确答案
①对失水后的晶体进行冷却时必须防止吸水,否则会导致结果有误差
②2CaSO4 1400℃ 2CaO+2SO2↑+O2↑
③95.6%
解析
①对失水后的晶体进行冷却时必须防止吸水,否则会导致结果有误差。
故答案为:对失水后的晶体进行冷却时必须防止吸水,否则会导致结果有误差
②200℃加热反应完全失去结晶水得到硫酸钙,1400℃加热硫酸钙,得到能使品红溶液褪色的气体为二氧化硫,S元素化合价降低,则有氧气生成,硫酸钙分解生成氧化钙、二氧化硫与氧气,反应方程式为:2CaSO4 1400℃ 2CaO+2SO2↑+O2↑,
故答案为:2CaSO4 1400℃ 2CaO+2SO2↑+O2↑
③200℃加热反应完全失去结晶水得到硫酸钙,固体减轻质量总为180g﹣44g=36g,为结晶水总质量,
设固体A中含有生石膏的质量为m,则:
CaSO4•2H2O=CaSO4+2H2O
172 36
m 36g
所以m==172g
所以固体A中生石膏的质量分数=×100%=95.6%,
故答案为:95.6%
考查方向
解题思路
①对失水后的晶体进行冷却时必须防止吸水
②200℃加热反应完全失去结晶水得到硫酸钙,1400℃加热硫酸钙,得到能使品红溶液褪色的气体为二氧化硫,S元素化合价降低,则有氧气生成,硫酸钙分解生成氧化钙、二氧化硫与氧气;
③200℃加热反应完全失去结晶水得到硫酸钙,固体减轻质量总为180g﹣44g=36g,为结晶水总质量,由CaSO4•2H2O=CaSO4+2H2O计算CaSO4•2H2O的质量,进而计算其含量。
易错点
化学计算、电解原理应用
正确答案
SO2-2e-+2H2O==SO42-+ 4H+
解析
阳极发生氧化反应,由电解池示意图可知,二氧化硫在阳极失去电子,氧化得到硫酸,阳极电极反应式为:SO2﹣2e﹣+2H2O═SO42﹣+4H+,
故答案为:SO2-2e-+2H2O==SO42-+ 4H+
考查方向
解题思路
阳极发生氧化反应,由电解池示意图可知,二氧化硫在阳极失去电子,氧化得到硫酸。
易错点
化学计算、电解原理应用