- 真题试卷
- 模拟试卷
- 预测试卷
化学促进了科技进步和社会发展。下列叙述中没有涉及化学变化的是( )
正确答案
下列说法错误的是( )
正确答案
聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是( )
正确答案
化学实验操作是进行科学实验的基础。下列操作符合规范的是( )
正确答案
科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是( )
正确答案
甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
新法合成的反应:
下列说法错误的是(阿伏加德罗常数的值为
正确答案
铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )
正确答案
海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是( )
正确答案
科学家发现某些生物酶体系可以促进



下列说法正确的是( )
正确答案
室温时,用







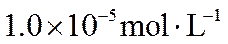



下列说法正确的是( )
正确答案
为探究



依据上述实验现象,结论不合理的是( )
正确答案
向体积均为



正确答案
下列离子方程式正确的是( )
正确答案
反应物(S)转化为产物(P或
下列有关四种不同反应进程的说法正确的是( )
正确答案
某实验小组以


可选用试剂:




步骤1.
按如图所示装置进行实验,得到

步骤2.产品中
①称取产品

②在不断搅拌下,向①所得溶液逐滴加入热的
③沉淀完全后,

回答下列问题:
(1)Ⅰ是制取______________气体的装置,在试剂a过量并微热时,发生主要反应的化学方程式为______________;
(2)Ⅱ中b仪器的作用是______________;Ⅲ中的试剂应选用______________;
(3)在沉淀过程中,某同学在加入一定量热的
(4)沉淀过程中需加入过量的
(5)在过滤操作中,下列仪器不需要用到的是______________(填名称);
(6)产品中
正确答案
(1)①. HCl ②. H2SO4(浓)+NaCl
(2) ①. 防止倒吸 ②. CuSO4溶液
(3)静置,取上层清液于一洁净试管中,继续滴加硫酸溶液,无白色沉淀生成,则已沉淀完全
(4)使钡离子沉淀完全
(5)锥形瓶 (6)97.6%
2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的


Ⅰ.
Ⅱ.
①下列说法正确的是______________;
A)平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B)混合气体的密度保持不变时,说明反应体系已达到平衡
C)平衡时
D)将炭块粉碎,可加快反应速率
②反应平衡时,


(2)一种脱除和利用水煤气中
①某温度下,吸收塔中





②再生塔中产生
③利用电化学原理,将

正确答案
(1)①. BD ②. 吸收 ③. 31.2 ④.
(2) ①. 10 ②. 2

钛(



已知“降温收尘”后,粗
回答下列问题:
(1)已知





正确答案
(1)C (2) ①. 5TiO2+6C+10Cl2
(3) ①. 3VOCl3+Al=3VOCl2+AlCl3 ②. 蒸馏
(4) ①. 不能 ②. 若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质; (5)AC
[选修3:物质结构与性质](15分)
铁和硒(
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态

②该新药分子中有______________种不同化学环境的C原子;
③比较键角大小:气态

(2)富马酸亚铁
①富马酸分子中

②富马酸亚铁中各元素的电负性由大到小的顺序为______________。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化


①产物中N原子的杂化轨道类型为______________;
②与
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为______________;
②
③该晶胞参数



正确答案
(1) ①. [Ar] 3d104s24p4 ②. 6 ③. > ④. SeO3的空间构型为平面三角形,SeO
(2)①. 11:3 ②. O>C>H>Fe
(3) ①. sp3杂化 ②. H2O
(4) ①. KFe2Se2 ②. 4 ③.
[选修5:有机化学基础](15分)
物质J是一种具有生物活性的化合物。该化合物的合成路线如下:
已知:①
②
回答下列问题:
(1)A中官能团的名称为______________、______________;
(2)

(3)B的结构简式为______________;
(4)
(5)

(6)I中的手性碳原子个数为______________(连四个不同的原子或原子团的碳原子称为手性碳原子);
(7)参照上述合成路线,以


正确答案
(1)①. 醚键 ②. 醛基
(2)①. 取代反应 ②. 加成反应
(3)
(4)
(5) ①. 5 ②.
(6)1 (7)
























































































