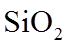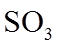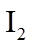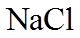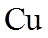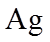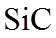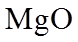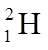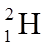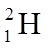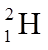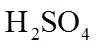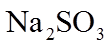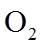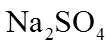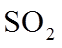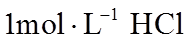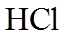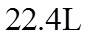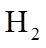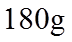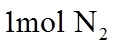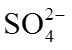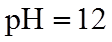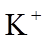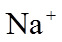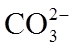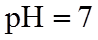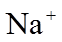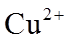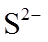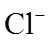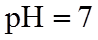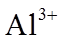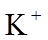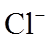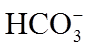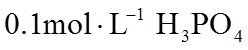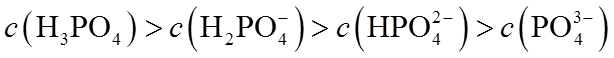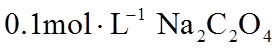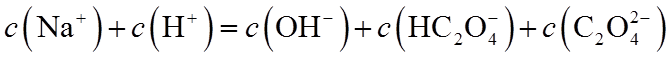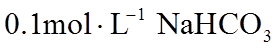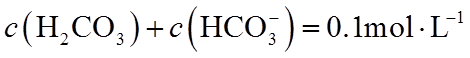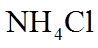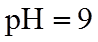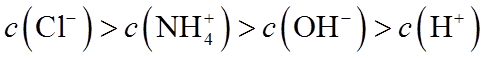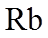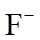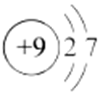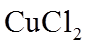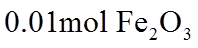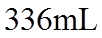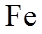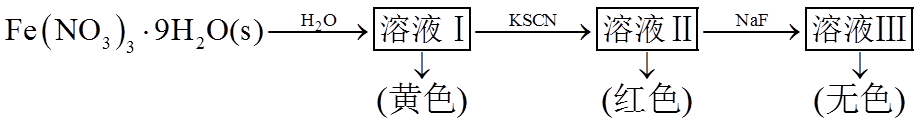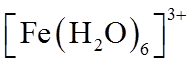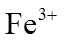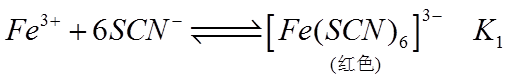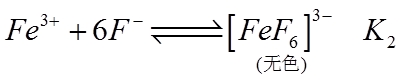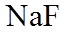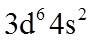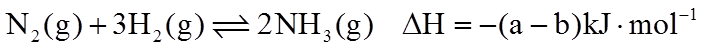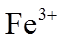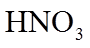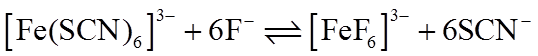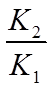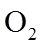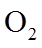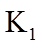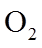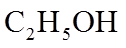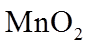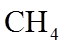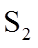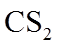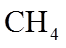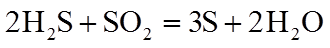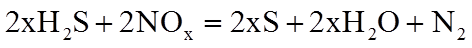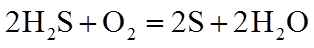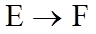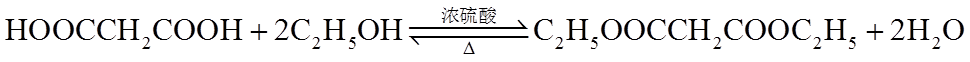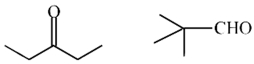- 真题试卷
- 模拟试卷
- 预测试卷
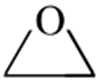
2.下列各组物质的晶体类型相同的是( )
正确答案
3.核聚变发电有望成为解决人类能源问题的重要手段之一。氘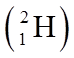
正确答案
4.关于反应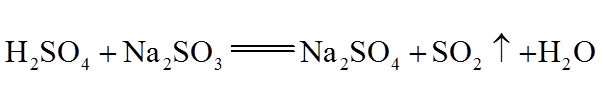
正确答案
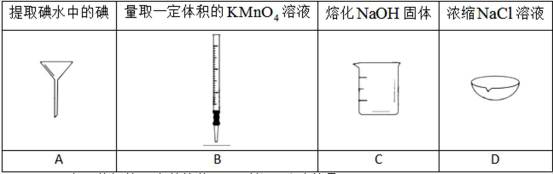
6.进行下列实验操作时,选用仪器正确的是( )
正确答案
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
正确答案
8.最理想的“原子经济性反应”是指反应物的原子全部转化为期望的最终产物的反应。下列属于最理想的“原子经济性反应”的是( )
正确答案
9.常温下,下列各组离子在给定溶液中能大量共存的是( )
正确答案
10.常温下,下列有关电解质溶液的叙述正确的是( )
正确答案
1.近年我国在科学技术领域取得了举世瞩目的成就。对下列成就所涉及的化学知识的判断错误的是( )
正确答案
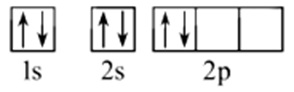
5.下列化学用语表达正确的是( )
正确答案
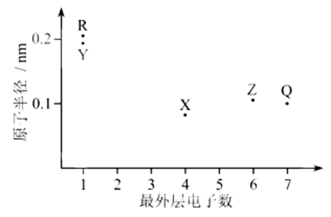
12.元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。下列判断正确的是( )
正确答案
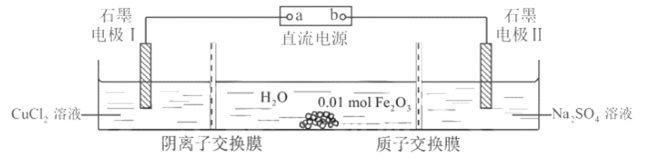
11.如下所示电解装置中,通电后石墨电极Ⅱ上有
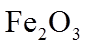
正确答案
13.(14分)铁单质及其化合物的应用非常广泛。
(1)基态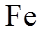
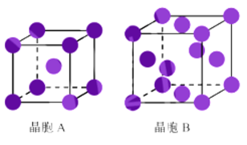
(2)用X射线衍射测定,得到
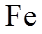
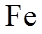
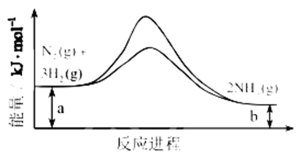
(3)合成氨反应常使用铁触媒提高反应速率。右图为有、无铁触媒时,反应的能量变化示意图。写出该反应的热化学方程式_________。从能量角度分析,铁触媒的作用是________________________。
(4)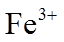
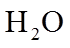

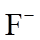
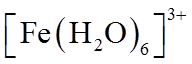
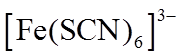
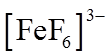
①
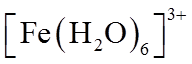
②已知
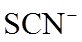
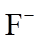

向溶液Ⅱ中加入
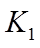
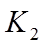
正确答案
(1)
降低反应活化能
(4)①由
②
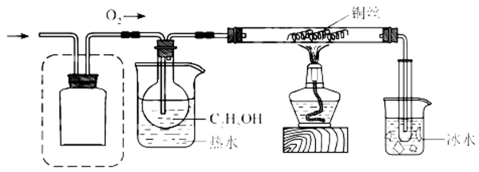
15.(18分)某化学小组同学利用一定浓度的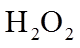

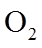
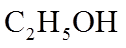
Ⅰ.制备
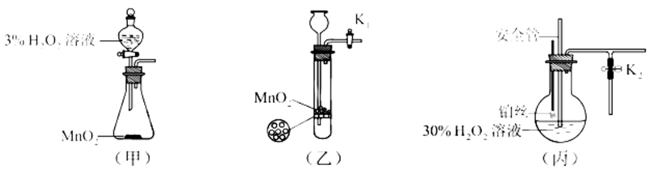
该小组同学设计了如下气体发生装置(夹持装置省略)
(1)甲装置中主要仪器的名称为________。
(2)乙装置中,用粘合剂将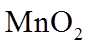

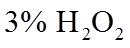
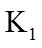
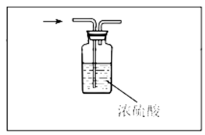
(3)丙装置可用于制备较多
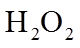
(4)丙装置的特点是____________(填序号)。
a.可以控制制备反应的开始和结束
b.可通过调节催化剂与液体接触的面积来控制反应的速率
c.与乙装置相比,产物中的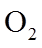
Ⅱ.氧化
该小组同学设计的氧化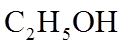
(5)在图中方框内补全干燥装置和干燥剂。
Ⅲ.检验产物
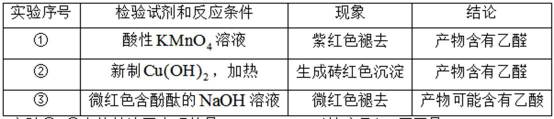
(6)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论.
实验①~③中的结论不合理的是____________(填序号),原因是_______________。
正确答案
(1)分液漏斗 锥形瓶
(2)刚好没过
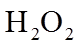
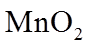
(3)液面上升 打开弹簧夹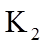
(5)
(6)① 乙醇也能使酸性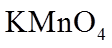
16.(14分)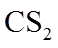
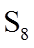

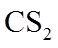
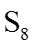
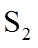
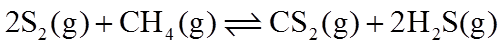
(1)
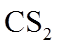
(2)某温度下,若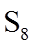

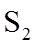
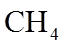
①当
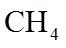
②当以下数值不变时,能说明该反应达到平衡的是________(填序号)。
a.气体密度 b.气体总压 c.
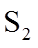
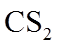
(3)一定条件下,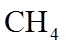
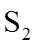
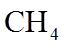

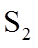
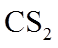
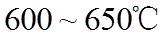
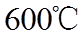
(4)用燃煤废气(含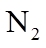
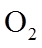

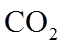
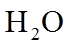
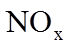
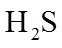
正确答案
(1)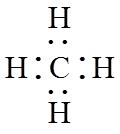

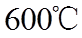
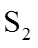
(4)
写出任意一个,或者其他合理答案均可
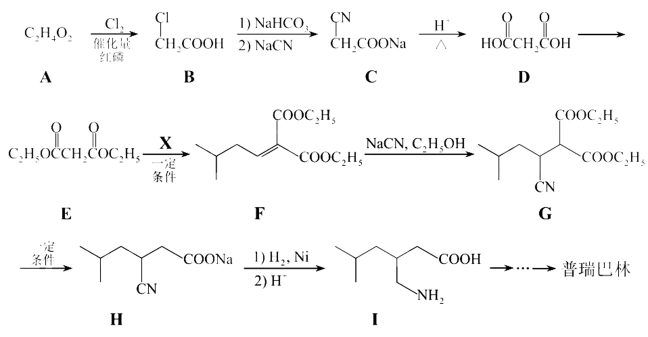
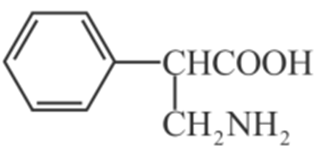
14.(18分)普瑞巴林能用于治疗多种疾病,结构简式为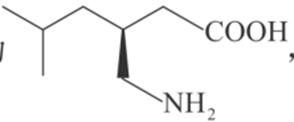
(1)普瑞巴林分子所含官能团的名称为_________。
(2)化合物A的命名为_________。
(3)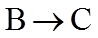
(4)写出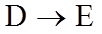
(5)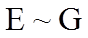
(6)
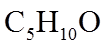
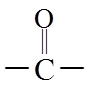
(7)参考以上合成路线及反应条件,以
正确答案
(1)羧基 氨基 (2)乙酸 (3)取代反应
(4)
(5)G (6)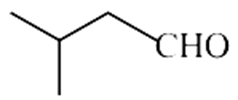
(7)