- 真题试卷
- 模拟试卷
- 预测试卷
2.下列叙述不涉及氧化还原反应的是
正确答案
3.短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数是其最高能级电子数的2倍,Z可与X形成淡黄色化合物Z2X2,Y、W最外层电子数相同。下列说法正确的是
正确答案
6.从中草药中提取的 calebin A(结构简式如下)可用于治疗阿尔茨海默症。下列关于 calebin A的说法错误的是
正确答案
10.微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用下图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
正确答案
1.实验室中下列做法错误的是
正确答案
4.下列关于C、Si及其化合物结构与性质的论述错误的是
正确答案
5.利用下列装置(夹持装置略)进行实验,能达到实验目的的是
正确答案
7.B3N3H6(无机苯)的结构与苯类似,也有大π键。下列关于B3N3H6的说法错误的是
正确答案
8.实验室分离Fe3+和Al3+的流程如下:
已知Fe3+在浓盐酸中生成黄色配离子[FeCl4]-,该配离子在乙醚(Et2O,沸点34.6℃)中生成缔合物
正确答案
9.以菱镁矿(主要成分为MgCO3,含少量SiO2/Fe2O3和Al2O3)为原料制备高纯镁砂的工艺流程如下:
已知浸出时产生的废渣中有SO2、Fe(OH)3和Al(OH)3。下列说法错误的是
正确答案
12.α-氰基丙烯酸异丁酯可用作医用胶,其结构简式如下。下列关于α-氰基丙烯酸异丁酯的说法错误的是
正确答案
13.采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图所示。忽略温度变化的影响,下列说法错误的是
正确答案
14.1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(
正确答案
15.25℃时,某混合溶液中
正确答案
11.下列操作不能达到实验目的的是
正确答案
17.(12分)CdSnAs2是一种高迁移率的新型热电材料,回答下列问题:
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为 ,其固体的晶体类型为 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为 (填化学式,下同),还原性由强到弱的顺序为 ,键角由大到小的顺序为 。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示, 1mol该配合物中通过螯合作用形成的配位键有 mol,该螯合物中N的杂化方式有 种。
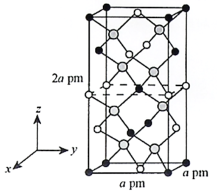
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
一个晶胞中有 个Sn,找出距离Cd(0,0,0)最近的Sn (用分数坐标表示)。CdSnAs2晶体中与单个Sn键合的As有 个。
正确答案
(1)正四面体形;分子晶体
(2)NH3、AsH3、PH3;AsH3、PH3、NH3;NH3、PH3、AsH3
(3)6;1
(4)4;(0.5,0,0.25)、(0.5,0.5,0);4
18.(12分)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ. 
Ⅱ. 
Ⅲ. 
回答下列问题:
(1)
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2O(g)的浓度为 mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为 。
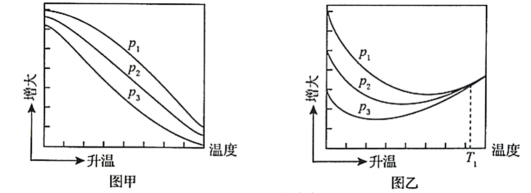
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:CO2的平衡转化率=
正确答案
(1)+40.9
(2)
(3)乙;p1、p2、p3;T1时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡没有影响
(4)A
20.(12分)某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1)装置A中a的作用是 ;装置C中的试剂为 ;装置A中制备Cl2的化学方程式为 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是 。
(3)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入 (填“酸式”或“碱式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO4溶液起始读数为15.00mL,此时滴定管中KMnO4溶液的实际体积为 (填标号)。
正确答案
(1)平衡气压,使浓盐酸顺利滴下; NaOH溶液;
(2)在装置A、B之间加装盛有饱和食盐水的洗气瓶
(3)酸式;C
(4)
16.(12分)用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下:
已知:MnO2是一种两性氧化物;25℃时相关物质的Ksp见下表。
回答下列问题:
(1)软锰矿预先粉碎的目的是 ,MnO2与BaS溶液反应转化为MnO的化学方程式为 。
(2)保持BaS投料量不变,随MnO2与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是 。
(3)滤液I可循环使用,应当将其导入到 操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为 (填化学式)。再使用氨水调溶液的pH,则pH的理论最小值为_______(当溶液中某离子浓度
(5)碳化过程中发生反应的离子方程式为 。
正确答案
(1)增大接触面积,充分反应,提高反应速率;
(2)过量的MnO2消耗了产生的Ba(OH)2
(3)蒸发
(4)H2O2;4.9
(5)
19.(12分)化合物F是合成吲哚-2-酮类药物的一种中间体,其合成路线如下:
知:Ⅰ.
Ⅱ.
Ⅲ.
正确答案
(1)
及时蒸出产物(或增大乙酸或乙醇的用量);
(2)取代反应;羰基、酰胺基
(3)CH3COCH2COOH;
(4)