- 真题试卷
- 模拟试卷
- 预测试卷
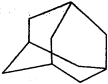
9.下图是金刚烷的结构示意图,1-溴金刚烷可用于合成甲型流感病毒的抑制剂。下列有关说法中正确的是
正确答案
解析
A.从金刚烷的结构简式可以看出金刚烷的分子式为C10H16,金刚烷分子中有10个碳原子,A错误;
B.从金刚烷的结构简式可以看出金刚烷分子含有2种等效氢原子,因此1-溴金刚烷的结构有两种,B正确;
C.烷烃的同系物的通式为:CnH2n+2,金刚烷不属于烷烃的同系物,C错误;
D.金刚烷所有的碳原子都是饱和的,不具有芳香烃相似的化学性质,D错误。
故选B。
考查方向
解题思路
A.从金刚烷的结构简式可以看出金刚烷的分子式为C10H16,金刚烷分子中有10个碳原子;
B.从金刚烷的结构简式可以看出金刚烷分子含有2种等效氢原子,因此1-溴金刚烷的结构有两种;
C.烷烃的同系物的通式为:CnH2n+2,金刚烷不属于烷烃的同系物;
D.金刚烷所有的碳原子都是饱和的,不具有芳香烃相似的化学性质。
易错点
解题注意金刚烷的结构简式可以看出金刚烷分子含有2种等效氢原子。
知识点
10.下列有关对如图所示铜锌原电池装置叙述正确的是
正确答案
解析
A.阳离子交换膜只能通过阳离子,该电池通过阳离子的移动,保持溶液中电荷平衡,A正确;
B.电池工作时,电子从锌极流向铜极,电流表指示出从Zn极到Cu极的电子流动方向,B错误;
C.电池工作过程中,硫酸根离子不能通过阳离子交换膜,乙池的c(SO42-)不变,C错误;
D.电池工作一段时间后,甲池中产生的锌离子通过阳极交换膜进入乙池,保持溶液中电荷平衡,溶液质量基本不变,D错误;
故选A。
考查方向
解题思路
A.阳离子交换膜只能通过阳离子,该电池通过阳离子的移动,保持溶液中电荷平衡;
B.电池工作时,电子从锌极流向铜极,电流表指示出从Zn极到Cu极的电子流动方向;
C.电池工作过程中,硫酸根离子不能通过阳离子交换膜,乙池的c(SO42-)不变;
D.电池工作一段时间后,甲池中产生的锌离子通过阳极交换膜进入乙池,保持溶液中电荷平衡,溶液质量基本不变;
易错点
本题考查了原电池原理,根据电极上得失电子确定正负极,原电池概念来分析解答,题目难度不大。
知识点
11.常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列说法中正确的是
正确答案
解析
A.该现象说明了NaHCO3溶解度相对与氯化铵等物质较小,NaHCO3可溶于水,A错误;
B.溶液中存在物料守恒,即:c(Na)=c(C),则:c(Na+)=c(HCO3﹣)+c(CO32﹣)+c(H2CO3),HCO3-水解程度大于电离程度,因此滤液中的c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-),B错误;
C.根据电荷守恒,滤液中c(Na+)+c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-),C错误;
D.滤液中剩余的溶质主要是少量碳酸氢铵和氯化铵,铵根离子水解,浓度小于氯离子,但水解程度较小,仍然大于碳酸氢根离子,铵根离子水解大于碳酸氢根离子水解,溶液显酸性,因此c(Cl-)>c(NH4+)>c(HCO3-)>c(H+)>c(OH-),D正确;
故选D。
考查方向
解题思路
A.该现象说明了NaHCO3溶解度相对与氯化铵等物质较小;
B.溶液中存在物料守恒,即:c(Na)=c(C),则:c(Na+)=c(HCO3﹣)+c(CO32﹣)+c(H2CO3),HCO3-水解程度大于电离程度;
C.根据电荷守恒,滤液中c(Na+)+c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-);
D.滤液中剩余的溶质主要是少量碳酸氢铵和氯化铵,铵根离子水解,浓度小于氯离子,但水解程度较小,仍然大于碳酸氢根离子,铵根离子水解大于碳酸氢根离子水解,溶液显酸性;
易错点
本题考查离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒即盐的水解原理的含义为解答关键,注意熟练掌握判断离子浓度大小常用方法,试题培养了学生灵活应用基础知识的能力。
知识点
12.A、B、C、D均属于短周期元素。A是元素周期表所有元素中原子半径最小的;B和C都只有两个电子层,B中一层电子数是另一层的两倍;C中两层电子数之和是两层电子数之差的两倍;D中一层电子数是另两层电子数之和。下列说法中正确的是
正确答案
解析
A、B、C、D均属于短周期元素。A是元素周期表所有元素中原子半径最小的,则A为H元素;B只有两个电子层,其中一层电子数是另一层的两倍,则B为C元素;C只有两个电子层,其中两层电子数之和是两层电子数之差的两倍,则C为O元素;D中一层电子数是另两层电子数之和,则D为S元素;据此解答各小题即可。A.元素的非金属性越强,简单离子的还原性越弱,O2-的简单离子的还原性小于S2-,A错误;
B.在自然界中硫的存在形式有游离态和化合态,单质硫主要存在于火山周围的地域中,以化合态存在的硫多为矿物,可分为硫化物矿和硫酸盐矿,B错误;
C.A元素所形成离子H-,核外电子排布和He原子相同,但核电荷数小,因此H-的半径有可能大于He原子的半径,C正确;
D.C、S的原子能相互结合形成化合物CS2,D错误。
故选C。
考查方向
解题思路
A、B、C、D均属于短周期元素。A是元素周期表所有元素中原子半径最小的,则A为H元素;B只有两个电子层,其中一层电子数是另一层的两倍,则B为C元素;C只有两个电子层,其中两层电子数之和是两层电子数之差的两倍,则C为O元素;D中一层电子数是另两层电子数之和,则D为S元素;据此解答各小题即可。A-H、B-C、C-O、D-S。
易错点
本题考查原子结构与元素周期律的关系,题目难度不大,正确推断元素的种类是解答本题的关键,要正确把握元素周期律的递变规律。
知识点
8.下列离子方程式中,正确的是
正确答案
解析
A.Na2O2是氧化物,在离子方程式中用化学式表示,即2Na2O2+2H2O=4OH-+O2↑,A错误;
B.次氯酸钙溶液中通入过量的CO2,生成碳酸钙和次氯酸,离子方程式为:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO,B正确;
C.碳酸氢钙溶液中滴入少量的NaOH溶液生成碳酸钙、碳酸钠和水,离子方程式为:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O,C错误;
D.硝酸铝溶液中加入过量氨水生成氢氧化铝,离子方程式为:Al3++3NH4OH=Al(OH)3↓+3NH4+,D错误。
故选B。
考查方向
解题思路
A.Na2O2是氧化物,在离子方程式中用化学式表示;
B.次氯酸钙溶液中通入过量的CO2,生成碳酸钙和次氯酸;
C.碳酸氢钙溶液中滴入少量的NaOH溶液生成碳酸钙、碳酸钠和水;
D.硝酸铝溶液中加入过量氨水生成氢氧化铝。
易错点
解题注意碳酸氢钙溶液中滴入少量的NaOH溶液生成碳酸钙、碳酸钠和水。
知识点
7.通常用于金属制品表面防腐的“银粉”,实际上是下列哪种金属的粉末
正确答案
解析
A.Al是银白色金属,表面可以形成一层致密的氧化膜,阻碍铝被进一步氧化,是常用于金属制品表面防腐的“银粉”,A正确;
B.Mg是银白色金属,易被空气中氧气氧化,不能用于金属制品表面防腐,B错误;
C.Cu是紫红金属,可以和空气中氧气、二氧化碳、水反应生成铜锈,不能用于金属制品表面防腐,C错误;
D.Au是金黄色金属,在空气中不能被氧化,但价格昂贵,不用于金属制品表面防腐,D错误;
故选A。
考查方向
解题思路
A.Al是银白色金属,表面可以形成一层致密的氧化膜,阻碍铝被进一步氧化;
B.Mg是银白色金属,易被空气中氧气氧化;
C.Cu是紫红金属,可以和空气中氧气、二氧化碳、水反应生成铜锈;
D.Au是金黄色金属,在空气中不能被氧化,但价格昂贵;
易错点
Mg也是银白色金属,但易被空气中氧气氧化,不能用于金属制品表面防腐,
知识点
碳的氧化物会对环境造成影响,但同时碳的单质、化合物又是重要的化工原料,是化学学科的重要研究对象。
18.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)=CH3OH(l) △H1=-128.5 kJ·mol-1
已知:CO(g)+1/2O2(g)=CO2(g) △H2=-283 kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) △H3=-285.8 kJ·mol-1
则用热化学方程式表示甲醇的燃烧热应为_____________。
19.科学家用X射线激光技术观察到了CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
①CO和O生成CO2是___________热反应;反应过程中,在催化剂作用下O与CO中的C逐渐靠近,最终形成的化学键类型属于_____________。
②结合已有知识和该反应过程,我们该如何理解,化学反应本质中的“分子破裂成为原子”这一观点?__________。
20.一定量的CO2与足量的C在体积可变的恒压密闭容器中反应:C(s)+CO2(g)
①550℃时的V逆________(填“大于”、“小于”或“等于”)925℃时的V逆。T℃时,若向平衡体系中充入惰性气体,化学平衡将_____________(填“向正反应方向”、“向逆反应方向”或“不发生”)移动。某同学是如何从图中数据,分析出该反应的正反应是吸热反应的?____________。
②650℃时,反应达平衡后CO2的转化率为_____________。
③若800℃时的压强为akPa,已知气体分压(p分)=气体总压(p总)×体积分数。800℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=________。
正确答案
CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) △H=-726.1 kJ·mol-1
解析
① CO(g)+2H2(g)=CH3OH(l) △H1=-128.5 kJ·mol-1
② CO(g)+1/2O2(g)=CO2(g) △H2=-283 kJ·mol-1
③ H2(g)+1/2O2(g)=H2O(l) △H3=-285.8 kJ·mol-1
根据盖斯定律,②-①+2③得甲醇燃烧的热化学方程式:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H2=-726.1 kJ·mol-1,甲醇的燃烧热应为-726.1kJ·mol-1。
考查方向
解题思路
根据盖斯定律,②-①+2③可以求出甲醇的燃烧热应为-726.1kJ·mol-1。
易错点
本题解题的关键是根据已知条件推理出未知结果,难度不大。
正确答案
①放 极性键(或共价键)
②参加反应的分子中,可能是部分分子破裂成为原子
解析
①根据能量--反应过程的图像知,状态I的能量高于状态III的能量,故CO和O生成CO2过程是放热反应;反应过程中,在催化剂作用下O与CO中的C逐渐靠近,最终形成的二氧化碳化学键类型属于极性共价键;
②通过上图,可以看见在化学反应中,并不是所有的分子都破裂成原子再重新组合成新的分子,因此化学反应本质中的“分子破裂成为原子”可以理解为:参加反应的分子中,可能是部分分子破裂成为原子;
考查方向
解题思路
①根据能量--反应过程的图像知,状态I的能量高于状态III的能量,故CO和O生成CO2过程是放热反应;反应过程中,在催化剂作用下O与CO中的C逐渐靠近,最终形成的二氧化碳化学键类型属于极性共价键;
②通过上图,可以看见在化学反应中,并不是所有的分子都破裂成原子再重新组合成新的分子,因此化学反应本质中的“分子破裂成为原子”可以理解为:参加反应的分子中,可能是部分分子破裂成为原子;
易错点
本题解题的关键是根据已知条件推理出未知结果,难度不大。
正确答案
①小于 向正反应方向 温度越高时,产物CO的体积分数越大
②25.0%
③ 12.4akPa
解析
①温度越高,化学反应速率越快,因此550℃时的V逆小于925℃时的V逆;
T℃时,若向平衡体系中充入惰性气体,各气体浓度不变,化学平衡将不发生移动;
温度越高,CO体积分数越大,温度升高,平衡向正反应方向移动,该反应的正反应是吸热反应;
②650℃时,反应达平衡后CO气体体积分数为40%,设650℃时,反应达平衡后CO2的转化率为x;
650℃时,反应达平衡后CO2的转化率为25%。
③800℃时,反应达平衡后CO气体体积分数为93%,Kp=(0.93akPa)2/0.07akPa=12.4akPa
考查方向
解题思路
①温度越高,化学反应速率越快;
T℃时,若向平衡体系中充入惰性气体,各气体浓度不变,化学平衡将不发生移动;
温度越高,CO体积分数越大,温度升高,平衡向正反应方向移动,该反应的正反应是吸热反应;
②650℃时,反应达平衡后CO气体体积分数为40%,设650℃时,反应达平衡后CO2的转化率为x,根据体积分数即可求出结果;
③800℃时,反应达平衡后CO气体体积分数为93%,Kp=(0.93akPa)2/0.07akPa=12.4akPa
易错点
本题解题的关键是根据已知条件推理出未知结果,难度不大。
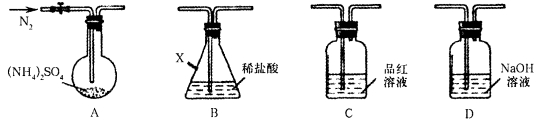
(NH4)2SO4俗称硫铵,常用作氮肥和化工原料。查阅资料发现(NH4)2SO4在260℃和400℃时分解产物不同。现选用下图所示装置进行实验(夹持和加热装置略)对其分解产物进行实验探究。
21.连接装置A—B—C—D,检查气密性,按图示加入试剂(装置B盛0.2000mol/L盐酸100.00mL)。通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2。品红溶液不褪色,取下装置B,加入指示剂,用0.1000mol/LNaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00 mL。经检验滴定后的溶液中无SO42-。
①仪器X的名称是___________。实验中开始加热后还要继续通入氮气的目的是___________。品红溶液不褪色和滴定后B的溶液中无SO42-,说明该条件下硫铵的分解产物除了NH3外还有______________。
②滴定前,要排尽滴定管尖嘴的气泡,其操作方法为___________。通过滴定测得装置B内溶液吸收NH3的物质的量是___________。
22.连接装置A—D—B,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
①若用HNO3酸化的Ba(NO3)2检验装置D内溶液中是否存在SO32-,是否合理,理由是______________。
②(NH4)2SO4在400℃分解的化学方程式是___________,单位物质的量的硫铵完全分解转移电子的物质的量为__________mol。
正确答案
①锥形瓶 将A中产生的气体全部排出,被后面装置中的试剂吸收 H2SO4
②大拇指和食指的指尖挤压玻璃球,并将尖嘴部分向上翘起 0.0175mol
解析
(NH4)2SO4俗称硫铵,常用作氮肥和化工原料。查阅资料发现(NH4)2SO4在260℃和400℃时分解产物不同。现选用下图所示装置进行实验(夹持和加热装置略)对其分解产物进行实验探究。连接装置A—B—C—D,检查气密性,按图示加入试剂(装置B盛0.2000mol/L盐酸100.00mL)。通入N2排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停止通入N2。品红溶液不褪色,取下装置B,加入指示剂,用0.1000mol/LNaOH溶液滴定剩余盐酸,终点时消耗NaOH溶液25.00 mL。经检验滴定后的溶液中无SO42-。
①仪器X的名称是锥形瓶。为了将A中产生的气体全部排出,被后面装置中的试剂吸收,实验开始加热后还要继续通入氮气。品红溶液不褪色和滴定后B的溶液中无SO42-,说明该条件下硫铵的分解产物除了NH3外还有H2SO4;
②滴定前,要排尽滴定管尖嘴的气泡,其操作方法为大拇指和食指的指尖挤压玻璃球,并将尖嘴部分向上翘起。通过滴定测得装置B内溶液吸收NH3的物质的量是0.2000mol/L×0.1L-0.1000mol/L×0.25L=0.0175mol。
考查方向
解题思路
①仪器X的名称是锥形瓶。为了将A中产生的气体全部排出,被后面装置中的试剂吸收,实验开始加热后还要继续通入氮气。品红溶液不褪色和滴定后B的溶液中无SO42-,说明该条件下硫铵的分解产物除了NH3外还有H2SO4;
②滴定前,要排尽滴定管尖嘴的气泡,其操作方法为大拇指和食指的指尖挤压玻璃球,并将尖嘴部分向上翘起。通过滴定测得装置B内溶液吸收NH3的物质的量是0.2000mol/L×0.1L-0.1000mol/L×0.25L=0.0175mol。
易错点
解题的关键是注意(NH4)2SO4在400℃分解,生成氨气、氮气、二氧化硫和水,在反应中,氮元素化合价上升,失去电子生成氮气;硫元素化合价降低,得到电子生成二氧化硫;3mol (NH4)2SO4分解3molSO2,得电子6mol。
正确答案
①不合理,因为无论溶液中存在SO32- 还是SO42- 均会产生同样的现象
②3(NH4)2SO4 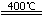
解析
(NH4)2SO4俗称硫铵,常用作氮肥和化工原料。查阅资料发现(NH4)2SO4在260℃和400℃时分解产物不同。现选用下图所示装置进行实验(夹持和加热装置略)对其分解产物进行实验探究。连接装置A—D—B,检查气密性,按图示重新加入试剂。通入N2排尽空气后,于400℃加热装置A至(NH4)2SO4完全分解无残留物,停止加热,冷却,停止通入N2。观察到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置D内溶液中有SO32-,无SO42-。进一步研究发现,气体产物中无氮氧化物。
①不能用HNO3酸化的Ba(NO3)2检验装置D内溶液中是否存在SO32-,因为无论溶液中存在SO32- 还是SO42- 均会产生同样的现象,生成白色沉淀;
②(NH4)2SO4在400℃分解,生成氨气、氮气、二氧化硫和水,化学方程式是3(NH4)2SO4 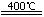
考查方向
解题思路
①不能用HNO3酸化的Ba(NO3)2检验装置D内溶液中是否存在SO32-,因为无论溶液中存在SO32- 还是SO42- 均会产生同样的现象,生成白色沉淀;
②(NH4)2SO4在400℃分解,生成氨气、氮气、二氧化硫和水,在反应中,氮元素化合价上升,失去电子生成氮气;硫元素化合价降低,得到电子生成二氧化硫;3mol (NH4)2SO4分解3molSO2,得电子6mol。
易错点
解题的关键是注意(NH4)2SO4在400℃分解,生成氨气、氮气、二氧化硫和水,在反应中,氮元素化合价上升,失去电子生成氮气;硫元素化合价降低,得到电子生成二氧化硫;3mol (NH4)2SO4分解3molSO2,得电子6mol。
【化学——选修2:化学与技术】
硅是无机非金属材料的主角,硅芯片的使用,促进了信息技术的革命。
23.陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了SiO2、Na2CO3外还有__________。玻璃制作过程中发生了Na2CO3+SiO2
24.工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
①请写出反应Ⅱ、Ⅲ的化学方程式:Ⅱ_________、Ⅲ___________。
②在流化床反应的产物中,SiHCl3大约占85%,所含有的其它物质的沸点数据如下表:
提纯SiHCl3的主要工艺操作依次是沉降、冷凝和分馏(相当于多次蒸馏)。沉降是为了除去____________;在空气中冷凝所得液体主要含有____________;若在实验室进行分馏提纯该液体,应该采取以下加热方法中的___________。
A.电炉加热
B.酒精灯加热
C.砂浴加热
D.水浴加热
③SiHCl3极易水解,其完全水解时的反应方程式为_____________。
正确答案
CaCO3 高温下Na2SiO3的稳定性比Na2CO3强
解析
陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了SiO2、Na2CO3外还有CaCO3。虽然碳酸酸性强于硅酸,但是高温下Na2SiO3的稳定性比Na2CO3强,因此玻璃制作过程中发生了Na2CO3+SiO2
考查方向
解题思路
陶瓷、水泥和玻璃都属于传统硅酸盐材料。其中,生产普通玻璃的主要原料除了SiO2、Na2CO3外还有CaCO3。虽然碳酸酸性强于硅酸,但是高温下Na2SiO3的稳定性比Na2CO3强;
易错点
本题考查硅酸盐工业,难度较小,主要考查学生对硅酸盐工业的了解,体现化学的社会作用,以识记为主,加强基础知识的掌握。
正确答案
①Si +3HCl 

②Si SiCl4和SiHCl3 D
③SiHCl3+4H2O =H4SiO4+ H2↑+3HCl↑(或H2SiO3)
解析
①工业上提纯硅有多种路线,其中一种工艺流程主要反应如下:2C+SiO2


②流化床反应是一种利用气体或液体通过颗粒状固体层而使固体颗粒处于悬浮运动状态,并进行气固相反应过程或液固相反应过程。在流化床反应的产物中,SiHCl3大约占85%,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和分馏(相当于多次蒸馏)。沉降是为了除去Si(固体);在空气中冷凝,SiCl4和SiHCl3液化;若在实验室进行分馏提纯该液体,温度在31.8-57.6℃之间,应该采取水浴加热方法加以分离,故选D;
③SiHCl3极易水解,其完全水解时生成H2、HCl、H2SiO3,反应方程式为SiHCl3+4H2O =H4SiO4+ H2↑+3HCl↑(或H2SiO3)。
考查方向
解题思路
①工业上提纯硅有多种路线,其中一种工艺流程主要反应如下:2C+SiO2


②流化床反应是一种利用气体或液体通过颗粒状固体层而使固体颗粒处于悬浮运动状态,并进行气固相反应过程或液固相反应过程。在流化床反应的产物中,SiHCl3大约占85%,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和分馏(相当于多次蒸馏)。沉降是为了除去Si(固体);在空气中冷凝,SiCl4和SiHCl3液化;若在实验室进行分馏提纯该液体,温度在31.8-57.6℃之间,应该采取水浴加热方法加以分离;
③SiHCl3极易水解,其完全水解时生成H2、HCl、H2SiO3。
易错点
本题考查硅酸盐工业,难度较小,主要考查学生对硅酸盐工业的了解,体现化学的社会作用,以识记为主,加强基础知识的掌握。
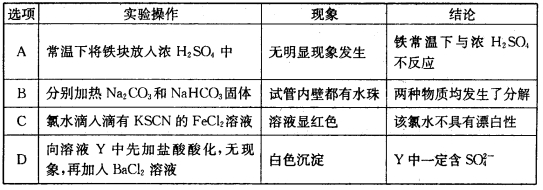
13.下列实验操作、现象和结论均正确的是
正确答案
D
解析
A.常温下,将铁块放入浓硫酸中,无明显现象,因为铁在浓硫酸中发生钝化现象,发生了化学反应,A错误;
B.碳酸钠加热不易分解,即使分解,也不会生成水,B错误;
C.氯水滴入含有KSCN的FeCl2溶液,氯水将亚铁离子氧化成三价铁离子,溶液变红色,显示了氯水的氧化性,不是漂白性,C错误;
D.向溶液Y中先加盐酸酸化,无现象,排除了银离子、碳酸根离子、亚硫酸根离子的干扰,再加入氯化钡溶液,产生白色沉淀,Y一定含硫酸根离子,D正确。
故选D。
考查方向
解题思路
A.常温下,将铁块放入浓硫酸中,无明显现象,因为铁在浓硫酸中发生钝化现象,发生了化学反应;
B.碳酸钠加热不易分解,即使分解,也不会生成水;
C.氯水滴入含有KSCN的FeCl2溶液,氯水将亚铁离子氧化成三价铁离子,溶液变红色,显示了氯水的氧化性,不是漂白性;
D.向溶液Y中先加盐酸酸化,无现象,排除了银离子、碳酸根离子、亚硫酸根离子的干扰。
易错点
本题考查化学实验方案的评价,为高频考点,把握物质的性质及发生的反应为解答的关键,涉及物质的检验、硝酸的性质、氧化还原反应等,综合性较强,题目难度不大。